Clear Sky Science · sv
Märkfri bestämning av massa och storlek för få-kDa biomolekyler med hierarkisk vision-transformer-förstärkt nanofluidisk spridningsmikroskopi
Se de minsta molekylerna
Många av kroppens viktigaste budbärare — såsom hormoner och immunsignaler — är så små att de nästan varit osynliga för kraftfulla mikroskop om de inte försetts med fluorescerande markörer. Dessa markörer kan förändra hur molekyler beter sig, en allvarlig nackdel för läkemedelsutveckling och grundläggande biologi. Denna studie presenterar ett sätt att väga och bestämma storleken på enskilda molekyler så små som insulin utan några markörer, genom att kombinera nanofluidiska chip och avancerad artificiell intelligens. Det öppnar en väg för att observera viktiga biomolekyler i deras naturliga tillstånd, en och en.
Mikrokanaler som reagensrör
I metodens kärna ligger nanofluidisk spridningsmikroskopi, som använder ett nagelstort chip etsad med extremt smala kanaler. Dessa kanaler är bara några tiotals nanometer över — tusentals gånger tunnare än ett människohår. Molekyler upplösta i en buffert driver fritt genom kanalerna i stället för att fastna på en yta. När chippet belyses med synligt ljus sprider både kanalväggarna och en passerande molekyl ljus. Eftersom kanalen är mycket större än molekylen interfererar deras spridda ljus på ett sätt som kraftigt förstärker molekylens optiska signatur. Genom att subtrahera bilder av en tom kanal från bilder tagna när en molekyl är närvarande får forskarna en film‑liknande registrering (en kymograf) av dess passage genom kanalen, innehållande information om både dess massa och hur snabbt den diffunderar.
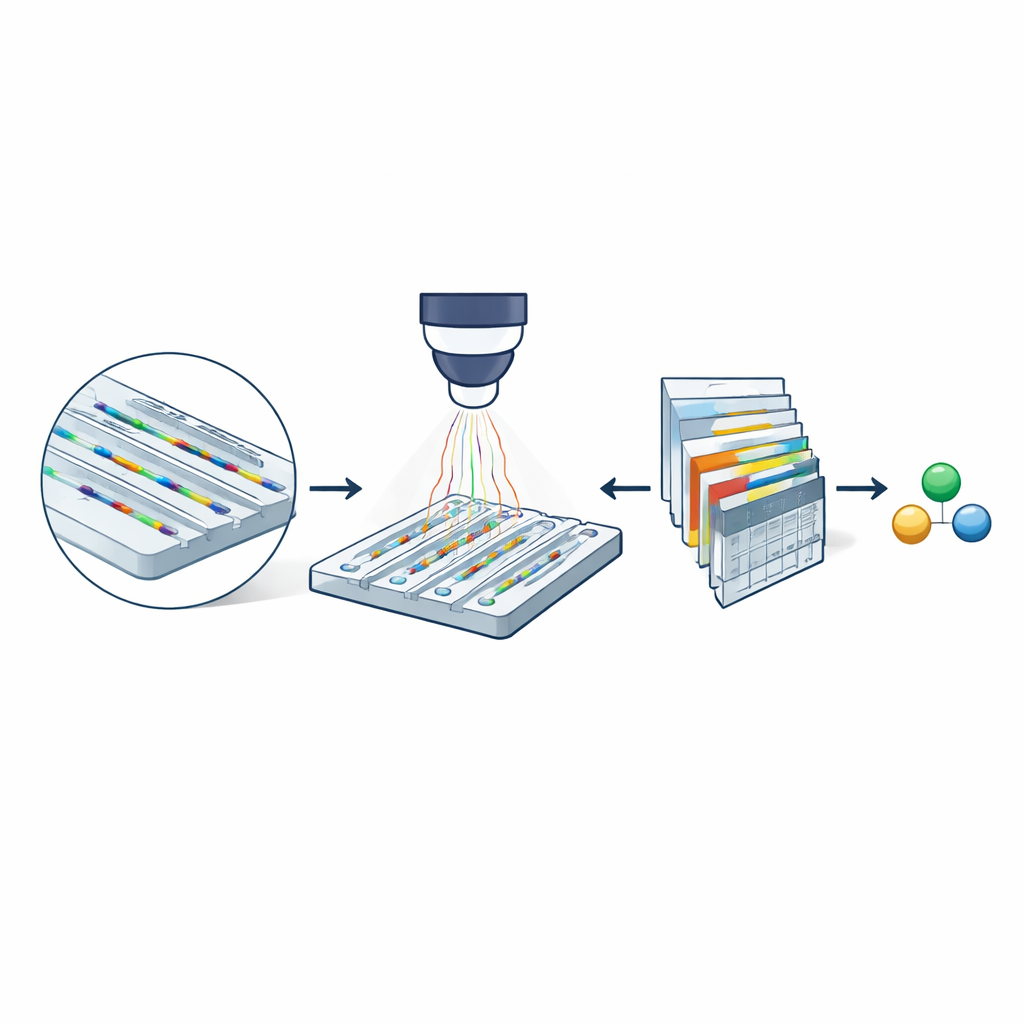
Varför smalare kanaler spelar roll
Även med denna optiska förstärkning kunde tidigare varianter av tekniken bara karakterisera molekyler tyngre än omkring 60 kilodalton — typiska stora proteiner — eftersom signaler från mindre arter drunknade i brus. Teamet visar att en minskning av nanochannelns tvärsnittsarea dramatiskt förbättrar känsligheten: den optiska kontrasten från en molekyl ökar när kanalarean minskar. Experiment som jämför två kanalstorlekar med proteinet bovint serumalbumin visar att dess bana är tydligt synlig i den smalare kanalen men nästan förlorad i den bredare. Denna enkla geometriska förändring antyder att i princip mycket mindre biomolekyler kan bli detekterbara om deras svaga signaler kan extraheras pålitligt från brusiga bildsekvenser.
Låta en AI läsa brusiga filmer
För att nå detta område utvecklade forskarna en specialiserad djupinlärningsmodell kallad hierarkisk vision-transformer. Istället för att försöka rekonstruera varje molekyls exakta spår pixel för pixel skannar modellen kymografen i flera skalor och producerar två utdata: en sannolikhetskarta som markerar var en molekyl sannolikt befinner sig i varje punkt i tid och rum, och en egenskapskarta som kodar uppskattningar av molekylvikt och hydrodynamisk storlek. Genom att vikta egenskapsuppskattningarna med sannolikhetskartan kan modellen ignorera regioner som mestadels är brus. Träningen bygger helt på simulerade banor lagda över experimentellt uppmätt bakgrundsbrus, vilket gör att systemet lär sig hur verkliga signaler bör se ut även när de knappt är synliga för ögat.
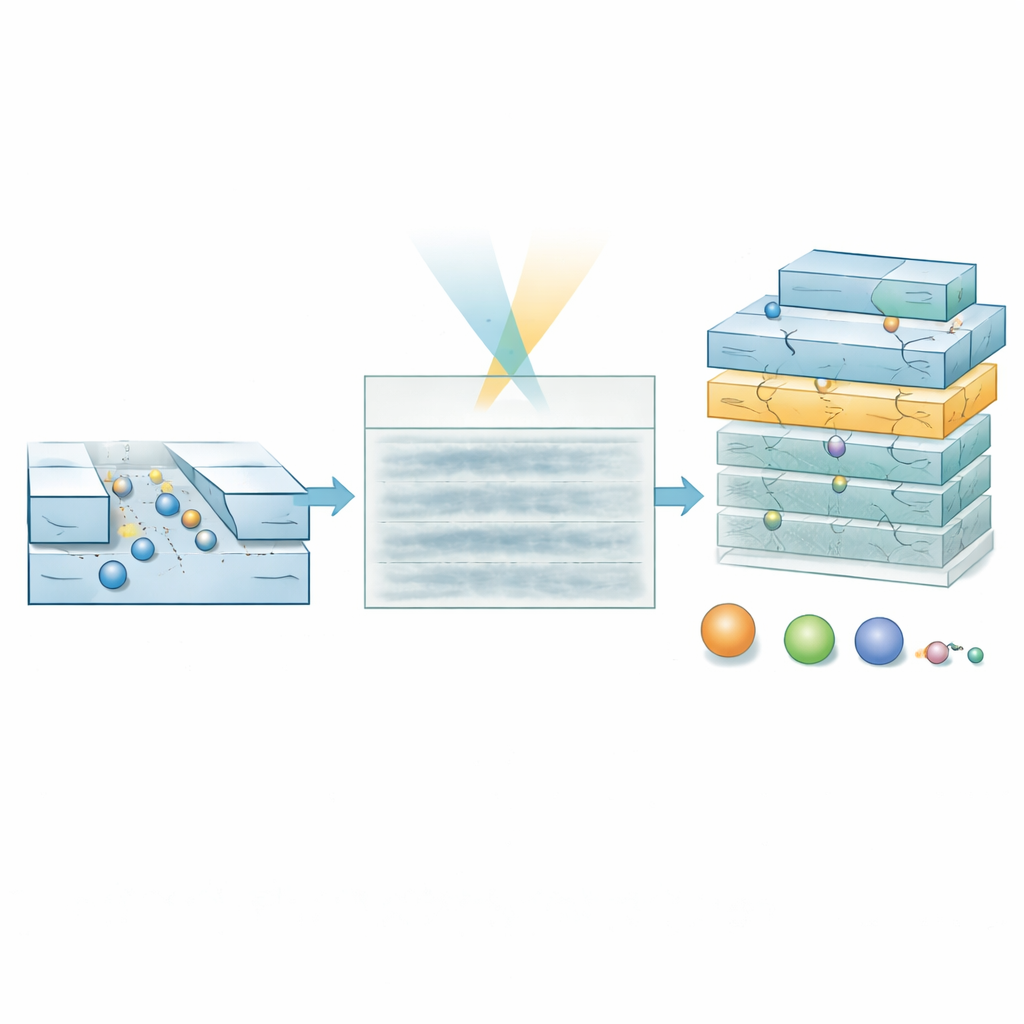
Testning på DNA och hormonmolekyler
Författarna validerade först tillvägagångssättet med en standard DNA‑"stege", en blandning av dubbelsträngade fragment med kända längder och massor, i relativt breda kanaler där alla fragment med avsikt ligger under den vanliga detektionsgränsen. I de råa filmerna syns inga tydliga DNA‑spår. Ändå producerar AI‑modellen sannolikhetskartor som korrekt framhäver var molekyler passerar och förutspår massor som matchar de förväntade värdena när lågkonfidensdata filtrerats bort. Metoden rapporterar också korrekt mindre effektiva storlekar för de styva, stavliknande DNA‑fragmenten än deras fulla fysiska längd, vilket återspeglar hur deras form påverkar diffusion. Det mest krävande testet använde ultrasmå kanaler för att studera peptidhormonet insulin, som väger endast omkring 5,8 kilodalton och är ungefär 1,5 nanometer över. Även här ser kymograferna funktionlösa ut, men modellen extraherar en snäv klusterbild av massa‑ och storleksvärden i utmärkt överensstämmelse med litteraturvärden, tydligt åtskilda från buffert‑kontroller.
Pressa mot gränserna
För att förstå hur långt denna strategi kan nå jämförde teamet modellens precision med Cramér–Rao‑lägre gräns, en statistisk gräns som definierar den bästa möjliga noggrannheten för varje orubblad estimator givet bruset i data. Med stora uppsättningar simuleringar visar de att när antalet ramar som bidrar till en molekyls bana ökar bortom ungefär tio tusen, närmar sig modellens uppskattningar av massa och storlek detta teoretiska optimum även för en sex‑kilodalton partikel. Experiment på insulin vid olika koncentrationer återger samma trend: längre effektiva banor ger mer precisa mätningar, begränsade främst av hur länge små, snabbt diffunderande molekyler stannar i synfältet. Författarna föreslår framtida strategier — såsom att försiktigt fånga molekyler i kanalerna eller återanvända data med bootstrap‑metoder — för att ytterligare öka användbar observationstid.
Vad detta betyder för biologi och medicin
I vardagliga termer visar detta arbete att det numera är möjligt att väga och bestämma storleken på några av kroppens minsta och viktigaste molekyler individuellt, utan att röra dem med fluorescerande taggar eller fästa dem på en yta. Genom att förena nanofabricerade kanaler med en specialbyggd AI som läser brusiga ljusspridningsfilmer sänker metoden massdetektionsgränsen för denna märkfria mikroskopiplattform med ungefär en faktor tio. Detta öppnar dörren för att studera familjer av små signalproteiner och peptidhormoner — såsom cytokiner, kemokiner och insulin — på enskildmolekylnivå, och för att karakterisera små biologiska nanopartiklar och läkemedelsbärare med oöverträffad känslighet. När tekniken mognar kan den bli ett kraftfullt verktyg inom läkemedelsupptäckt, diagnostik och grundläggande studier av hur molekylära interaktioner formar livet på de minsta skalorna.
Citering: K. Moberg, H., Yeroshenko, B., Fritzsche, J. et al. Label-free mass and size characterization of few-kDa biomolecules by hierarchical vision transformer augmented nanofluidic scattering microscopy. Nat Commun 17, 2533 (2026). https://doi.org/10.1038/s41467-026-70514-z
Nyckelord: märkningsfri enskildmolekylmikroskopi, nanofluidisk spridning, vision-transformer, små biomolekyler, insulindetektion