Clear Sky Science · sv
Ytans hydrofobicitet och styvhet bestämmer proteinkoronan på oralt administrerade nanopartiklar för behandling av kolit
Att förvandla piller till smartare behandlingar
Personer med inflammatoriska tarmsjukdomar som kolit tar ofta kraftfulla antiinflammatoriska läkemedel, men stor del av varje dos går förlorad eller ger biverkningar på andra håll i kroppen. Den här studien utforskar ett nytt sätt att få orala läkemedel att fungera mer som styrda projektiler: genom att konstruera små läkemedelsbärande partiklar som rekryterar kroppens egna tarmproteiner som ett naturligt riktmärke, vilket hjälper läkemedlen att hitta de immunceller som driver inflammation i tarmen.
Hur tarmen klär nanopartiklar
När vilken nanopartikel som helst kommer in i kroppen täcks den snabbt av ett tunt lager proteiner och bildar det forskare kallar en ”proteinkorona”. I en sjuk tarm ser denna korona mycket annorlunda ut än i frisk vävnad eftersom den lokala proteinblandningen har förändrats. Författarna fann tidigare att kolit ger upphov till en särskild intestinal korona som i viss mån styr partiklar mot immunceller kallade makrofager, som både driver och dämpar inflammation. Här försöker de aktivt forma den koronan genom att justera två grundläggande egenskaper hos läkemedelsbärande partiklar—deras vattenavstötning (hydrofobicitet) och deras styvhet—för att omvandla en måttlig, sjukdomsframkallad effekt till en stark riktstrategi.
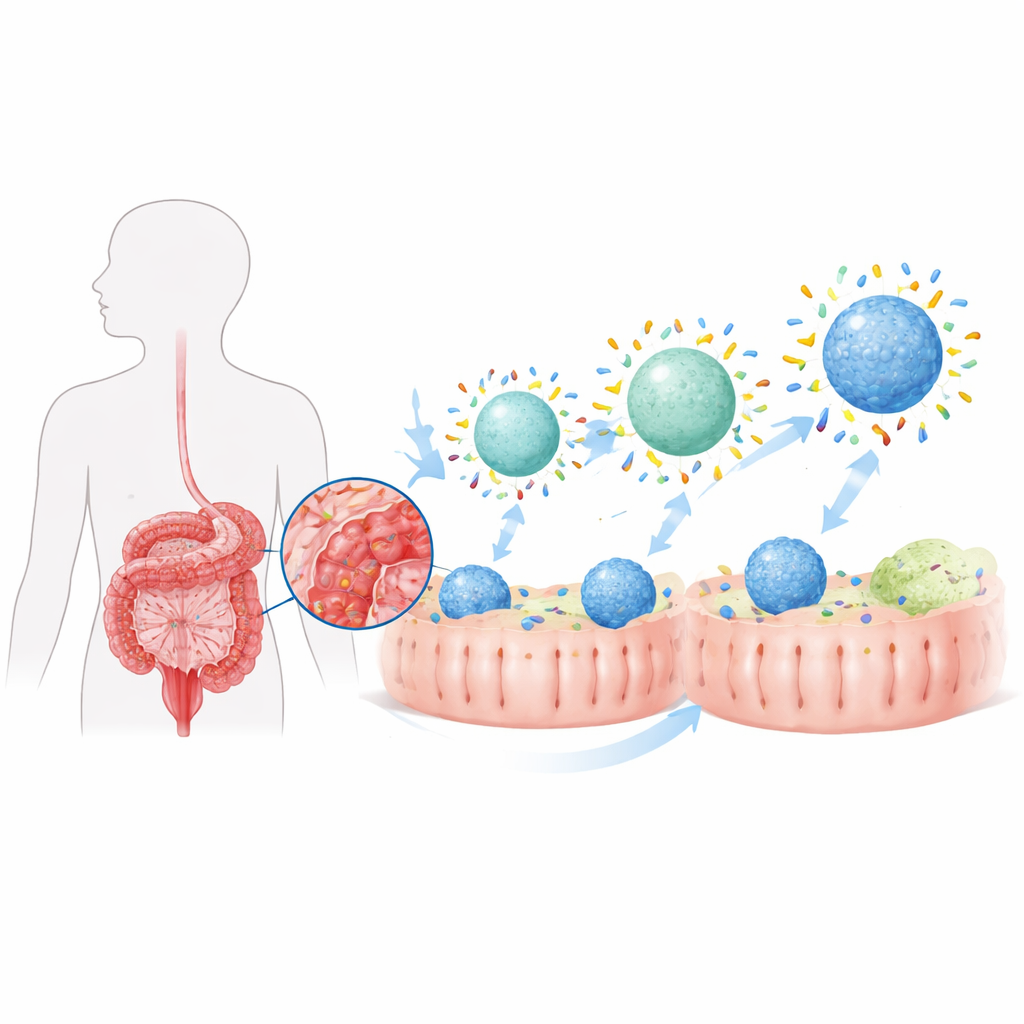
Göra partiklar mer attraktiva för proteiner
Teamet byggde lipidbaserade nanopartiklar liknande små fettblåsor och finjusterade hur vattenvänliga eller vattenavstötande deras ytor var genom att tillsätta olika mängder av en vanlig polymerbeläggning. Partiklar med mer hydrofobiska ytor band betydligt fler intestinala proteiner när de exponerades för kolitvätskor, både i djur och i provrör. När dessa ”fobiska” partiklar laddades med steroiden budesonid och gavs oralt till råttor med kolit levererade de mycket mer läkemedel till kolons makrofager än mer vattenälskande versioner. Som ett resultat återvann de behandlade djuren mer kroppsvikt, visade mindre förkortning och vävnadsskada i kolon och hade lägre nivåer av inflammatoriska molekyler i tarmen. Dock, trots förbättrad inflammation, återgick inte tarmen helt till ett friskt tillstånd, vilket tyder på att enbart ökad total mängd korona‑proteiner inte räckte.
Förstärka partiklarna för att välja bättre partner
För att driva konceptet längre behöll forskarna de hydrofobiska ytorna men ändrade den interna strukturen för att göra partiklarna mjuka, medelstora eller styva genom att fylla deras kärnor med plastkulor i olika storlekar. Alla tre plockade fortfarande upp liknande totala mängder intestinalt protein, men proteinblandningen förändrades. De styvaste partiklarna bildade koronor särskilt rika på proteiner som kan fästa vid receptorer på makrofager eller bära små näringsämnen som dessa celler tar upp. Ett sådant protein, S100A8, är rikligt i inflammerade tarmar och kan engagera specifika makrofagreceptorer. Blockering av S100A8 på koronan minskade markant upptaget av de styva partiklarna av makrofager, vilket avslöjade det som en nyckelkomponent för riktning vald av partikelns styvhet.
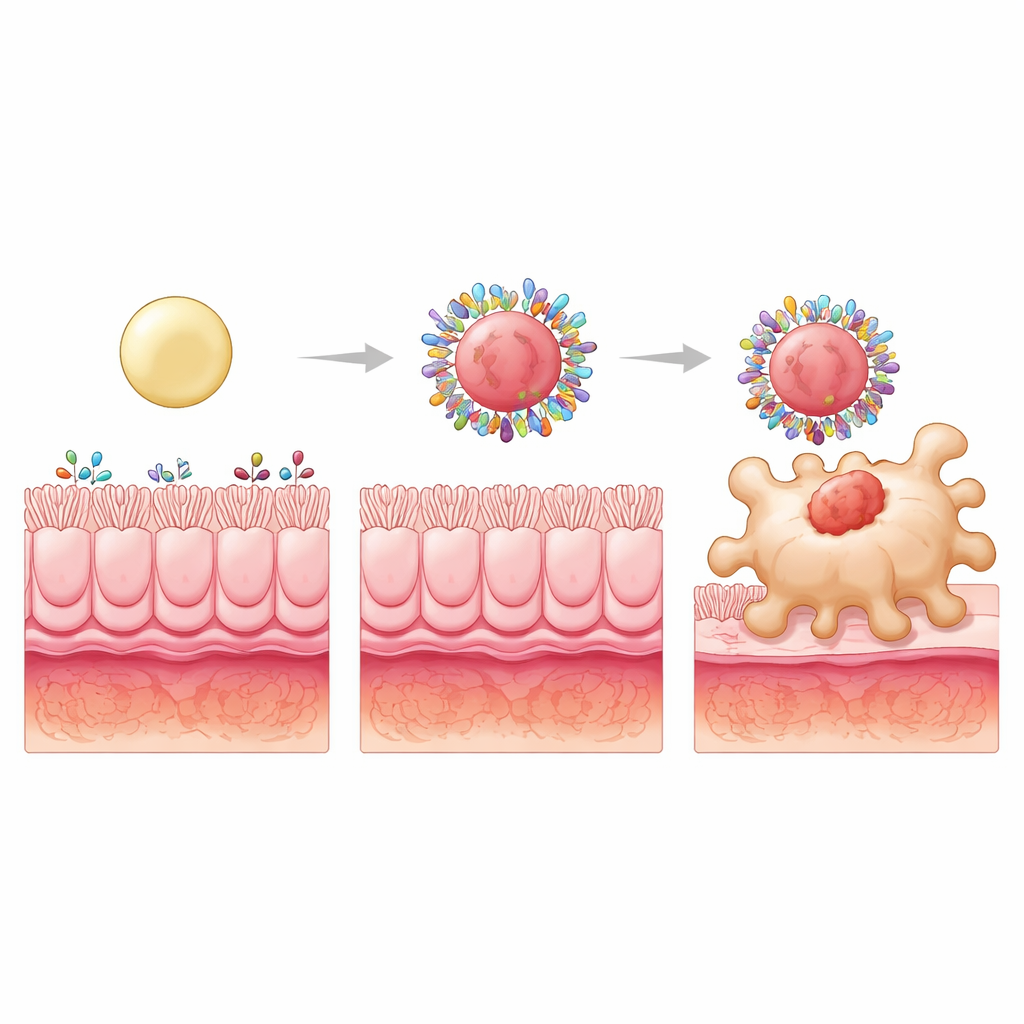
Från bättre riktning till bättre läkning
När budesonid packades i dessa höghydrofoba, högstyva partiklar och gavs oralt till råttor med kolit var fördelarna påtagliga. Den styva formuleringen minskade inte bara tarmsskada och oxidativ stress, utan normaliserade också flera inflammatoriska signaler till nivåer som sågs hos friska djur. Den återställde en hälsosammare balans mellan ”attack”‑ och ”lugna” makrofagtyper och ökade antalet regulatoriska T‑celler, som hjälper till att hålla immunsvaret i schack. Viktigt är att dessa vinster beroende på den sjukdomsändrade proteinmiljön i kolit; samma design visade ingen särskild riktning i friska råttor, vilket understryker att koronan är en dynamisk, sjukdomsspecifik medhjälpare.
Varför detta är viktigt för framtida läkemedel
Detta arbete visar att vi kan styra kroppens egna proteiner att fungera som smarta, självförnyande ”etiketter” på orala läkemedelsbärare helt enkelt genom att finjustera bärares ytoch mekaniska egenskaper. Genom att först öka proteinupptaget via hydrofobiska ytor och sedan använda styvhet för att gynna makrofag‑homande proteiner som S100A8 skapade forskarna nanopartiklar som naturligt söker upp de immunceller som driver kolit och levererar behandling där den behövs mest. Samma designlogik—att manipulera hur partiklar upplevs och beter sig vid tarmytan—kan anpassas till många typer av nanomediciner och sjukdomar och erbjuder en ny, mer subtil väg till riktad behandling utan att fästa på konstlade riktmolekyler.
Citering: Wu, J., Ni, M., Xing, L. et al. Surface hydrophobicity and rigidity determines protein corona on orally delivered nanoparticles treating colitis. Nat Commun 17, 2497 (2026). https://doi.org/10.1038/s41467-026-70453-9
Nyckelord: nanopartikeldrogering, inflammatorisk tarmsjukdom, proteinkorona, oral nanomedicin, makrofag‑inriktning