Clear Sky Science · sv
En släktövergripande interaktionsatlas över NS4B‑ortologer identifierar en konserved roll för UFMylering i ortoflavivirusreplikation
Varför denna virusstudie är viktig
Virus som dengue, Zika och West Nile sprider sig till nya områden och kan orsaka allt från feber till hjärninfektioner och fosterskador. Vi saknar dock fortfarande breda, tillförlitliga behandlingar. Denna studie undersöker hur ett dold samarbete mellan dessa virus och ett relativt okänt cellulärt märkningssystem kallat UFMylering hjälper patogenerna att föröka sig. Genom att kartlägga detta förhållande över många besläktade virus identifierar författarna en gemensam svag punkt som kan utnyttjas för att utveckla framtida antivirala läkemedel.
Följa en viktig viral insider
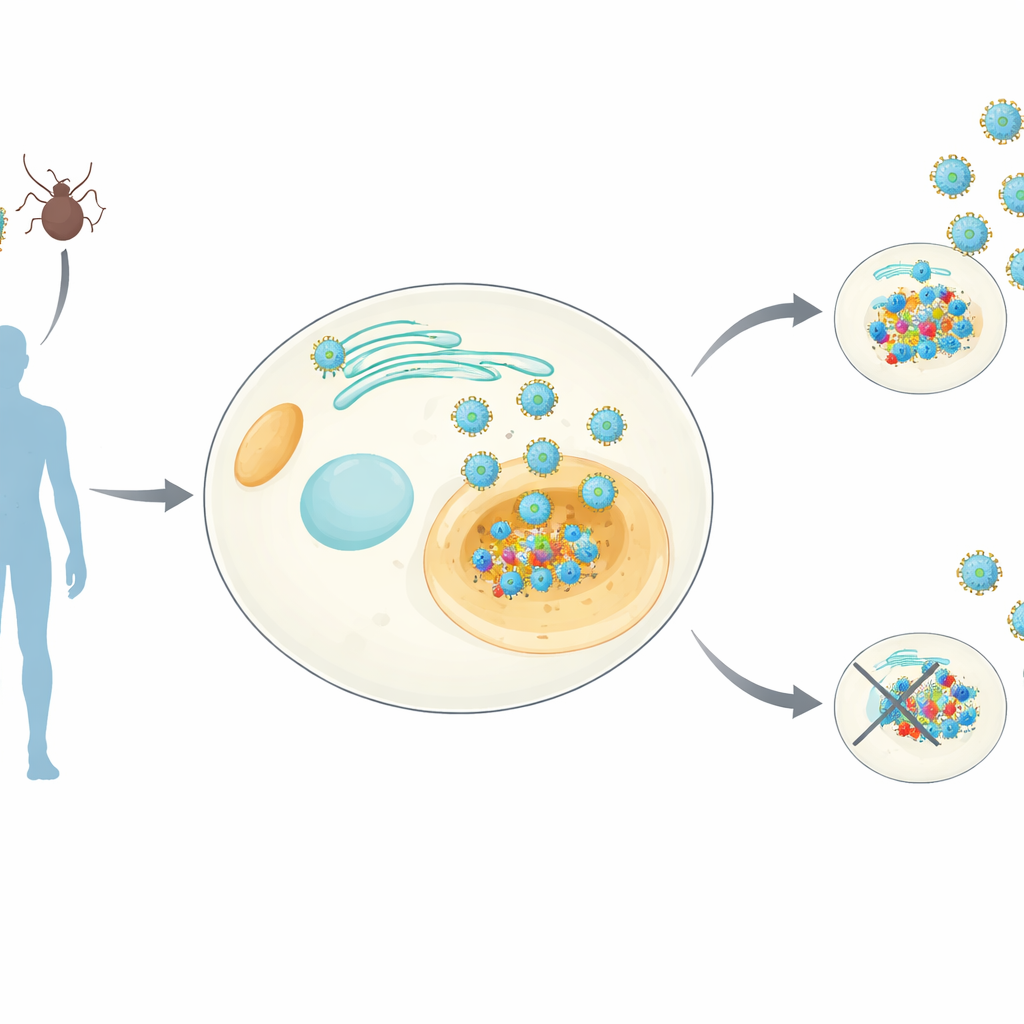
Orthoflavivirus – gruppen som inkluderar dengue, Zika, gula febern och andra – bär alla på ett litet protein kallat NS4B som lägger sig i membran inne i våra celler. NS4B är känt för att vara nödvändigt för viral replikation, men dess exakta funktioner har varit dunkla. Forskarna skapade humana cellinjer som stabilt uttrycker NS4B från åtta olika orthoflavivirus. De använde därefter känsliga masspektrometritekniker för att dra ner NS4B tillsammans med de mänskliga proteiner som satt fast vid det, och parallellt mätte de hur NS4B‑uttryck förändrar den totala blandningen av proteiner i cellen. Detta gav en släktövergripande ”interaktionsatlas” – som de kallar NS4Bome – som visar både gemensamma och virus‑specifika värdsmål.
Delade knep och skräddarsydda hack
Atlasen avslöjade 538 mänskliga proteiner som interagerar med NS4B och över 500 vars mängd förändras när NS4B är närvarande. Många av dessa är koncentrerade till vägar som hanterar energiproduktion i mitokondrierna, formningen av inre membran och transporten av nyproducerade proteiner och fetter. Vissa interaktioner delades av de flesta virus, vilket antyder evolutionärt bevarade knep som alla orthoflavivirus använder. Andra framträdde endast i vissa arter eller stammar, vilket potentiellt förklarar varför vissa virus föredrar myggor framför fästingar, eller orsakar hjärnsjukdom i stället för blödningsfeber. Denna systematiska överblick förvandlar en rörig samling tidigare, fragmentariska studier till en sammanhängande karta över hur dessa virus omprogrammerar cellen.
En överraskande allierad: UFMyleringssystemet
Bland de många partner som NS4B band till, stack en ut: UBA5, initieringsenzymet i UFMyleringsvägen. UFMylering är ett cellulärt system som fäster en liten proteintagg, UFM1, på utvalda mål och påverkar processer såsom proteinkvalitetskontroll och stressresponser. Med hjälp av RNA‑interferens och CRISPR‑baserade genutslag visade teamet att celler utan UBA5 eller annars oförmögna att utföra UFMylering hade kraftigt minskad replikation av Zika och flera närbesläktade virus. Återinförande av normalt UBA5 återställde virusets tillväxt, medan mutantformer som inte längre kunde driva UFMylering inte gjorde det, vilket bevisar att själva märkningsaktiviteten är avgörande för infektion.
Hur märkning stöder virala fabriker
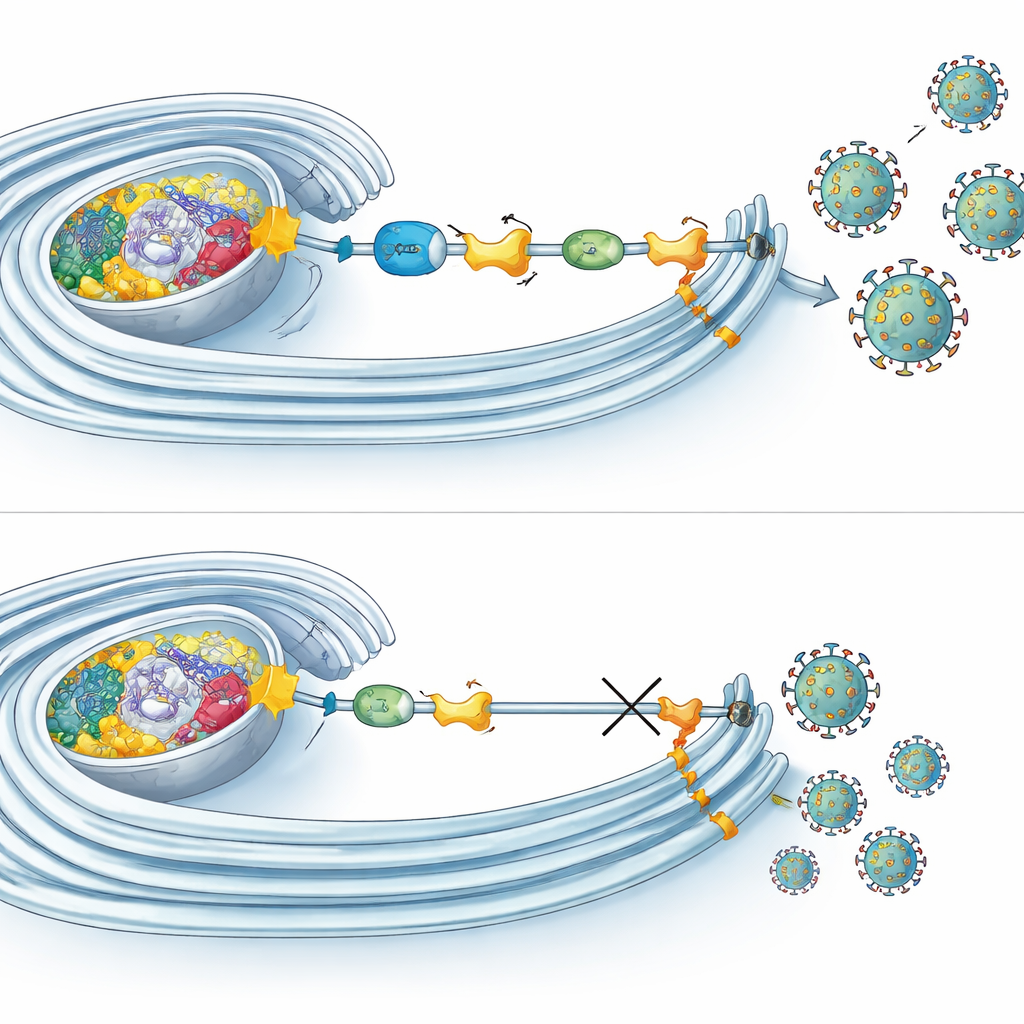
Mikroskopi och biokemiska experiment visade att flera UFMyleringskomponenter samlas på exakt de platser där viral RNA kopieras inne i omformade membran. Där associerar de inte bara med NS4B utan även med andra virala proteiner som bygger upp replikationsmaskineriet. Intressant nog stoppade inte blockering av UFMylering viral inträde, RNA‑produktion eller proteinsyntes. I stället förlamades främst sena steg i cykeln, såsom montering eller frisättning av infektiösa partiklar. Samtidigt visade sig UFMylering påverka hur mitokondrier andas: när vägen var inaktiverad visade cellerna minskad syreförbrukning och förändrade mitokondrieformer. I kontrast ökade mitokondriell respiration tidigt under Zika‑infektion, vilket tyder på att virus kan utnyttja UFMylering för att höja cellens energiutbyte just när de behöver det som mest.
Testa ett läkemedel i celler och små fiskar
Författarna vände sig sedan till en småmolekylförening, DKM 2‑93, som blockerar UBA5:s aktiva säte. I odlade humana celler minskade denna hämmare Zikavirusproduktion ungefär tiofaldigt vid doser som lämnade cellerna i stort sett friska, och visade aktivitet i flera celltyper. För att se om denna strategi kunde fungera i en levande organism använde de en zebrafiskmodell för Zika‑infektion, som efterliknar nyckelfunktioner av sjukdomen i den utvecklande hjärnan. Behandling av infekterade embryon med DKM 2‑93 under tidig hjärnutveckling sänkte signifikant nivåerna av viralt RNA och minskade andelen fiskar med svåra missbildningar, vilket indikerar verklig antiviral nytta in vivo.
Vad detta betyder för framtida behandlingar
Genom att bygga en omfattande karta över hur NS4B från många orthoflavivirus interagerar med mänskliga proteiner lyfter denna studie fram UFMylering som en bevarad hjälparväg som dessa virus är beroende av för att producera infektiösa partiklar. Eftersom samma värdsystem verkar stödja dengue, Zika, West Nile och andra, kan läkemedel som selektivt dämpar UFMylering fungera som bredspektrumantiviraler, snarare än att rikta in sig på ett virus i taget. Medan mer arbete behövs för att förstå exakt vilka proteiner som märks och för att säkerställa säkerhet, identifierar fynden ett lovande värdbaserat mål som en dag kan hjälpa till att dämpa utbrott av flera mygg‑ och fästburen sjukdomar med en enda terapeutisk strategi.
Citering: Rajasekharan, S., Barragan Torres, V.A., Pinheiro Gomes, Y.C. et al. A genus-wide interaction atlas across NS4B orthologues identifies a conserved role for UFMylation in orthoflavivirus replication. Nat Commun 17, 2489 (2026). https://doi.org/10.1038/s41467-026-70437-9
Nyckelord: Zikavirus, dengue, värd–virus‑interaktioner, UFMylering, bredspektrumantiviraler