Clear Sky Science · sv
Ribosomala modifieringar är kopplade till mesenkymal ödesval i den neurala krage-linjen
Hur små cellfabriker formar ansikten och tumörer
Våra ansikten och delar av nervsystemet byggs upp från en vandrande grupp embryonala celler som kallas neurala krageceller. Dessa celler kan omvandlas till ben, brosk, nerver med mera. Denna studie visar att deras val påverkas inte bara av gener utan av subtila kemiska justeringar av cellens proteintillverkande maskineri — ribosomer. Samma molekylära egenskaper som hjälper till att bygga ett normalt ansikte kan, när de felregleras, prägla farligare former av barncancer.
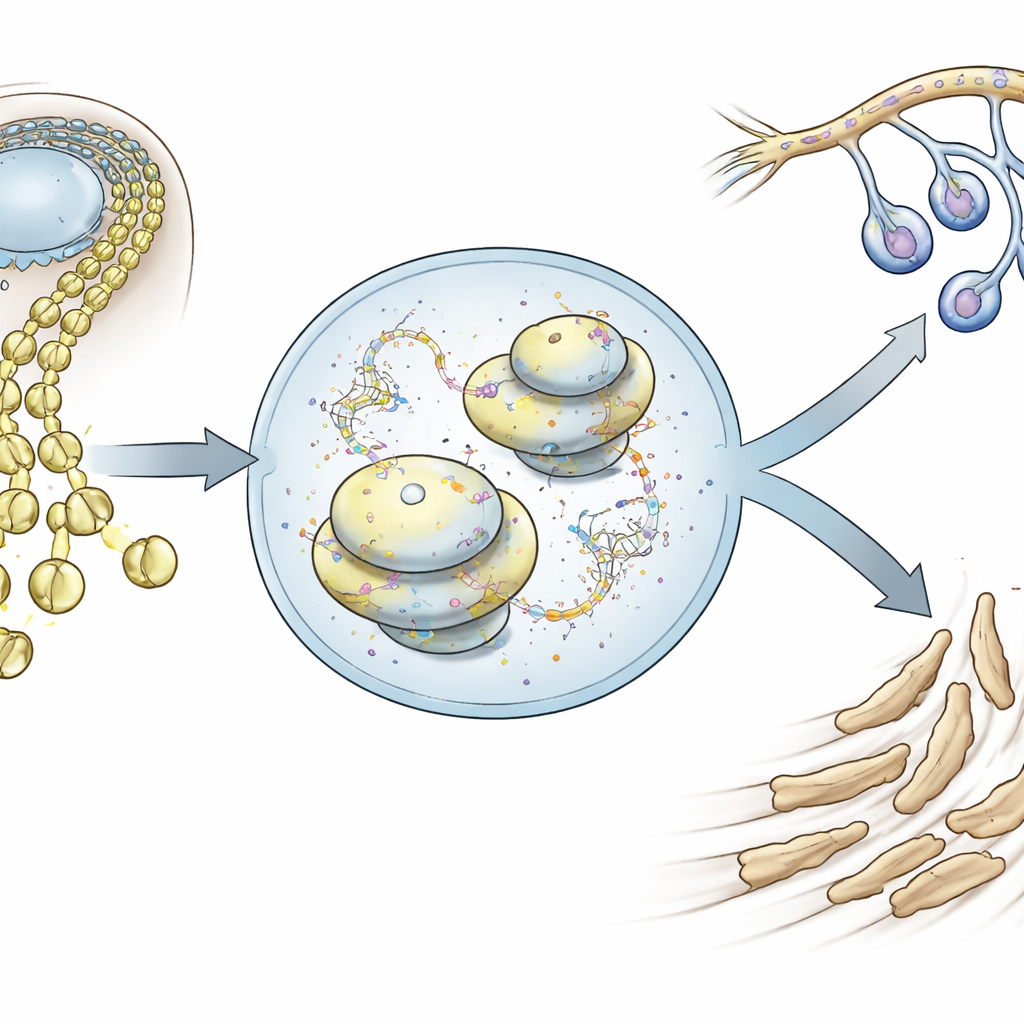
Formskiftande celler som bygger ansiktet
Neurala krageceller uppstår längs den tidiga hjärnan och ryggmärgen och migrerar sedan utåt, för att så småningom bilda stora delar av skallen, käkarna och perifera nerver. Med hjälp av enkelcells-RNA-sekvensering i mus-embryon följde författarna tusentals individuella kraniala neurala krageceller när de lämnade neuraltuben och flyttade in i ansiktet. De fann att redan mycket tidigt visar dessa celler en subtil lutning mot ett av två huvudsakliga öden: en mesenkymal bana som ska bilda ansiktets ben och brosk, eller en neuro-glial bana som ska bilda neuroner och gliaceller. Dessa två genaktivitetsprogram är initialt blandade i samma celler, men blir ömsesidigt uteslutande när utvecklingen fortskrider, vilket tvingar fram ett ödesbeslut.
Proteinfabriker som beslutsfattare
När teamet undersökte vilka gener som var kopplade till den tidiga biasen mot ansiktsmesenkym upptäckte de två huvudgrupper. Den ena innehöll välkända aktörer som driver celler att lösgöra sig, röra sig och ändra identitet — en process känd som epitel-till-mesenkymal transition. Den andra, mer överraskande gruppen kretsade kring ribosomuppbyggnad och kemisk modifiering av ribosomalt RNA, kärnan i det proteintillverkande maskineriet. Istället för att bara producera fler ribosomer slog de kraniala neurala kragecellerna på faktorer som finjusterar hur ribosomer byggs och kemiskt markeras. Att störa ribosomalt RNA-produktion i mus-embryon vid ögonblicket för ödesval påverkade i stort sett inte utvecklande nerver men hämmade kraftigt ansiktets skelettstrukturer, vilket visar att den mesenkymala vägen är särskilt beroende av denna ribosomala kontroll.
En speciell markering på ribosomalt RNA
Vid en djupare granskning fokuserade forskarna på en enda nukleotid i 18S-ribosomalt RNA, på en position avgörande för korrekt proteinsyntes. I kraniala neurala krageceller som var biaserade mot mesenkymala öden lästes detta läge upprepade gånger fel vid sekvensering — ett kännetecken för tung kemisk modifiering snarare än en verklig mutation. Tidigare arbete hade visat att en trio enzymer lägger till en sammansatt modifiering här genom flera steg. Genom att kombinera mänskliga genom- och RNA-data med massespektrometri av mus-embryonala vävnader bekräftade studien att denna position är normal i DNA:t men kemiskt förändrad i RNA:t i varierande grad, och att andelen modifierad form skiljer sig mellan hjärn- och ansiktsvävnader. Överuttryck eller utslagning av enzymerna som bygger denna modifiering i cellkulturer och i mus-embryon störde neuralkrageutvecklingen och gav påtagliga kraniofaciella defekter, vilket understryker att precisa nivåer av denna RNA-markör hjälper till att styra celler mot den skelettbildande banan.
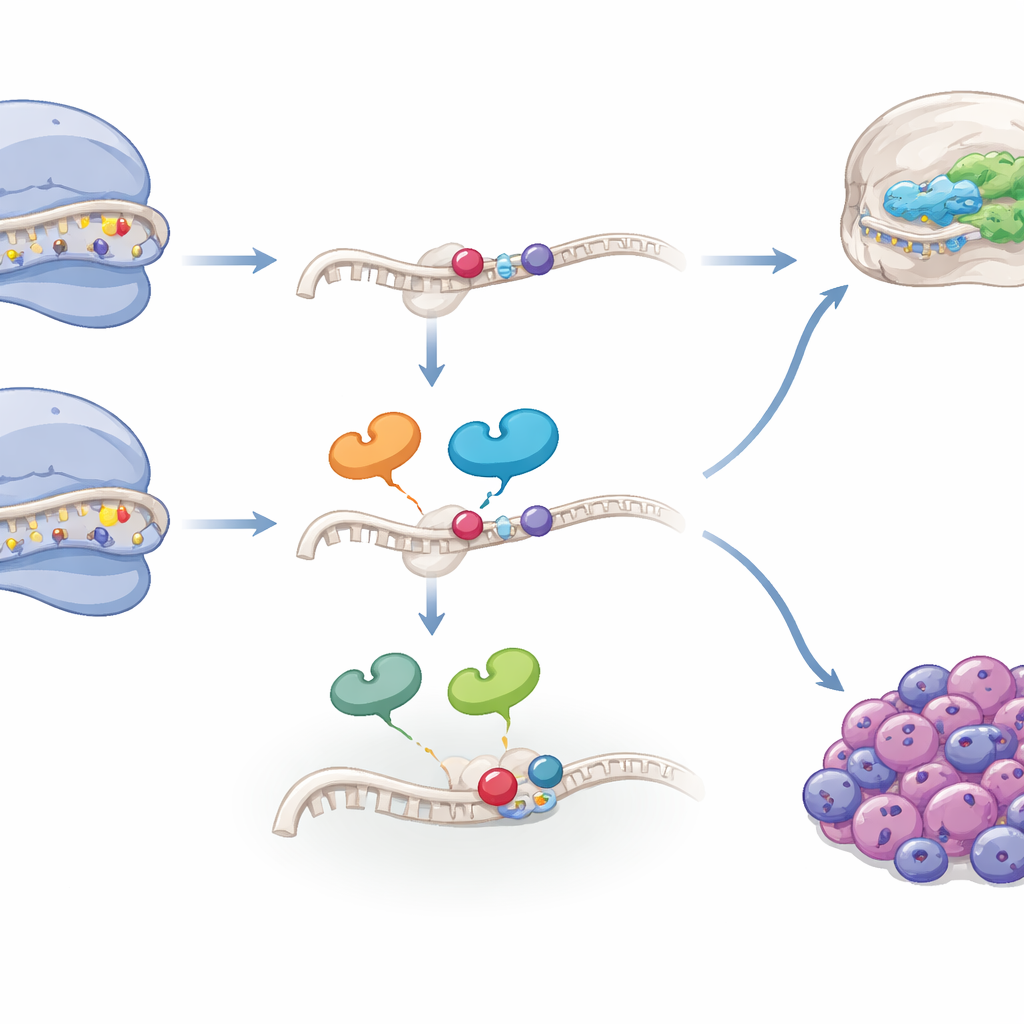
Från utveckling till cancerrisk
Eftersom neurala krageceller också kan ge upphov till tumörer såsom neuroblastom, undersökte författarna om samma ribosomala egenskaper återfinns i cancer. Genom att analysera enkelcells- och bulk-RNA-data från flera neuroblastom- och hjärntumörkohorter fann de att en ribosomal "kontroll- och RNA-modifierings"-gensignatur är berikad i tumörcellsubpopulationer med mer mesenkym-liknande drag — tillstånd ofta kopplade till behandlingsresistens och dålig prognos. I flera patientkohorter förutsåg höga nivåer av denna signatur starkt sämre överlevnad, särskilt i neuroblastomfall utan amplification av den välkända riskgenen MYCN. Specifika komponenter, såsom monteringsfaktorn WDR74 och modifieringsenzymet TSR3, var förhöjda i aggressiva cellinjer och gjorde dessa celler mer känsliga för läkemedel som stressar ribosomen. Intressant nog klarade sig tumörer med mycket låga eller mycket höga nivåer av den nyckel-RNA-modifieringen vid den framhävda positionen sämre än de med intermediära nivåer, vilket tyder på att både brist och överskott av denna specialiserade ribosompool kan vara skadligt.
Vad detta betyder för ansikten och barndomscancer
Tillsammans antyder dessa fynd att ribosomer inte bara är passiva proteinfabriker utan finjusterade enheter vars kemiska sammansättning hjälper bestämma hur embryonala celler bygger ansiktet och hur vissa tumörer beter sig. I neurala krageceller verkar en särskild kemisk markering på ribosomalt RNA gynna produktionen av proteiner som behövs för att bilda ansiktets ben och brosk, medan dess felreglering i cancer kopplas till farligare, formförändrande tumörceller. Att förstå och potentiellt rikta in sig på detta ribosomala ”finstilta” kan öppna nya vägar för att förebygga kraniofaciella missbildningar och för att identifiera eller behandla högrisk-neuroblastom.
Citering: Poverennaya, I., Murtazina, A., Li, L. et al. Ribosomal modifications are associated with mesenchymal fate selection in the neural crest lineage. Nat Commun 17, 2326 (2026). https://doi.org/10.1038/s41467-026-70375-6
Nyckelord: neuralkrageutveckling, ribosommodifieringar, kraniofaciell bildning, neuroblastom, specialiserade ribosomer