Clear Sky Science · sv
Kontroll av lysosomfunktion genom GTPas‑aktiverande proteinet TBC1D9B och dess bindningspartner TMEM55B
Hur cellernas återvinningscentraler håller balansen
Inuti varje cell finns små blåsliknande strukturer kallade lysosomer som fungerar som återvinningscentraler och kontrollnav för tillväxt. När de fungerar väl bryts utslitna delar ned och byggstenarna återanvänds; när de sviktar samlas avfall och sjukdomar, inklusive neurodegeneration och cancer, kan uppstå. Denna studie visar hur två relativt okända proteiner hjälper till att växla lysosomer mellan ett kringströvande, tillväxtvänligt tillstånd och ett klustrat, avfallsrensande läge, vilket ger insikt i hur celler anpassar sig vid överflöd och svält.
Att förflytta återvinningscentraler i cellen
Lysosomer är inte fasta på en plats. De rör sig längs interna spår, drivna utåt av ett motorpaket och inåt av ett annat. Var de befinner sig i cellen är väsentligt: när näringsämnen är rikliga sprider sig lysosomer mot cellens yttre regioner och hjälper till att understödja tillväxtsignaler; när maten är knapp drar de sig tillbaka mot mitten, blir mer sura och trappas upp i nedbrytningen av cellulärt material. Ett litet, brytare‑liknande protein kallat ARL8 är känt för att driva lysosomer utåt, men hittills hade ingen identifierat ett särskilt bromssystem som kan stoppa detta. Författarna misstänkte att en sådan broms är avgörande för att låta celler snabbt gå över i ett sparläge under svält.
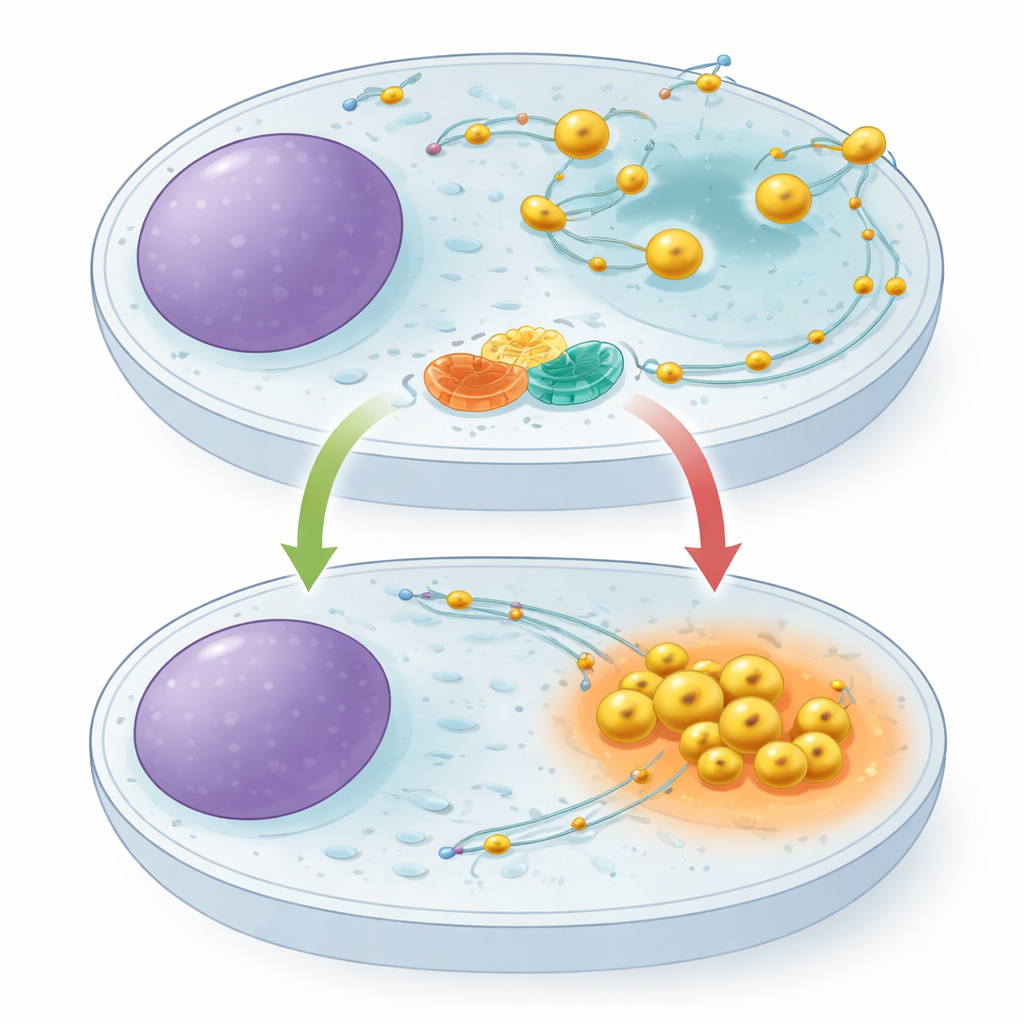
Partnerskap på lysosomens yta
Genom proteinfångstmetoder och masspektrometri upptäckte forskarna att ett protein som heter TBC1D9B fäster vid ett lysosomalt membranprotein kallat TMEM55B. TMEM55B sitter tvärs över lysosomens yttre membran, medan TBC1D9B till stor del är lösligt och kan docka vid membranet. Teamet visade att de två bildar ett direkt komplex: renat TBC1D9B binder till den exponerade delen av TMEM55B i provrör, och taggade versioner av proteinerna drar ner varandra från cellextrakt. Noggrann kartläggning av proteindelar visade att flera regioner av TBC1D9B kontaktar TMEM55B, vilket positionerar TBC1D9B på lysosomens yta utan att blockera den del av proteinet som är ansvarig för dess katalytiska aktivitet.
När bromsen fallerar springer lysosomerna lösa
För att ta reda på vad detta partnerskap gör använde författarna CRISPR‑redigering för att ta bort antingen TMEM55B eller TBC1D9B från humana celler. I båda fallen klustrades lysosomerna inte längre nära kärnan utan spreds istället mot cellkanten och rörde sig snabbare längs sina spår, vilket efterliknade celler i ett ständigt mättat tillstånd. Återinsättning av normalt TBC1D9B återställde korrekt positionering, men en version utan katalytisk förmåga gjorde det inte, vilket indikerar att dess enzymatiska aktivitet är väsentlig. När cellerna svalt drog kontrollcellerna in sina lysosomer och ökade deras nedbrytande kapacitet, visat av ökad aktivitet hos nyckelenzym och förbättrad nedbrytning av testlast. Celler utan TMEM55B eller TBC1D9B lyckades inte med detta: deras lysosomer förblev perifera och deras nedbrytande svar på svält var dämpat. Autofagi, processen där celler självät skadade komponenter, var också påverkad, med mindre effektiv bearbetning av en autofagirapportör och ackumulering av adapterproteinet p62.
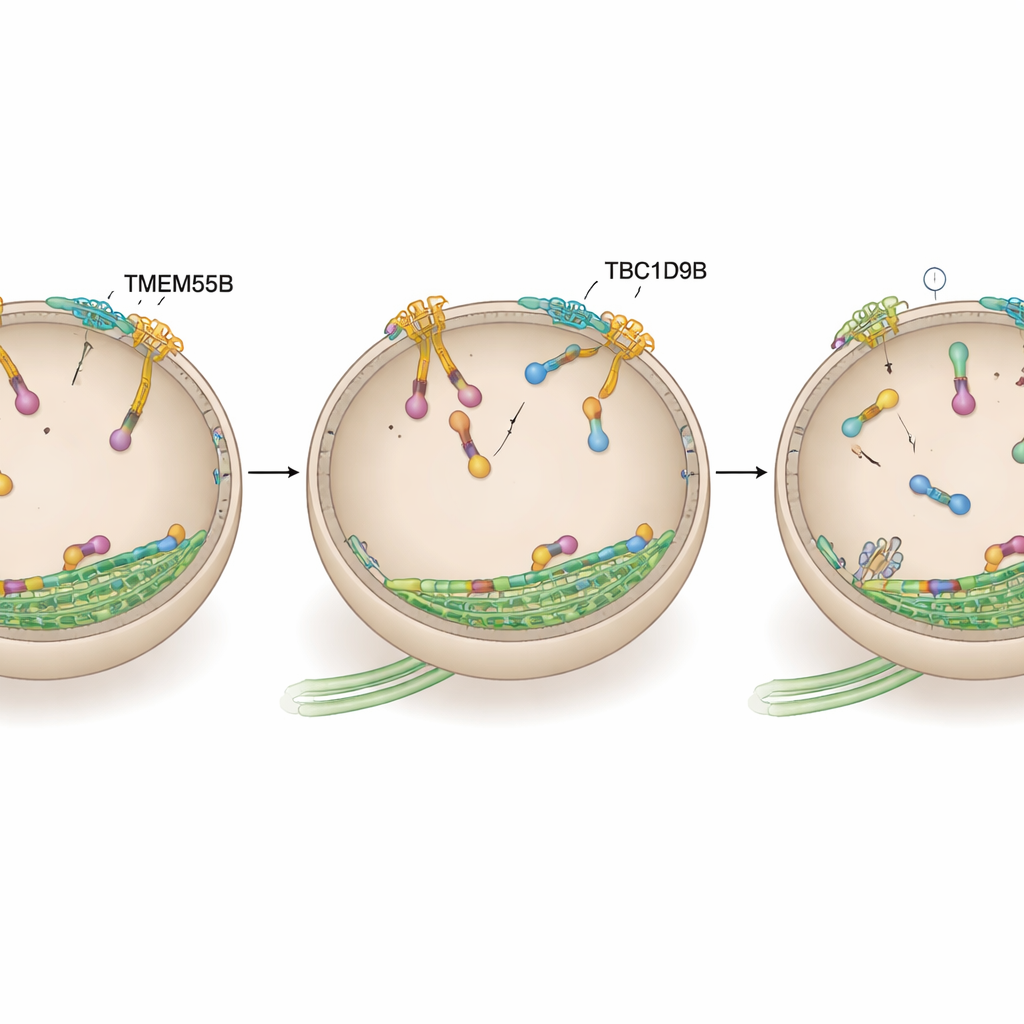
Att stänga av lysosommotorn
Teamet frågade sedan om TBC1D9B utövar sina effekter genom att verka direkt på ARL8, den motorbrytare som driver utåt. Genom närhetsmärkning i mänskliga neuroner och bindningstester i cellinjer och med renade proteiner visade de att TBC1D9B selektivt binder till den aktiva, GTP‑bundna formen av ARL8B‑varianten, men inte till dess inaktiva form eller till den nära besläktade ARL8A. Strukturell modellering förutsade att nyckelrester i TBC1D9B kontaktar GTP‑fickan i ARL8B. I biokemiska tester påskyndade TBC1D9B hydrolysen av GTP bundet till ARL8B, vilket effektivt omvandlade proteinet från dess "på"‑ till dess "av"‑tillstånd; en muterad version av TBC1D9B utan dessa rester kunde inte längre göra det. I linje med detta visade celler som saknade TMEM55B eller TBC1D9B ökad ARL8B på lysosomer, medan överuttryck av TBC1D9B drog lysosomer tillbaka mot cellcentrat, liknande en nedreglering av ARL8B‑aktivitet.
En ny kontrollknapp för cellernas hushållning
Slutligen testade författarna om denna ARL8B‑broms förklarar de cellulära förändringar som ses när TBC1D9B saknas. När ARL8B utplånades förblev lysosomerna klustrade nära kärnan oberoende av om TMEM55B eller TBC1D9B fanns, och defekterna i autofagi orsakade av TBC1D9B‑bortfall övervägdes i stor utsträckning. Tillsammans stöder data en modell där TMEM55B rekryterar TBC1D9B till lysosomer, där det inaktiverar ARL8B och tillåter lysosomer att växla från ett dispergerat, tillväxtstödjande tillstånd till ett centraliserat, nedbrytningsfokuserat. För icke‑specialister betyder detta att studien har avslöjat en viktig ratt som celler använder för att avgöra när de ska återvinna mer aggressivt, en process med implikationer för sjukdomar där avfall samlas i hjärnan, för ämnesomsättningen och för cancer.
Citering: Duhay, V., Tian, M., Kosieradzka, K. et al. Control of lysosome function by the GTPase-activating protein TBC1D9B and its binding partner TMEM55B. Nat Commun 17, 2487 (2026). https://doi.org/10.1038/s41467-026-70345-y
Nyckelord: lysosomer, autofagi, cellsignalering, organelletransport, neurodegeneration