Clear Sky Science · sv
Aktivering av NF-κB i astrocyter försämrar sårläkning efter traumatiska hjärnskador hos hanmöss
Varför hjärnkontusioner inte alltid läker snyggt
När någon får ett slag mot huvudet är den synliga skadan på utsidan bara en del av historien. Djupt inne i hjärnan utspelar sig ett komplext läkningssvar som kan avgöra om en person återhämtar sig väl eller utvecklar bestående problem med tänkande, humör eller rörelse. Denna studie i hanmöss avslöjar hur en central stressväg i stödjeceller kallade astrocyter kan förvandla ett normalt läkningssvar till ett som faktiskt förvärrar skadan efter en traumatisk hjärnskada.
Hjärnans dolda första insatser
Astrocyter är stjärnformade celler som omger nervceller och blodkärl och hjälper till att hålla hjärnans inre miljö stabil. Efter en skallskada ändrar de snabbt form och beteende, bildar en barriär runt det skadade området och hjälper till att återuppbygga vävnad. Forskarna fokuserade på en molekylär brytare inne i dessa celler kallad NF-κB, som är välkänd för att reglera inflammation i många vävnader. De frågade om denna brytare efter en sluten skallskada, liknande vanliga mänskliga hjärnskakningar och kontusioner, hjälper eller skadar hjärnans förmåga att läka.
En stressbrytare som tänds efter påverkan
Genom att analysera genaktivitet i musens hjärnvävnad efter skada fann teamet en våg av gener kopplade till inflammation och NF-κB-signalering, särskilt tre till sju dagar efter traumat, när sekundära skador ökar. Med hjälp av rapportermöss visade de att NF-κB-aktivering inte spreds över hela hjärnan utan koncentrerades kring slaggplatsen. Där var den särskilt aktiv i mikroglia (hjärnans immunsoldater) och i astrocyter som bildade sårets gräns. Denna tidpunkt och lokalisation tyder på att NF-κB i astrocyter kan vara en avgörande regulator för hur hjärnan organiserar sin ärrbildning och kontrollerar immunresponsen.
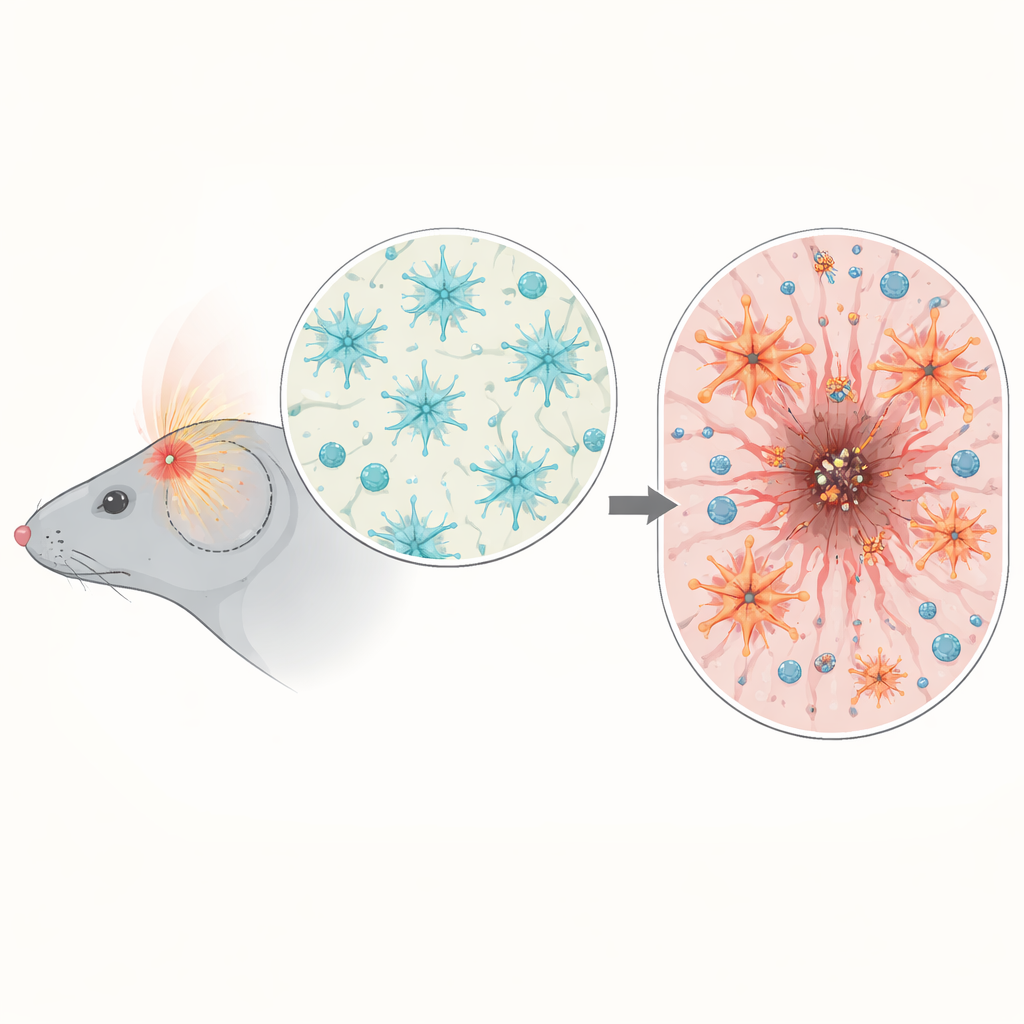
När astrocyter skruvas upp för långt
För att testa orsak och verkan skapade forskarna möss där NF-κB i astrocyter antingen konstgjort ökats eller dämpats, men först efter att hjärnans utveckling var färdig. När dessa möss utsattes för huvudtrauma förlorade de med överaktivt NF-κB i astrocyterna mer vikt, visade sämre tidiga neurologiska poäng och hade större, mer långlivade hjärnläsioner i både vävnadssektioner och på MRI-bilder. I stället för att bilda ett prydligt, välavgränsat ärr som avgränsade den skadade kärnan, producerade deras astrocyter en tjock, oorganiserad gräns som inte krympte såret över tid. Den normala balansen av stödjande matrixproteiner runt skadan stördes, och en viktig yttre barriärstruktur känd som glial limitans bildades dåligt, vilket lämnade den omgivande hjärnan mindre skyddad.
När läkningsprogrammen spårar ur
Teamet gick in på molekylär nivå och isolerade astrocyter och närliggande immunceller för gen-för-gen-analys. Hos friska djur undertrycker skada normalt vissa dagliga husfunktioner hos astrocyter samtidigt som gener som stödjer sårslutning och regeneration sätts på. I kontrast såg astrocyter med kroniskt aktivt NF-κB redan “skadade” ut även före traumat, och efter påverkan lyckades de inte fullt ut aktivera fördelaktiga reparationsprogram som är kopplade till en kontrollerad omvandling som hjälper celler bygga en effektiv gräns. I stället favoriserade de kraftigt inflammatoriska gener, antog drag av ett toxiskt astrocyttillstånd kopplat till åldrande och neurodegenerativ sjukdom och visade tecken på en “senescensliknande” sekretorisk profil förenlig med kroniska, icke-läkande sår.
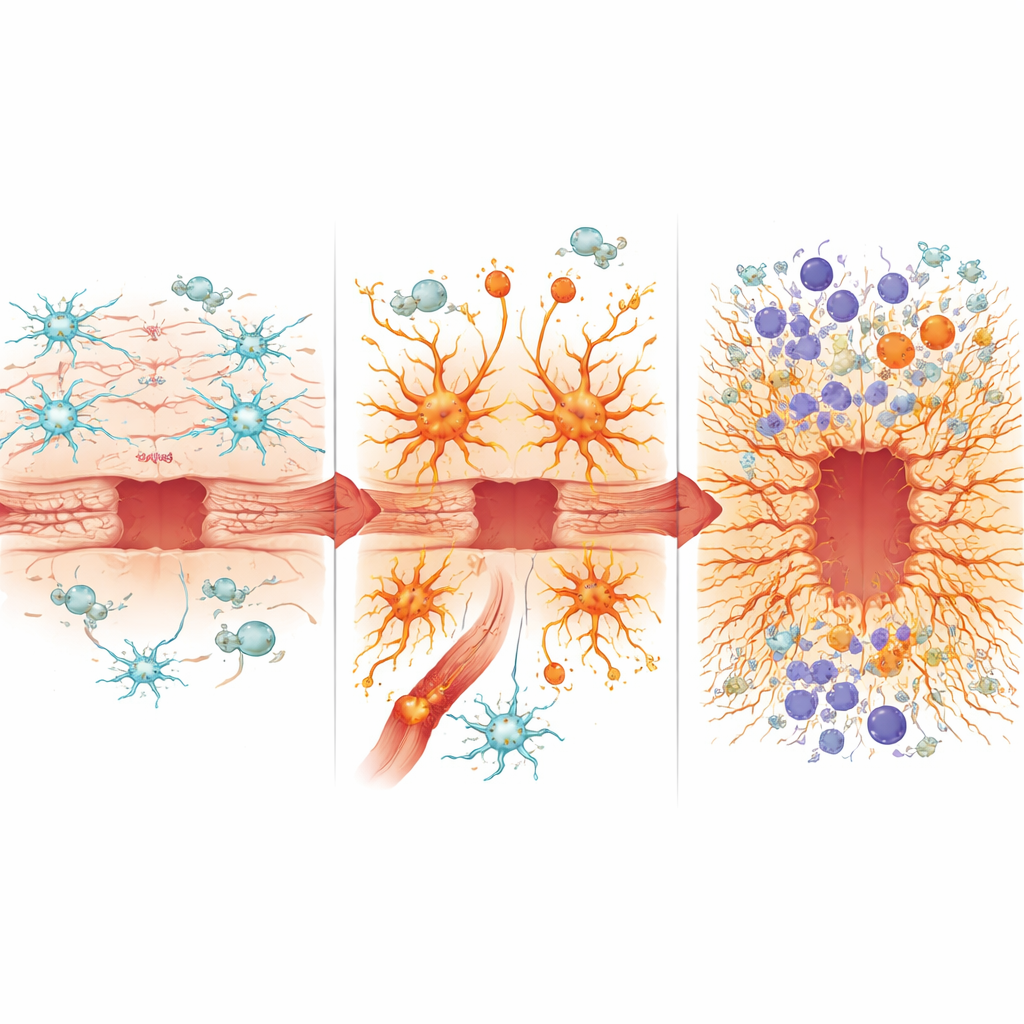
Att elda på immunsvaret
Dessa felprogrammerade astrocyter omformade också hjärnans immunlandskap. Blod–hjärn-barriären blev mer läckande och släppte in fler perifera immunceller. Möss med överaktivt NF-κB i astrocyter visade kraftigare infiltration av inflammatoriska myeloida celler och förändrade blandningar av neutrofiler, monocyter och dendritiska celler, samt ökade mängder cytotoxiska T‑celler som kan skada vävnad ytterligare. Immunceller i denna miljö uttryckte starkare signaler drivna av interferon- och inflammasomvägar, båda förknippade med aggressiv, potentiellt neurotoxisk inflammation. Samtidigt minskade nivåerna av flera skyddande eller reparationsfrämjande proteiner, såsom osteopontin, medan andra kopplade till oxidativ stress, järnöverskott och ärrbildning, inklusive heme oxygenase-1 och lipocalin‑2, ökade. Kvoten mellan osteopontin och lipocalin‑2 framträdde som en enkel markör som korrelerade med bättre eller sämre läkning i de olika musstammarna.
Vad detta betyder för återhämtning efter huvudskador
Tillsammans visar resultaten att när NF-κB-stressvägen i astrocyter är kroniskt uppreglerad, skiftar dessa celler från att stödja organiserad reparation till att driva kaotisk ärrbildning och långvarig inflammation. I stället för att bygga en ren gräns som innehåller skadan och möjliggör vävnadsremodellering bidrar de till en läckande, inflammatorisk nisch som förstorar lesionen och försämrar långsiktigt utfall. Även om arbetet gjordes på hanmöss pekar det på astrocytärt NF-κB som ett lovande mål för terapier som syftar till att förbättra återhämtning efter traumatisk hjärnskada och antyder att blodnivåer av molekyler som osteopontin och lipocalin‑2 en dag kan hjälpa kliniker att övervaka hur väl en patients hjärna läker.
Citering: Hein, T.M., Nespoli, E., Hakani, M. et al. NF-κB activation in astrocytes impairs wound healing after traumatic brain injury in male mice. Nat Commun 17, 2323 (2026). https://doi.org/10.1038/s41467-026-70304-7
Nyckelord: traumatisk hjärnskada, astrocyter, neuroinflammation, bildning av hjärnsår, NF-kappa B