Clear Sky Science · sv
Mechanismer för hämning av PfDNMT2 och PfATP6‑medierad resistens mot malariakandidaten SC83288 i Plasmodium falciparum
Varför detta är viktigt för malaria
När malariaparasiter utvecklar resistens mot dagens läkemedel får läkare färre behandlingsalternativ för en sjukdom som fortfarande dödar hundratusentals människor varje år, främst små barn. Denna studie dissekerar hur ett lovande experimentellt läkemedel, kallat SC83288, angriper den dödligaste malariaparasiten och hur parasiten ibland lyckas försvara sig. Att förstå både läkemedlets angrepp och parasitens motangrepp är avgörande för att kunna utveckla SC83288 till en framtida behandling som förblir effektiv så länge som möjligt. 
Ett nytt vapen mot en dödlig parasit
SC83288 har vuxit fram ur arbete för att förbättra ett gammalt veterinärläkemedel och framstår nu som en kraftfull antimalariakandidat. I laboratorietester och djurmodeller rensar det snabbt malariaparasiter ur blodet vid mycket låga koncentrationer, inklusive stammar som redan är resistenta mot förstahandsbehandlingar som artemisinin‑baserade kombinationer och äldre läkemedel som antifolater och kinoliner. Det verkar också på de parasitstadier som kan överföras till myggor. Omfattande säkerhetstester i djur har hittills inte visat några stora varningsflaggor, vilket placerar SC83288 som en realistisk kandidat för kliniska prövningar på människor.
Hur läkemedlet slår ut parasitens tillväxt
Forskarna följde parasitens 48‑timmarscykel inne i röda blodkroppar och tillsatte SC83288 vid olika tidpunkter. När läkemedlet fanns närvarande under de första två tredjedelarna av denna cykel slutade parasiterna kopiera sitt DNA och misslyckades med att dela sina cellkärnor, en process som kallas karyokines. Under mikroskop blev behandlade parasiter små och kondenserade, ett kännetecken för döende celler, medan senare steg såsom uppdelning i dotterparasiter och utsprängning ur den röda blodkroppen inte påverkades om delningen redan var slutförd. Detta pekade ut SC83288:s huvudverkan till det kritiska fönstret när parasitens genetiska material dupliceras i förberedelsen för att bilda många avkommor.
Att slå mot parasitens ”epigenetiska” kontrollcenter
För att förstå vad SC83288 träffar inne i parasiten kombinerade teamet genuttrycksprofilering, metaboliska mätningar och direkta enzymtester. De fann tydliga tecken på att läkemedlet stör hur parasiten använder små kemiska markörer för att kontrollera DNA och RNA. Nivåerna av en viktig donormolekyl för dessa markörer, S‑adenosylmetionin, blev obalanserade, och globala märken på DNA och RNA sjönk kraftigt efter behandling. Med fokus på ett centralt enzym, PfDNMT2, som normalt lägger till metylgrupper både på DNA och på en specifik transfer‑RNA, visade forskarna att SC83288 direkt hämmar dess aktivitet i provrör och i parasiter. När parasiter var konstruerade för att producera mycket mer PfDNMT2 blev de mindre känsliga för läkemedlet, medan extra tillgång på metyldonormolekyler delvis räddade parasiter från SC83288:s effekter. Tillsammans stöder dessa resultat en modell där SC83288 dödar genom att undergräva parasitens epigenetiska och genuttrycks‑maskineri, vilket leder till avstannad DNA‑replikation och celldöd. 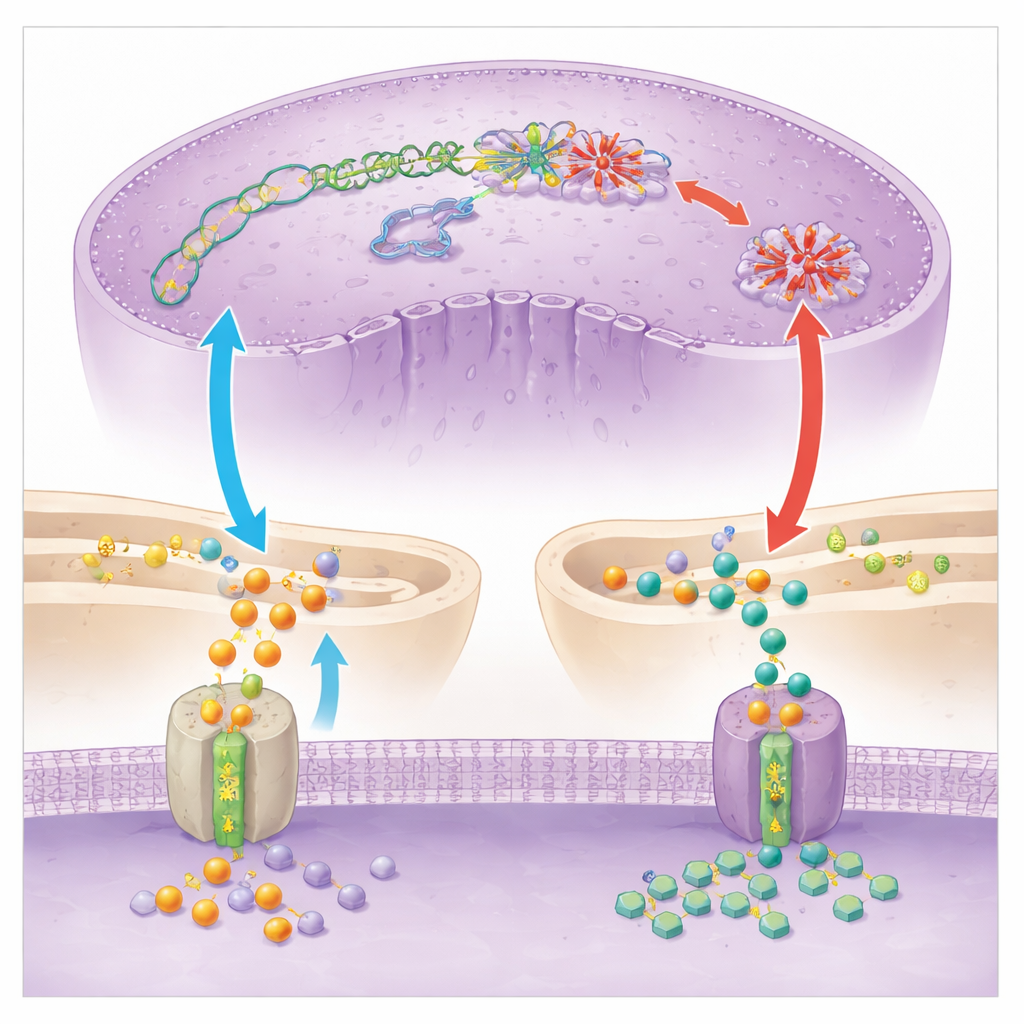
Hur parasiten undviker smällen
Inget potent läkemedel kommer utan risk för resistens, och SC83288 är inget undantag. Efter långvarig exponering i odling förvärvade vissa parasitlinjer förändringar inte i målenzymet PfDNMT2, utan i en membranpump kallad PfATP6, som normalt hjälper till att kontrollera kalciumnivåerna inne i parasitens endoplasmatiska retikulum, ett nätverk av interna membran. Med hjälp av genetisk modifiering införde teamet en av dessa mutationer i en standardparasitstam och visade att den gjorde parasiterna omkring tusen gånger mindre känsliga för SC83288. Detaljerade transportexperiment i jäst och i parasiter, liksom avbildning med en klickbar fluorescerande version av läkemedlet, visade varför: mutant PfATP6 fungerar som en dammsugare och drar SC83288 bort från kärnan och in i det endoplasmatiska retikulumet. Läkemedlet tar sig fortfarande in i infekterade röda blodkroppar, men blir nu sequestrerat i ett fack där det har mindre påverkan på nukleära processer.
Det dolda priset för resistens
Även om PfATP6‑mutationen skyddar parasiter från SC83288 kommer det till ett högt pris. Resistentaparasiter växte mycket långsammare än sina omuterade motsvarigheter och visade störd kalciumbalans, vilket tyder på att den förändrade pumpen utför sitt normala arbete dåligt. I blandade odlingar konkurrerades de mindre lämpade mutanterna snabbt ut av de mer välanpassade vildtypparasiterna när inget läkemedel fanns närvarande. Detta tyder på att även om sådan resistens kan uppstå under starkt läkemedelstryck, är det osannolikt att den sprider sig brett i fält eftersom resistenta parasiter skulle vara i underläge när SC83288 saknas. Ur ett folkhälsoperspektiv gör denna höga fitnesskostnad, kombinerat med läkemedlets nya sätt att slå mot parasitens epigenetiska kontrollsystem, SC83288 till en särskilt attraktiv kandidat i kampen för att ligga steget före malaria.
Citering: Sanchez, C.P., Duffey, M., Celada, R.V. et al. Mechanisms of PfDNMT2 inhibition and PfATP6-mediated resistance to the antimalarial candidate SC83288 in Plasmodium falciparum. Nat Commun 17, 2327 (2026). https://doi.org/10.1038/s41467-026-70280-y
Nyckelord: läkemedelsresistens vid malaria, Plasmodium falciparum, epigenetisk terapi, DNA‑metylering, utveckling av antimalariamedel