Clear Sky Science · sv
NAA40 och NAC samarbetar i kotranslationell histonacetylering hos människor
Hur celler finjusterar sina genetiska strömbrytare
Inuti varje mänsklig cell modifieras nyligen skapade proteiner kemiskt samtidigt som de rör sig ut ur cellens proteinfabriker, ribosomerna. Dessa små justeringar kan avgöra var ett protein hamnar, hur länge det lever och till och med hur våra gener slås på eller av. Denna artikel fokuserar på ett högspecialiserat protein som kallas NAA40 och ett hjälparkomplex som kallas NAC, och visar hur de samarbetar på ribosomen för att modifiera histonproteiner — spolarna runt vilka DNA är lindat — och därigenom påverka genaktivitet och potentiellt cancerutveckling.
En liten mössa som ändrar histonernas beteende
Många mänskliga proteiner får en liten kemisk mössa vid sin N-terminal, en process som kallas N-terminal acetylering. Histonerna H2A och H4, som hjälper till att packa DNA till kromatin, är nästan alltid acetylerade på detta sätt. NAA40 är ovanlig bland enzymer eftersom den nästan uteslutande specialiserar sig på att lägga till denna mössa på just dessa histoner medan de syntetiseras. Denna acetylmark konkurrerar med andra kemiska etiketter, såsom fosforylering och metylering, på samma region av histonerna, så om NAA40 verkar eller inte kan skifta hur tätt DNA är paketerat och hur gener regleras. Viktigt är att förändrade nivåer av NAA40 har kopplats till flera cancerformer, vilket gör det till ett lovande mål för nya terapier.
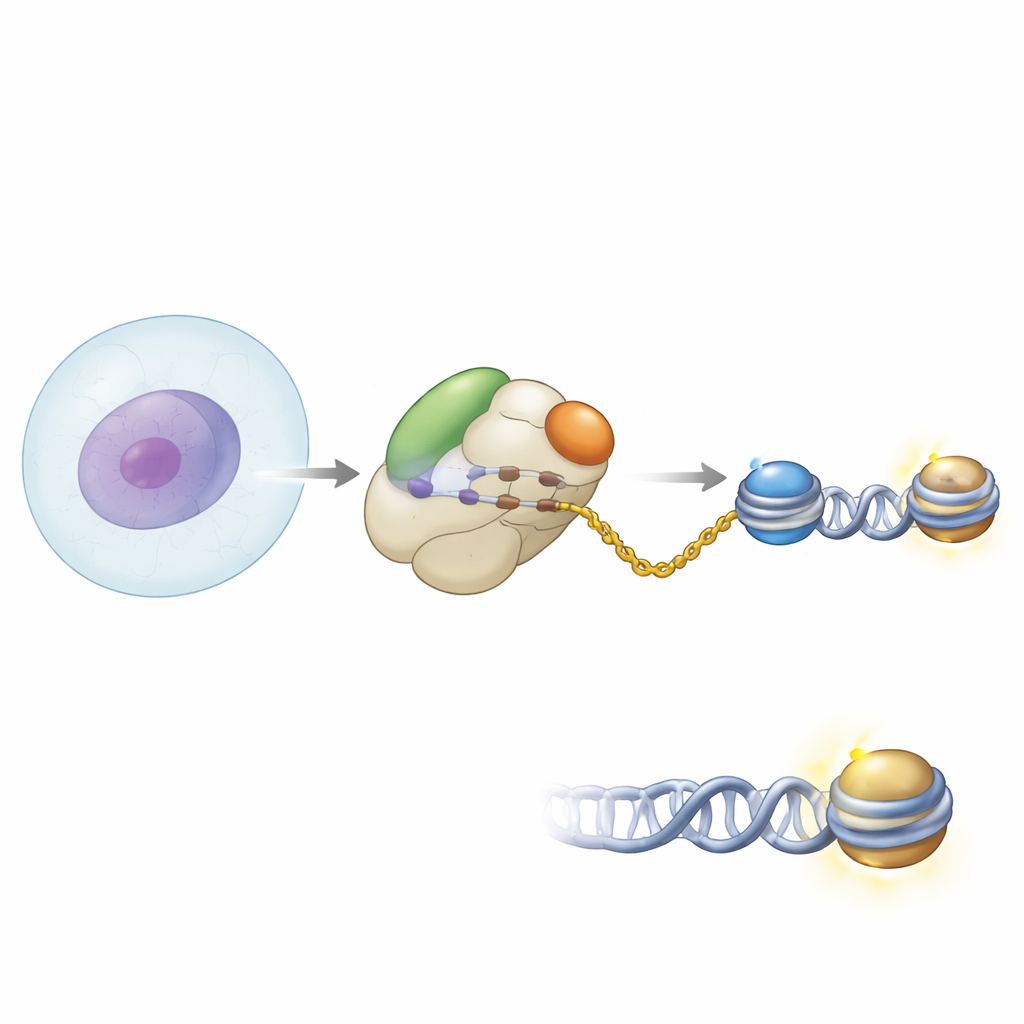
Samarbete vid proteinfabrikens port
Författarna använde biokemiska metoder och högupplöst kryo-elektronmikroskopi för att se hur NAA40 är positionerat på den mänskliga ribosomen. De fann att NAA40 sitter precis vid tunneln där nyfödda polypeptidkedjor träder ut. Där arbetar den inte ensam: den binder tillsammans med det nascent polypeptide–associated complex, eller NAC, ett vanligt ribosombundet hjälparkomplex som övervakar nya proteiner när de kommer ut. Strukturella ögonblicksbilder visade att NAA40 förankras vid ribosomen av ett unikt positivt laddat helixsegment vid sin egen början, medan NAC är fäst via en av sina subenheter till ribosomens yta. En flexibel domän av NAC sträcker sig över för att kontakta NAA40 och fungerar i praktiken som en bro mellan enzymet och ribosomen.
Varför NAC behövs för histonfininställning
För att testa hur viktigt detta partnerskap är rekonstituerade forskarna dessa interaktioner med renade komponenter i provrör. De observerade att NAA40 på egen hand binder svagt till ribosomer, men när NAC är närvarande blir ribosombindningen mycket starkare. Om de tog bort ett specifikt ”UBA”-område från NAC som kontaktar NAA40 försvann denna förbättrade bindning. I humana celler ledde uttömning av NAC till reducerad NAA40-beroende acetylering av histon H4 och en motsvarande ökning av en konkurrerande fosforyleringsmarkering på samma histonstjärt. Denna förändring skedde utan att mängden eller lokaliseringen av NAA40 själv förändrades, vilket indikerar att NAC:s huvudroll är att rekrytera och positionera NAA40 korrekt på translaterande ribosomer så att histoner kan modifieras effektivt när de syntetiseras.
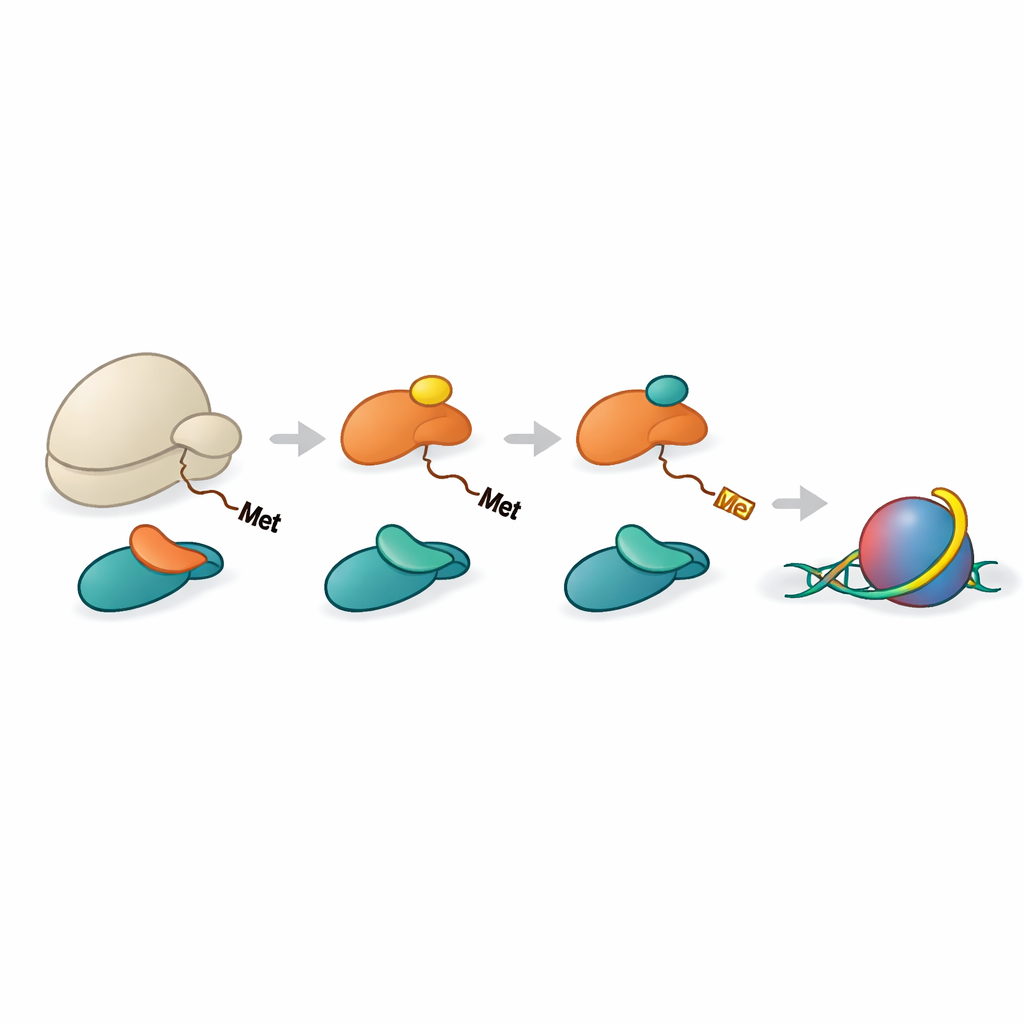
En koordinerad monteringslinje för histonbearbetning
Histonerna H2A och H4 måste först förlora sin initiala metioninaminosyra innan NAA40 kan känna igen dem. Ett annat enzym, METAP1, genomför denna trimning. Teamet visade att NAC kan hjälpa till att föra METAP1 och NAA40 tillsammans med ribosomen och bilda en multi-enzymassembly vid peptidutgången. Högupplösta strukturer av rekonstituerade komplex visade METAP1 och NAA40 bundna sida vid sida på ribosomen, med sina aktiva ytor positionerade på nästan lika avstånd från utgångstunneln. Denna geometri innebär att när en histonstjärt sträcker sig bara ett dussin eller så aminosyror bortom ribosomen kan METAP1 ta bort startmetioninen och NAA40 omedelbart lägga till acetylmössan, vilket minimerar fördröjningen mellan de två stegen.
Konsekvenser för genreglering och cancer
Sammanfattningsvis visar studien att NAA40 inte bara driver omkring i cellen för att leta efter histoner att modifiera. Istället är det förankrat vid ribosomen av NAC och utgör en del av en organiserad bearbetningsstation som förbereder histoner i samma ögonblick som de syntetiseras. Genom att nära koppla borttagning av metionin och tillsats av acetyl säkerställer cellen att histon H2A, H4 och DNA-skadeassocierade varianten H2A.X snabbt får en acetylmarkör som kan forma kromatinstruktur och genuttryck. Eftersom störningar i detta tidiga histonmärkningssteg kan gynna cancerogent växande, ger förståelsen av den precisa arrangemanget av NAA40, NAC och METAP1 på ribosomen en strukturell ritning som kan vägleda designen av läkemedel inriktade på att finjustera denna kritiska epigenetiska kontrollpunkt.
Citering: Guan, D., Denk, T., Klavaris, A. et al. NAA40 and NAC cooperate in co-translational histone acetylation in humans. Nat Commun 17, 2486 (2026). https://doi.org/10.1038/s41467-026-70279-5
Nyckelord: histonacetylering, NAA40, ribosom, nascent polypeptide-associated complex, epigenetisk reglering