Clear Sky Science · sv
En cellcykelberoende övergång från acetylering till fosforylering reglerar tidsmässig centrosommognad
Hålla vårt genetiska gods på rätt spår
Varje gång en cell i vår kropp delar sig måste den fördela sitt DNA med yttersta noggrannhet. När denna process går fel kan celler få för många eller för få kromosomer, ett farligt tillstånd som kopplas till cancer och andra sjukdomar. Den här studien avslöjar en molekylär tidmätare som hjälper celler att bygga de små strukturer som krävs för att separera kromosomer korrekt, och blottar en möjlig svag punkt som framtida cancerbehandlingar skulle kunna utnyttja.
Cellens små trafiknav
I centrum för varje delande cell finns centrosomer, små strukturer som fungerar som trafiknav för de fibrer som drar isär kromosomerna. Innan en cell går in i delning måste dessa nav “mogna”: de förstärks med hjälpproteiner och blir kraftfulla organisatörer av mikrotubuli, de dynamiska fibrerna som bildar delningsspindeln. Om den här mognaden sker för tidigt, för sent eller inte alls kan kromosomer fördelas felaktigt, vilket leder till celler med onormalt kromosomantal. Att förstå hur celler slår på centrosomerna i precis rätt ögonblick har länge varit en öppen fråga inom cellbiologin.
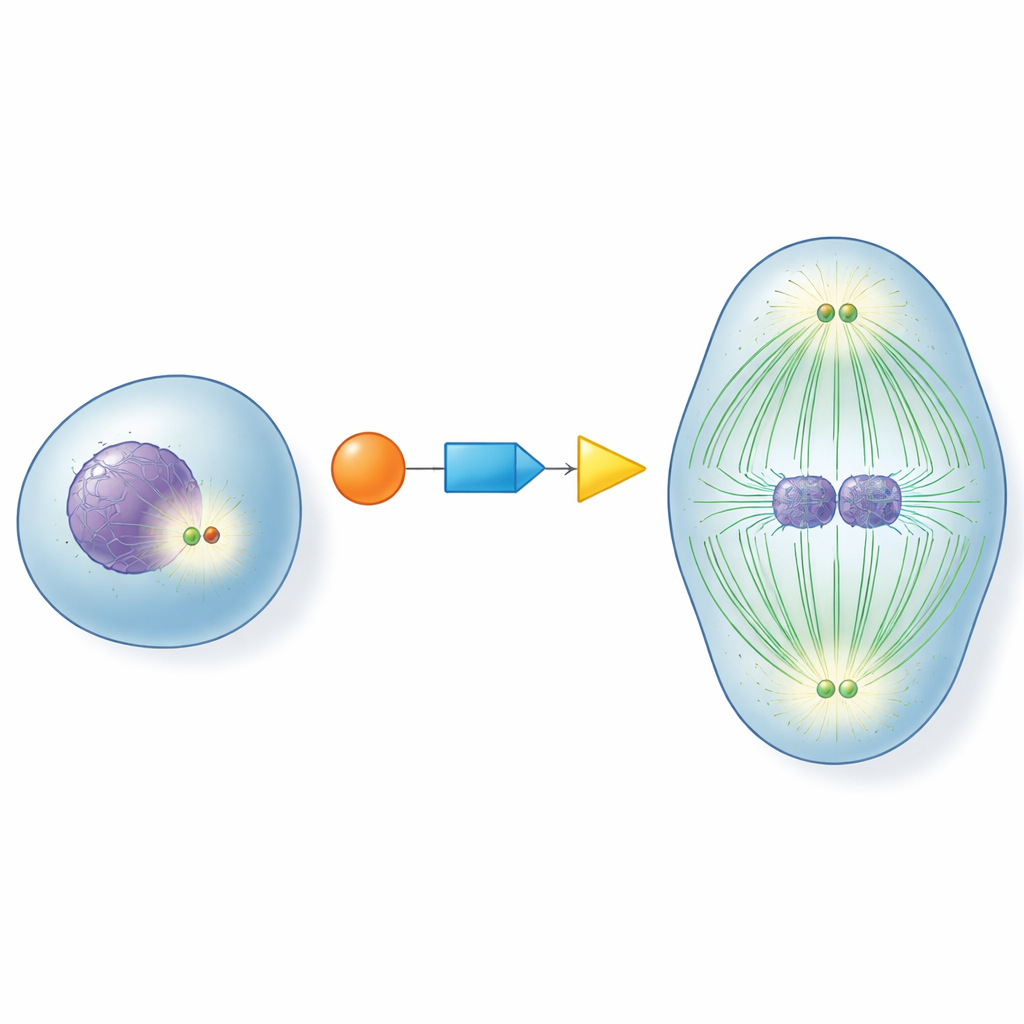
En molekylär stafettsignal för perfekt timing
Författarna koncentrerade sig på tre nyckelproteiner som fungerar tillsammans som en stafettrelä: CDK1, en huvudregulator av cellcykeln; RNF40, tidigare mest känd för att modifiera DNA‑paketerande proteiner; och PLK1, en central drivare av celldelning. De upptäckte att RNF40 fysiskt finns vid centrosomer under hela cellcykeln och binder direkt till PLK1. När cellerna närmar sig delning märker CDK1 kemiskt RNF40 på två specifika platser, vilket i sin tur gör RNF40 till en bättre dockningsplats för PLK1. Denna CDK1–RNF40–PLK1‑kedja säkerställer att PLK1 anländer till centrosomerna precis under den sena förberedelsefasen inför delning, vilket utlöser kraftfull centrosommognad, mikrotubulustillväxt och uppbyggnad av en välformad bipolär spindel.
En formföränderlig proteinswitch
Intressant nog accepterar RNF40 inte alltid dessa aktiverande märkningar. I icke‑delande och DNA‑kopieringsfaser bär RNF40 en annan kemisk dekoration — acetylgrupper — på två närliggande positioner. Dessa acetylmärken läggs till av ett enzym kallat PCAF och tas senare bort av en deacetylaspartner, HDAC1. Den acetylerade formen av RNF40 motstår modifiering av CDK1 och blockerar effektivt nästa steg i reläet. När cellerna går in i den sista fördelningsberedskapsfasen suddar HDAC1 gradvis ut acetylmärkena, vilket tillåter CDK1 att istället lägga på fosfatgrupper. Denna noggrant tidssatta övergång från acetylering till fosforylering förvandlar RNF40 från ett “standby”‑läge till ett “på”‑läge, redo att rekrytera PLK1 och driva upp centrosomen.
Vad händer när timingen misslyckas
För att undersöka hur avgörande denna switch är konstruerade forskarna celler där RNF40 inte längre kunde fosforyleras, eller där den tvingades stanna i ett acetyleringsliknande tillstånd. I båda fallen misslyckades PLK1 med att ackumuleras korrekt vid centrosomerna. Dessa celler visade försvagad mikrotubulustillväxt från centrosomer, missformade spindlar och felställda kromosomer. Många slutade med extra eller saknade kromosomer — ett onormalt tillstånd kallat aneuploidi — och vissa blev binukleära, tecken på katastrofala delningsfel. I cancermodeller bildade celler låsta i det “acetylerade” RNF40‑tillståndet mindre tumörer i möss och var mer känsliga för vanliga cytostatika som används vid behandling av kolorektal cancer, vilket tyder på att störning av denna switch kan bromsa tumörtillväxt.
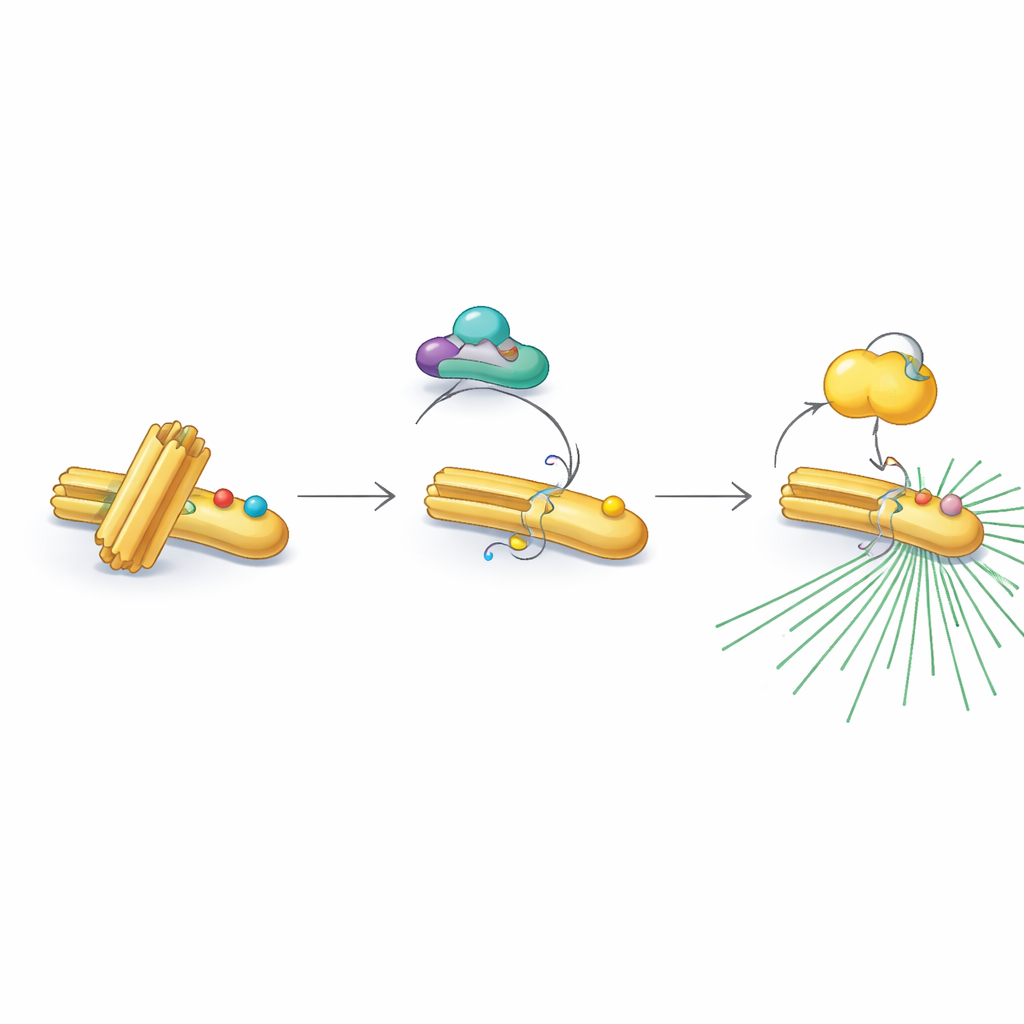
Kopplingar till mänsklig cancer och framtida möjligheter
Teamet undersökte också patientdata och tumörprover. De fann att RNF40 ofta är onormalt överrepresenterat i kolorektal cancer och att vissa cancerassocierade mutationer nära dess modifieringsställen stör dess fosforylering, vilket undergräver korrekt centrosomfunktion. Dessa iakttagelser kopplar den nybeskrivna tidmekanismen direkt till mänsklig sjukdom. Genom att peka ut ett specifikt protein som koordinerar när centrosomer mognar och hur kromosomer separeras lyfter studien fram en signaleringsnod som skulle kunna riktas för att pressa snabbt delande cancerceller in i dödliga delningsfel, samtidigt som friska celler lämnas mindre påverkade.
En ny möjlighet att få tillförlitlig celldelning att svikta
För icke‑specialister är huvudbudskapet att celler förlitar sig på en fint avvägd kemisk switch på ett enda protein, RNF40, för att avgöra exakt när maskineriet som separerar kromosomer ska aktiveras. Denna övergång från acetylering till fosforylering beter sig som ett trafikljus i en trafikerad korsning och slår över till grönt bara när cellen verkligen är redo att dela sig. När ljuset slutar fungera snubblar cellerna igenom delningen, samlar på sig genetiska fel och kan bli cancerösa. Att förstå och kunna kontrollera denna switch kan öppna nya vägar för behandlingar som selektivt destabiliserar cancerceller genom att sabotera deras förmåga att dela sig rent.
Citering: Li, J., Liang, J., Chen, G. et al. A cell cycle-dependent transition of acetylation to phosphorylation regulates timely centrosome maturation. Nat Commun 17, 2583 (2026). https://doi.org/10.1038/s41467-026-70271-z
Nyckelord: centrosommognad, celldelning, kromosominstabilitet, PLK1‑signalering, kolorektal cancer