Clear Sky Science · sv
Vägvalssekvenser mellan click‑ och acylöverföringsreaktioner drivna av aminoacylfosfater
Varför tidpunkten spelar roll i vardaglig kemi
Inne i varje cell byggs och modifieras viktiga molekyler i en mycket bestämd ordning, ungefär som steg i ett recept. Denna tidsordning avgör om ett protein aktiveras, stängs av eller till och med ändrar form. Kemister vill efterlikna denna slags inbyggda schema med enkla, icke‑levande molekyler i vatten, utan att förlita sig på enzymer eller yttre stimuli som ljus eller pH‑skift. Denna artikel beskriver ett konstgjort reaktionssystem som gör just detta: det utnyttjar strukturen hos små peptider och en populär bindningsbildande reaktion från "click chemistry" för att bestämma vilket kemiskt steg som sker först och vilket som måste vänta.
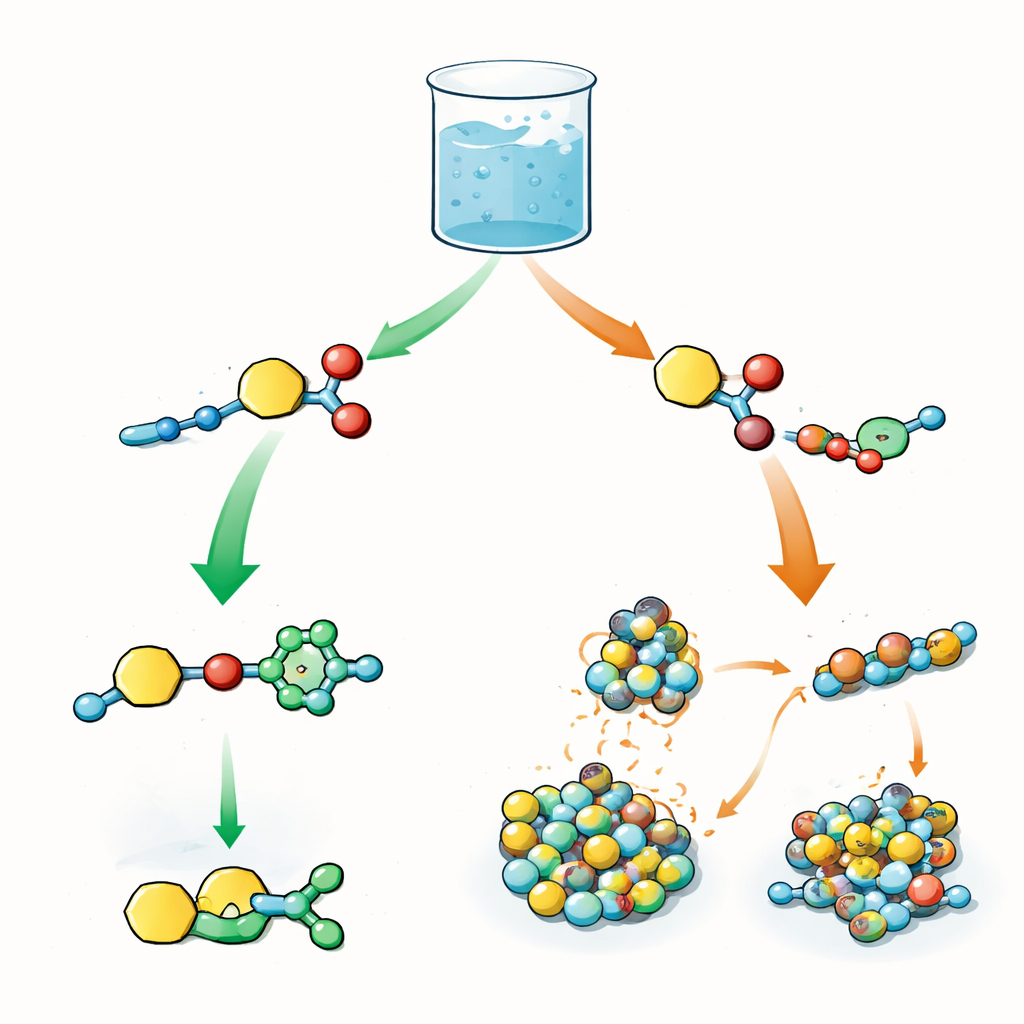
Två rivaliserande reaktioner i samma kolv
Författarna utformar en central byggsten som bär två reaktiva egenskaper: en som kan överföra en "acyl"‑grupp (en liten kemisk fragment ofta använd för att modifiera proteiner) och en annan som kan genomgå en click‑reaktion kallad koppar‑katalyserad azid‑alkyn cykloaddition. I samma bägare blandas denna byggsten med azider och med korta peptider som fungerar som nukleofiler, det vill säga de fångar upp acylgruppen. I biologin styr ordningen av sådana steg—aktivering, överföring och senare modifieringar—hur proteiner beter sig. Här är frågan liknande: när båda reaktionerna är möjliga samtidigt, väljer systemet click‑reaktionen först, acylöverföring först eller någon blandning av båda?
Långsam syre, snabb svavel
Teamet studerar först peptider som innehåller tyrosin, en aminosyra med en syrebaserad sidokedja. Under milt basiska förhållanden rusar click‑reaktionen i förväg: alkynen och aziden kopplas snabbt ihop, medan acylöverföring till tyrosins sidokedja är trög och knappast bygger upp påvisbara intermediärer. Flera click‑härledda produkter samexisterar, och det finns ingen tydlig tidslucka mellan stegen. När forskarna byter till cystein, en aminosyra med en svavelbaserad sidokedja, vänder historien. Cystein bildar snabbt tioestrar—svavelbundna acylprodukter—som uppträder i hög utbyte långt innan några click‑produkter syns. Först efter många timmar börjar click‑produkterna dyka upp. Denna förskjutning beror på att svavel inte bara reagerar mer ivrigt utan också binder kopparjoner, vilket binder upp katalysatorn och tillfälligt "pausar" click‑vägen.
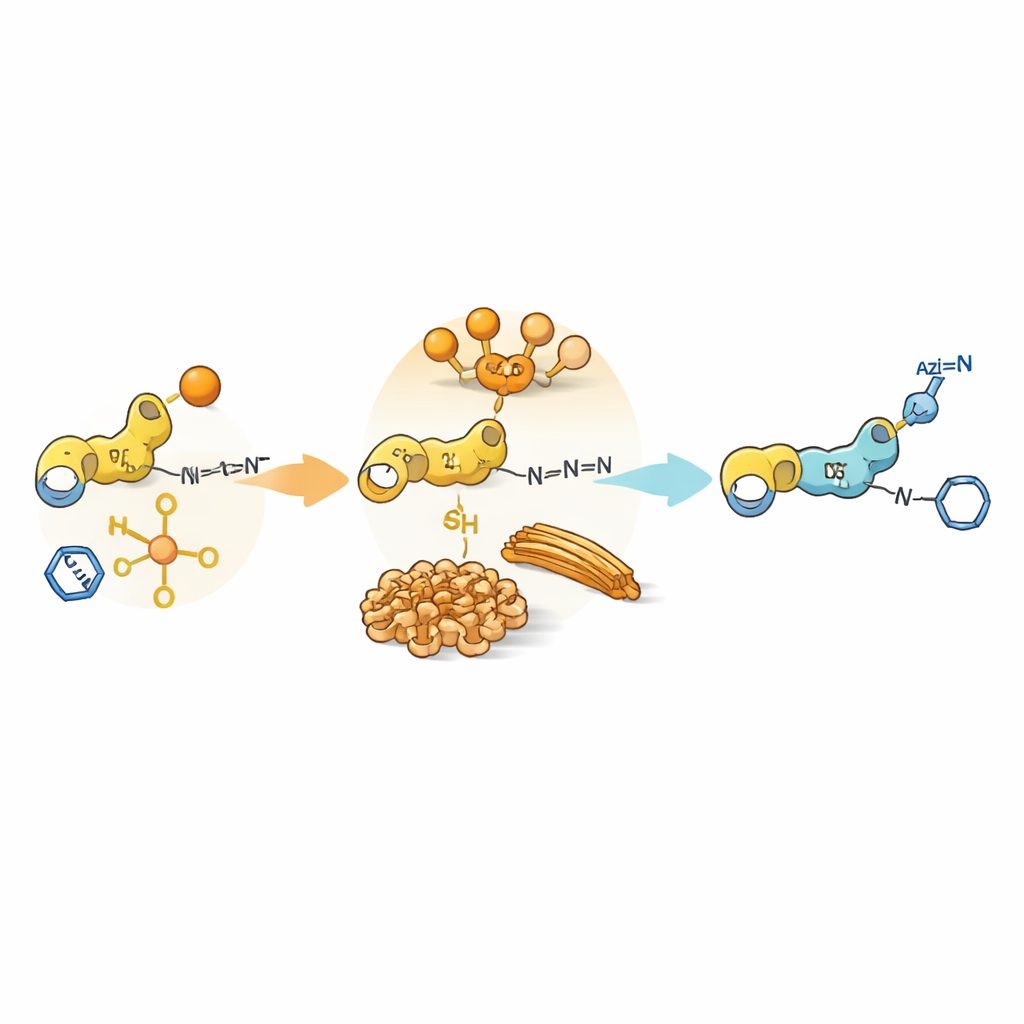
Självsammansättning som en kemisk grind
Utöver enkel reaktivitet kan peptiderna själva klumpa ihop sig till större strukturer och bilda mjuka geler eller fibrer i vatten. Dessa assembléer skapar små domäner där vissa partner är koncentrerade och andra utesluts. För vissa tyrosin‑ eller cystein‑innehållande dipeptider som bär extra aromatiska grupper självorganiseras intermediärerna till fibriller eller täta partiklar. Inuti dessa packade regioner gynnas acylöverföring eftersom nukleofil och acyldonator sitter sida vid sida, medan azid och kopparkatalysatorn främst stannar i omgivande lösning. Som ett resultat, även om click‑reaktionen är intrinskt snabb i fri lösning, bromsas den av behovet att nå de begravda reaktiva ytorna. Denna "fasmissmatch" mellan var katalysatorn befinner sig och var substraten är lokaliserade förlänger livet för acylerade intermediärer och fördröjer uppkomsten av click‑kemi.
Programmering av kaskader och val
För att testa hur långt de kan driva detta inbyggda schema designar författarna mer komplexa situationer. I ett fall innehåller en enda peptid både cystein och tyrosin och erbjuder två olika platser för acylöverföring. Reaktionen fortskrider som en trestegs‑kaskad: först bildas en tioester på cystein, sedan flyttar en andra acylgrupp till tyrosin, och först efter dessa steg dyker click‑produkterna upp. I en annan uppsättning experiment konkurrerar två olika azider—en flexibel och alifatisk, den andra styv och aromatisk—om samma reaktiva centrum. Överraskande nog väljer systemet konsekvent den alifatiska aziden, vilket visar att även formen och den elektroniska karaktären hos aziden kan snedvrida vilka produkter som dominerar, samtidigt som acylöverföringens timing förblir under peptidernas kontroll.
Vad detta betyder för framtida smarta material
I vardagliga termer visar detta arbete hur man kan packa flera potentiellt konkurrerande reaktioner i samma enkla vattenbaserade blandning och ändå få dem att gå i en bestämd ordning—utan enzymer, pumpar eller yttre strömbrytare. Genom att välja om en peptid bär syre eller svavel, genom att justera dess benägenhet att självorganisera och genom att anpassa azidpartnerns natur, kodar författarna in en slags intern klocka i ett litet kemiskt nätverk. Tidiga, reversibla acylöverföringar skapar kortlivade intermediärer som formar när och hur det robusta, nästan irreversibla click‑steget inträffar. Sådana programmerade sekvenser kan bli en grund för smarta material och syntetiska reaktionsnätverk som "bestämmer" sina egna vägar över tiden, på samma sätt som den noggrant tajmade kemin i levande celler.»
Citering: Bhattacharjee, D., Sharma, A., Dai, K. et al. Pathway selection between click and acyl transfer reactions driven by aminoacyl phosphates. Nat Commun 17, 2407 (2026). https://doi.org/10.1038/s41467-026-70199-4
Nyckelord: clickkemi, acylöverföring, supramolekylär sammansättning, reaktionsnätverk, peptidkemi