Clear Sky Science · sv
Single-cell multiomics uncovers an endothelial mechanosensitive PIEZO1-IL-33 axis driving pulmonary fibrosis
Varför stela lungor spelar roll
Pulmonell fibros är en förödande lungsjukdom där de tidigare elastiska luftblåsorna gradvis omvandlas till styvt ärrvävnad, vilket gör varje andetag ansträngande. Läkare kan i dag bara bromsa sjukdomen, inte stoppa eller vända den. Denna studie ställer en till synes enkel fråga med stora följder: hur känner cellerna som beklär lungornas blodkärl av att omgivande vävnad blivit abnormt stel, och hur omsätts denna känsla till mer ärrbildning? Genom att spåra denna händelsekedja ända ner till enskilda celler och gener avslöjar forskarna en mekanisk ”strömbrytare” i blodkärlen som kan vara möjlig att rikta läkemedel mot.
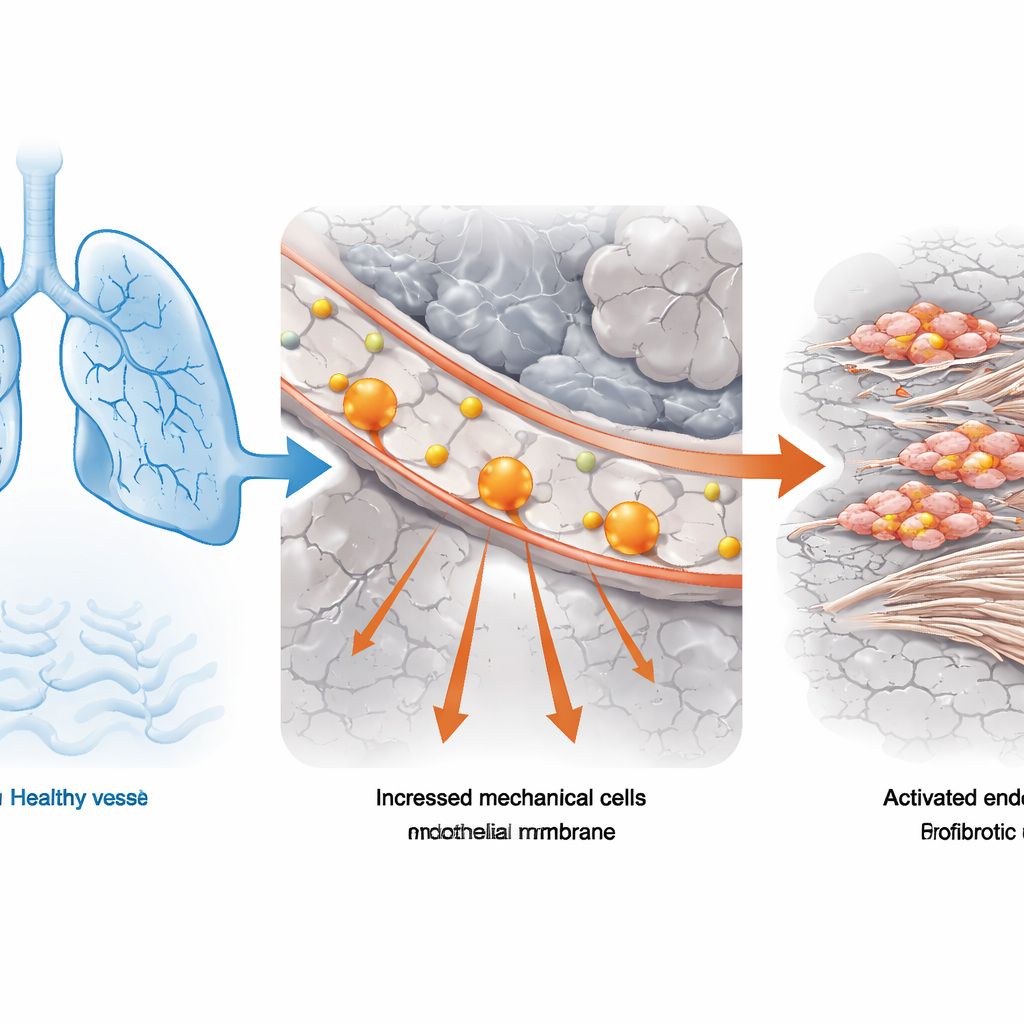
Från lungfunktionsprov till enskilda celler
Teamet började med lungvävnad från personer med idiopatisk pulmonell fibros, den vanligaste formen av sjukdomen, och från donatorer med normala lungor. De kombinerade standardiserade lungfunktionsmätningar (hur mycket luft en person kan andas ut med kraft) med kraftfull single-cell RNA-sekvensering, som läser av vilka gener som är aktiva i tusentals enskilda celler. Med ett beräkningsverktyg som kopplar samman övergripande kliniska data med single-cell-profiler identifierade de vilka celltyper som mest tydligt var associerade med kraftigt nedsatt lungfunktion. Vaskulära endotelceller—cellerna som bildar blodkärlens innersta lager—var särskilt framträdande hos patienter vars lungkapacitet var mindre än hälften av normal. I dessa endotelceller var genprogram kopplade till ”mekanisk stress” konsekvent uppreglerade, vilket tyder på att abnorma fysikaliska krafter var en del av problemet.
Mekanisk stress som en dold drivkraft
För att testa om sambandet mellan stresstålighet och sjukdom var generellt gick forskarna vidare till två musmodeller för lungsårbildning: en utlösts av cytostatikumet bleomycin och den andra av långvarig exponering för kiseldamm, en yrkesmässig risk. Genom att använda single-cell-metoder på dessa experimentella lungor fann de återigen att endotelceller bar tydliga signaturer av förhöjd mekanisk stress. I båda modellerna, i takt med att omgivande lungvävnad tjocknade och blev stelare, verkade blodkärlens innervägg skifta till ett maladaptivt tillstånd. Denna konvergens mellan mänskliga prover och djurmodeller stärkte idén att snedvridna fysiska krafter i lungan, snarare än enbart inflammation eller immunaktivitet, är centrala för hur fibros utvecklas och progredierar.
En trycksensor med kritisk roll
Genom att gå djupare sökte teamet efter specifika ”mekanosensorer”—proteiner som omvandlar fysisk töjning till biokemiska signaler—som var uppreglerade i stressade endotelceller. En jonkanal, kallad PIEZO1, framträdde upprepade gånger som en huvudmisstänkt. Både hos möss och människor med fibros var nivåerna av PIEZO1 tydligt högre i vaskulära endotelceller än hos friska kontroller. När forskarna konstruerade möss där PIEZO1 togs bort enbart i endotelet var dessa djur mycket mer motståndskraftiga mot bleomycin‑inducerad lungsårbildning: de hade mindre kollagenansamling, färre aktiverade ärrbildande celler och lägre nivåer av en biokemisk markör för fibros. Farmakologisk blockad av PIEZO1 med en peptid‑hämmare lindrade också ärrbildningen, medan aktivering av kanalen förvärrade fibros—om inte receptor var frånvarande i endotelcellerna. Tillsammans visade dessa experiment att PIEZO1 i kärlbeklädnadens celler inte bara är åskådare utan en nödvändig drivkraft för sjukdomen.
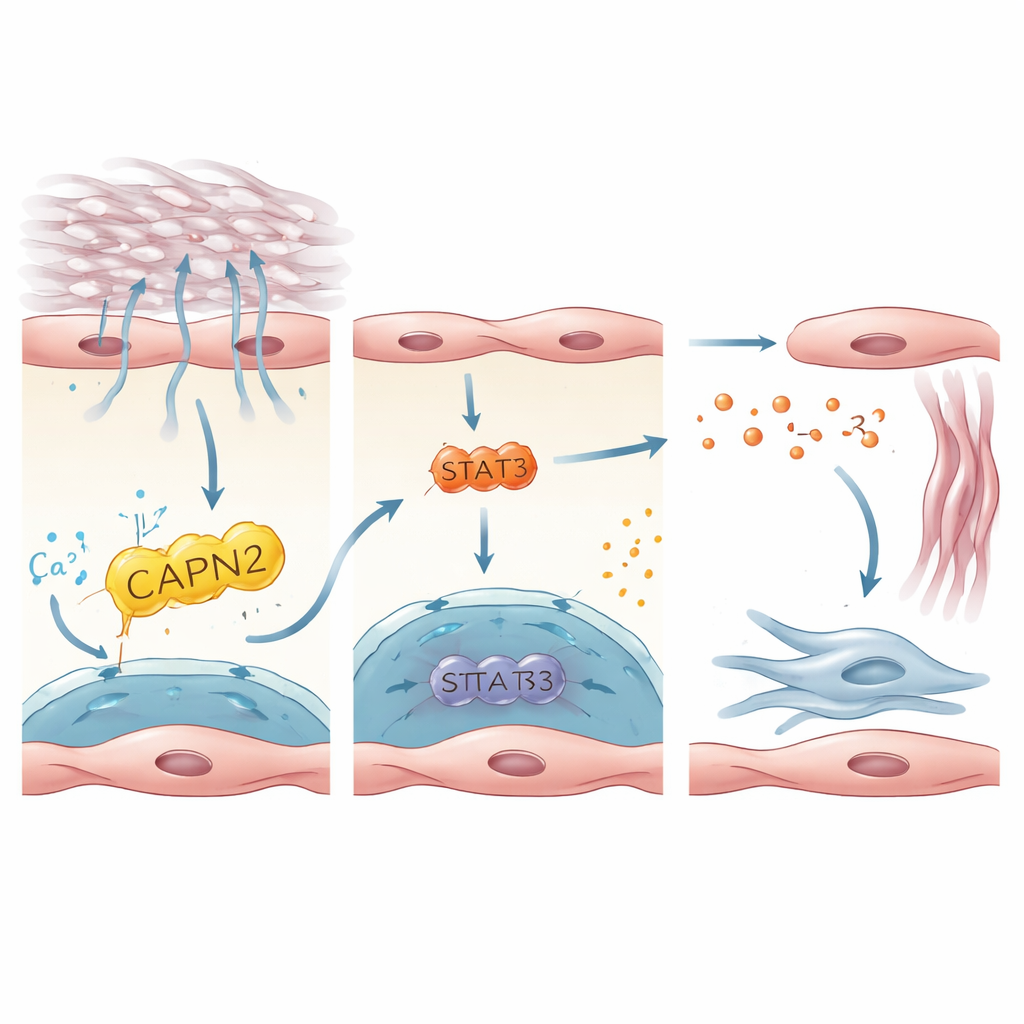
En signalväg som väcker ärrbildande celler
Studien följde därefter hur PIEZO1‑aktivering i endotelceller översätts till signaler som väcker fibroblaster, de celler som bygger upp ärrvävnad. Genom att integrera mänskliga och musdata identifierade författarna interleukin‑33 (IL‑33), ett litet protein som frisätts från stressade eller skadade celler, som en nyckelbudbärare. IL‑33 uttrycktes starkt i PIEZO1‑positiva endotelceller och var förhöjt i lungor från patienter och möss med fibros. I odlade humana endotelceller som växte på styva underlag eller utsattes för töjning för att efterlikna andning mot en stel lunga ökade PIEZO1‑aktivering IL‑33‑produktionen. Detta berodde på ett nedströms enzym, CAPN2, och en transkriptionsfaktor, STAT3, som tillsammans reglerade IL‑33‑gens aktivitet. Hos möss skyddade borttagning av IL‑33 specifikt i endotelceller mot fibros, medan tvångsöveruttryck av IL‑33 i endotelceller utplånade det skydd som förlust av PIEZO1 gav. Resultaten beskriver en linjär axel: mekanisk stress → PIEZO1 → CAPN2/STAT3 → IL‑33 → fibroblastaktivering och ärrbildning.
Vad detta betyder för framtida behandlingar
För icke‑specialister är budskapet att lungfibros inte drivs enbart av felstyrda immunceller; det är också en sjukdom av defekt ”känsel” i blodkärlen. Endotelceller uppfattar att deras omgivning blivit för stel, slår på PIEZO1‑strömbrytaren och frigör i respons IL‑33, en farosignal som uppmuntrar närliggande fibroblaster att fortsätta avsätta ärrvävnad. Genom att dissekera denna kedja från mekanisk kraft till genuttryck lyfter arbetet flera lovande mål—själva PIEZO1, CAPN2‑STAT3‑reläet och IL‑33—för terapier som syftar till att bryta den självförstärkande cykeln av stelhet och ärrbildning. Även om fler studier krävs för att säkert modulera dessa vägar hos människor, erbjuder denna mekanosensitiva endoteliala axel en ny, fysiskt grundad inriktning för att angripa en sjukdom som länge motstått effektiva behandlingar.
Citering: Zhang, L., Gui, X., Hou, R. et al. Single-cell multiomics uncovers an endothelial mechanosensitive PIEZO1-IL-33 axis driving pulmonary fibrosis. Nat Commun 17, 2655 (2026). https://doi.org/10.1038/s41467-026-70193-w
Nyckelord: pulmonell fibros, endotelceller, mekanotransduktion, PIEZO1, IL-33