Clear Sky Science · sv
Anpassningar i Plasmodium-tubulin bestämmer skilda mikrotubuli‑arkitekturer, mekanik och läkemedelskänslighet
Varför malarians skelett spelar roll
Malariaparasiter överlever inne i mänskliga blodkroppar, men de måste också pressa sig igenom myggor och olika vävnader. För att klara detta förlitar de sig på en intern stomme gjord av mikroskopiska rör kallade mikrotubuli. Denna studie ställer en enkel men kraftfull fråga: hur kan parasitens mikrotubuli vara så specialiserade och styva när deras grundläggande byggstenar ser så lika ut dem i våra egna celler? Svaret visar inte bara hur parasiten behåller sin form, utan också hur vi kan utforma läkemedel som riktar in sig på dess skelett utan att skada vårt eget. 
De små rören som formar en dödlig parasit
Mikrotubuli är ihåliga proteinerör som hjälper celler att dela sig, röra sig och behålla sin form. De byggs upp av parade protein-enheter som kallas tubulin. Över djur, växter och parasiter är tubulin förvånansvärt likt, vilket gör det svårt att förklara varför mikrotubuli kan se och bete sig så olika i olika organismer. I malariaparasiten Plasmodium falciparum bildar mikrotubuli olika arkitekturer: vissa är dynamiska och hjälper vid celldelning, medan andra är långa, styva stöd under parasitens yttre membran. Eftersom dessa strukturer är avgörande för parasitens tillväxt och spridning är de attraktiva mål för antimalariamedel—särskilt eftersom resistens mot nuvarande behandlingar fortsätter att öka.
Se parasitens tubulin i atomär detalj
Forskarna renade tubulin direkt från P. falciparum‑parasiter och använde högupplöst kryo‑elektronmikroskopi för att se hur det monteras till mikrotubuli. De jämförde dessa strukturer med de välstuderade mikrotubuli från däggdjurs‑hjärna. Vid första anblick ser parasitens tubulin nästan identisk ut med den mänskliga versionen och antar samma övergripande veckning. Men noggrann jämförelse avslöjade kluster av små sekvensförändringar runt nyckelfickor där energibärande molekyler (GTP och GDP) binder och där vissa läkemedel interagerar. Dessa subtila skift förändrar hur närliggande helixar och slingor är positionerade, särskilt på ytan av tubulin‑dimeren där andra proteiner och läkemedel hakar i. Arbetet tyder på att, medan den övergripande ritningen är bevarad, omformar lokala finjusteringar hos parasiten dessa viktiga platser.
Styvare rör genom starkare sidledes förbindelser
Mikrotubuli är polymerer: många tubulin‑dimerer staplas ända‑till‑ända till protofilament, och flera protofilament ligger sida‑vid‑sida för att bilda rörväggen. Teamet fann att i parasitens mikrotubuli ser de longitudinella kontakterna längs varje protofilament mycket lika ut dem i hjärnmikrotubuli. Skillnaden visar sig i de sidledes, eller laterala, kontakterna mellan intilliggande protofilament. Även om kontaktområdet faktiskt är något mindre i parasiten, visar simuleringar att dessa laterala kopplingar kollektivt är starkare, vilket gör gitterstrukturen styvare. Datorbaserad modellering av partier av mikrotubuliväggen visade att parasit‑tubulin böjer och vrider sig mindre än hjärn‑tubulin. Elektrontomografi av verkliga mikrotubuliändar bekräftade att parasitens mikrotubuli har kortare, mindre utspridda protofilament‑lockar, ett kännetecken för ett robustare rör. 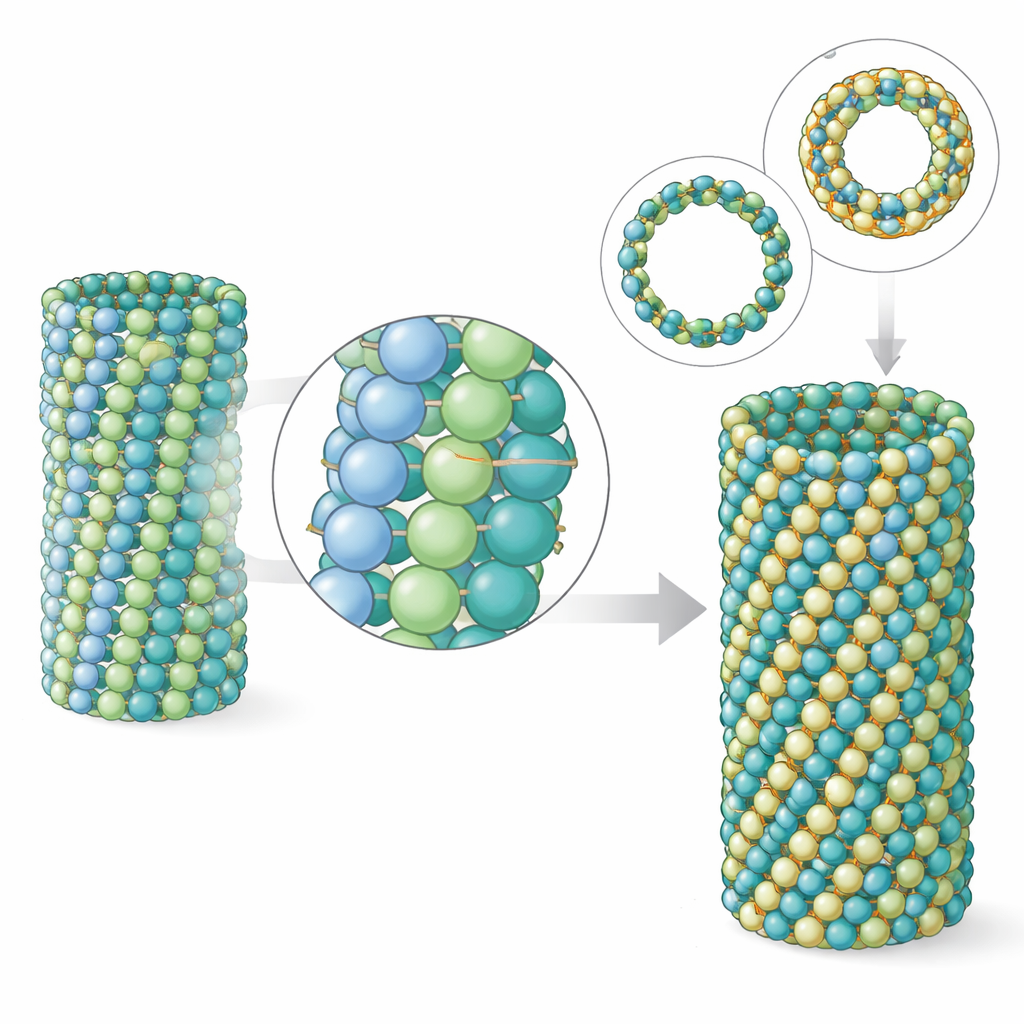
Ovanliga rörstorlekar som matchar parasitens behov
Ett annat slående drag hos P. falciparum är att i vissa livsstadier innehåller dess mikrotubuli fler byggstenar runt omkretserna än de vanliga 13 som finns i de flesta djurceller—ofta 15 eller till och med 17 rader med protofilament. Teamet återskapade detta beteende i provröret genom att ändra nukleotiden som användes under montering. Med en GTP‑lik molekyl som stabiliserar den växande staten föredrog parasitens tubulin naturligt 15‑protofilamentmikrotubuli. Författarna löste strukturen av dessa tjockare rör och visade hur de rymmer de extra protofilamenten med en lätt snedvridning av gitteret, men ändå förblir nästan perfekt cylindriska. När de jämförde dessa laboratorietillverkade 15‑protofilamentrör med dem som ses inne i parasitceller var överensstämmelsen i form och dimensioner anmärkningsvärt nära, vilket indikerar att tubulinets inneboende egenskaper—snarare än en mängd hjälpproteiner—är tillräckliga för att skapa parasitens karaktäristiska arkitekturer.
Ledtrådar för framtida, parasitspecifika läkemedel
Studien drar slutsatsen att evolutionen har finjusterat parasitens tubulin genom små, spridda sekvensändringar som tillsammans förändrar mikrotubulimekanik, arkitektur och läkemedelskänslighet. Dessa justeringar gör parasitens mikrotubuli styvare och möjliggör bildandet av icke‑standardiserade rörstorlekar som passar dess krävande livscykel, samtidigt som den grundläggande tubulindesignen förblir igenkännbar. Viktigt för medicin är att vissa läkemedelsbindande fickor verkar nästintill identiska mellan parasit och värd (som för cancerläkemedlet paklitaxel), vilket tyder på att de är dåliga mål för selektiva antimalariamedel. Andra, såsom den region som tros binda herbicidliknande föreningen oryzalin, uppvisar både sekvensskiften och subtila strukturella förskjutningar som kan förklara varför parasitens mikrotubuli är mer sårbara där än mänskliga. Kartläggning av dessa nyanserade skillnader ger en färdplan för att utforma framtida läkemedel som stör malariaparasitens skelett samtidigt som våra egna celler i stort lämnas orörda.
Citering: Bangera, M., Wu, J., Beckett, D. et al. Adaptations in Plasmodium tubulin determine distinct microtubule architectures, mechanics and drug susceptibility. Nat Commun 17, 2275 (2026). https://doi.org/10.1038/s41467-026-70181-0
Nyckelord: malariaparasit, mikrotubuli, tubulinstruktur, läkemedelsmål, kryoelektronmikroskopi