Clear Sky Science · sv
Kovalent “warhead”-sammanställning i fostriecinbiosyntes involverar malonylation–laktonisering av en bifunktionell tioesteras och enzymatisk demalonylation
Hur naturen bygger ett mikroskopiskt kemiskt “warhead”
Cancerläkemedel och antibiotika förlitar sig ofta på några få atomer ordnade på ett mycket precist sätt — ett litet ”warhead” som låser fast vid ett protein och stänger av dess funktion. Den naturliga föreningen fostriecin är ett sådant molekylärt vapen, med kraftfull aktivitet mot enzymer som är involverade i celltillväxt. Men dess komplexa struktur gör den svår att framställa eller modifiera i laboratoriet. Denna studie kartlägger steg för steg hur bakterier bygger fostriecins avgörande warhead och avslöjar enzymatiska knep som kemister nu kan låna för att designa nya läkemedel.
Det speciella krokar i potenta naturprodukter
Många lovande läkemedel från jordbakterier tillhör en familj som kallas polyketider. Inom denna familj finns en undergrupp som bär en reaktiv ring, känd för kemister som en α,β-omättad δ-lakton, som fungerar som en molekylär fiskkrok. Den kan bilda en permanent bindning med vissa aminosyror i proteiner och slå av viktiga biologiska brytare. I fostriecin och besläktade molekyler är denna krok kombinerad med en fosfatgrupp som hjälper dem att hitta specifika enzymer som styr celldelning. Dessa egenskaper gör dem attraktiva som antitumörområden, men samma reaktivitet och strukturella komplexitet gör dem svåra att syntetisera och instabila vid lagring.
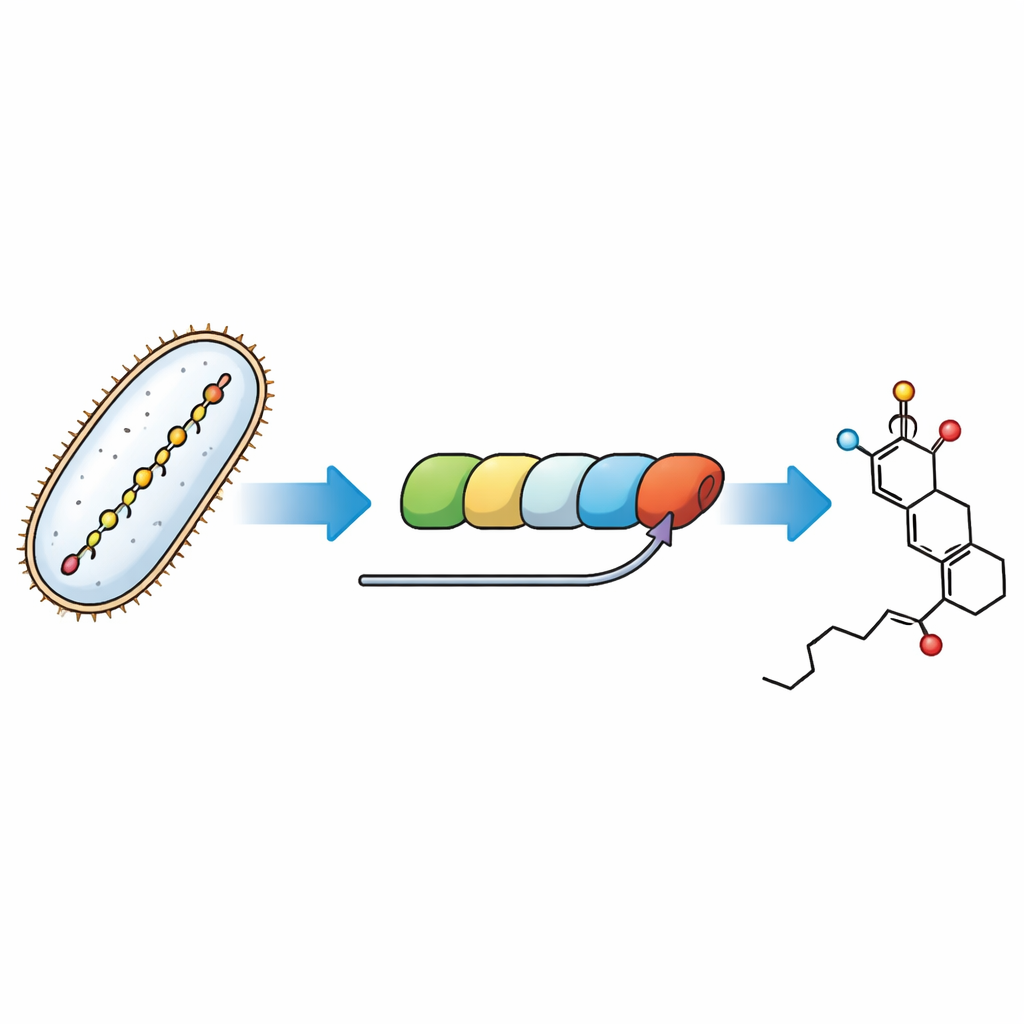
Spåra de sista stegen i en molekylär monteringslinje
Bakterier bygger fostriecin med ett massivt modulärt proteinkomplex kallat en polyketidsyntas — en monteringslinje där varje station förlänger och formar en växande kolkedja. Gåtan som behandlas här är hur den sista modulen i denna maskin smider warhead-ringen och inför ett tillfälligt ”handtag” kallat en malonylgrupp som senare måste tas bort. Genom att återskapa vägen i provrör med renade enzymer och noggrant utformade småmolekyl-substitut för de naturliga mellanprodukterna kunde forskarna följa enskilda steg och koppla dem till specifika delar av monteringslinjen.
Ett multitaskande enzym med en oväntad talang
Teamet upptäckte att den sista stationen i monteringslinjen, en domän kallad FosTE, beter sig på ett sätt som inte setts tidigare. Typiska versioner av denna domän klipper enkelt färdiga produkter från linjen. FosTE, däremot, fångar först en malonylfragment från en vanlig cellulär byggsten och för över den till en specifik syreatom på den växande kedjan, och underlättar sedan att kedjan böjer sig för att sluta sig till warhead-ringen. Mutation av en enda reaktiv serinaminosyra i FosTE slår ut båda aktiviteterna. Strukturell modellering pekar ut två positivt laddade argininrester i det aktiva sätet som omsluter malonylfragmentet och positionerar det för överföring — funktioner som normalt hanteras av en annan typ av enzym. Att byta dessa argininer mot neutrala rester tar bort malonylöverföringssteget samtidigt som den grundläggande ringbildningen i stor utsträckning förblir intakt, vilket bekräftar deras avgörande roll.
Låsa fast warheaden och förhindra spill
När ringen har bildats och bär sin tillfälliga malonylgrupp måste ett annat enzym, FosM, avlägsna denna grupp för att blotta det fullt beväpnade warheadet. Studien visar att FosM arbetar effektivt endast efter att ännu ett enzym, en bredspecificitetskinas kallad FosH, har tillsatt en fosfat på en närliggande position i molekylen. När forskarna tillförde den malonylerade ringen till FosM ensam skedde endast måttlig omvandling. Att tillsätta FosH först ledde till nästan fullständig borttagning av malonylgruppen och bildandet av den slutliga reaktiva enheten. Viktigt är att FosH också kan fosforylera relaterade ”shunt”-mellanprodukter som uppstår från sidoreaktioner, och på så sätt rädda dem så att de kan bearbetas korrekt istället för att gå förlorade som återvändsgränder.
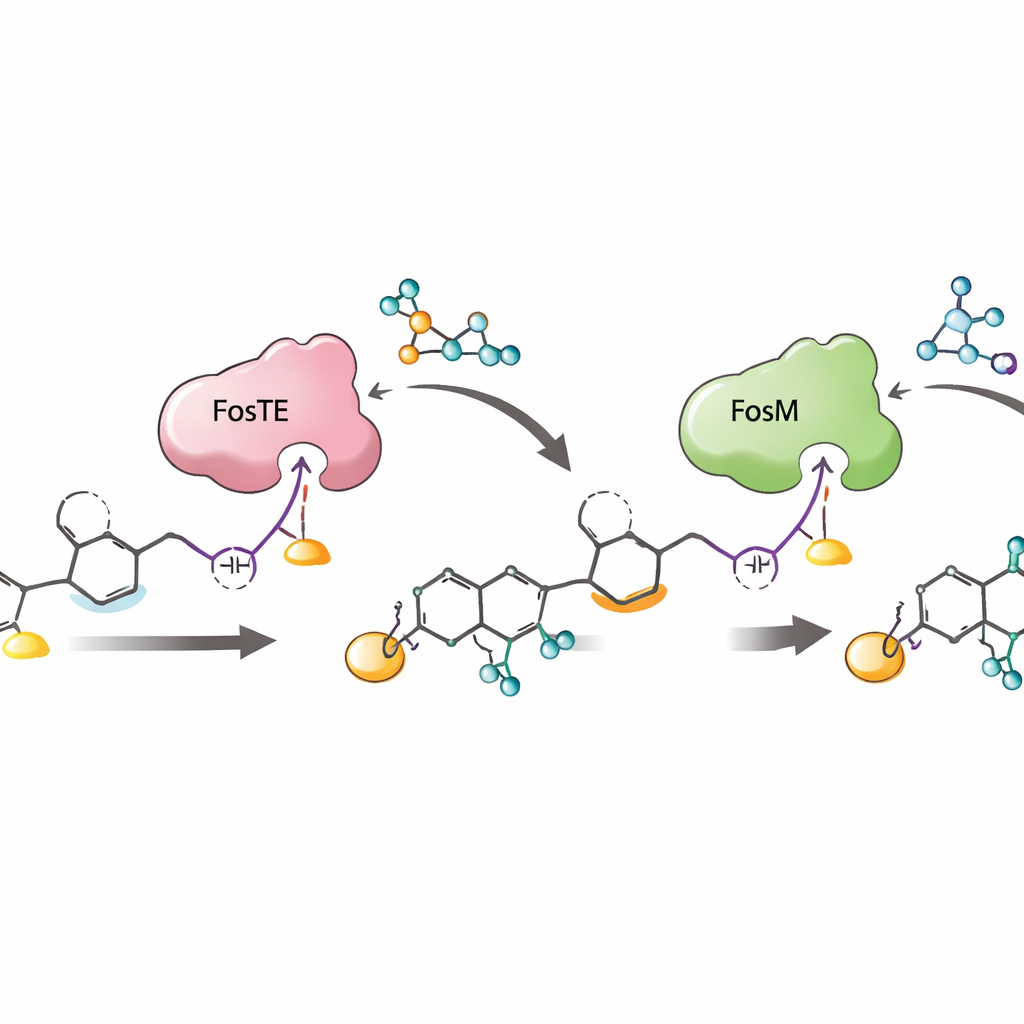
Varför denna enzymatiska koreografi är viktig
Tillsammans avslöjar arbetet en tätt koreograferad sekvens: kedjeförlängning på monteringslinjen, FosTE-styrd malonyladdition och ringstängning, FosH-fosforylering och slutligen FosM-utriggerad malonylborttagning. Denna ordning bygger inte bara effektivt det ömtåliga warheadet, den skyddar också instabila mellanprodukter från att falla sönder och maximerar produktionen av den önskade, fosforylerade formen som är mest aktiv som ett läkemedelsled. Genom att visa hur en enda enzymdomän både kan dekorera och släppa en växande molekyl — och hur partnerenzym finjusterar och räddar reaktiva mellanprodukter — erbjuder studien en ritning för att konstruera nya polyketider med warheads och för att bygga kortare, mer effektiva syntetiska vägar till komplexa antitumöra agenter som fostriecin.
Citering: Nguyen, L.N.K.T., Schlotte, L., Hoffmann, J. et al. Covalent warhead assembly in fostriecin biosynthesis involves malonylation-lactonisation by a bifunctional thioesterase and enzymatic demalonylation. Nat Commun 17, 2365 (2026). https://doi.org/10.1038/s41467-026-70144-5
Nyckelord: fostriecin, polyketidbiosyntes, enzymteknik, naturliga produkters warheads, kemoenzymatisk syntes