Clear Sky Science · sv
Translationell reglering genom oxidativ desulfuration av tRNA-modifikationer
Hur celler finjusterar proteinproduktion vid stress
Varje cell måste besluta vilka proteiner som ska produceras, hur snabbt de ska tillverkas och när produktionen ska dämpas. Denna studie avslöjar en subtil kemisk brytare på transfer-RNA (tRNA)-molekyler som hjälper celler att skruva ned proteinproduktionen när cellens miljö blir mer oxiderande, som vid inflammation eller metabol stress. Genom att följa hur denna brytare beter sig i däggdjursceller och i provrörssystem identifierar forskarna ett nytt sätt där skadeliknande förändringar i RNA faktiskt kan fungera som en regleringssignal.
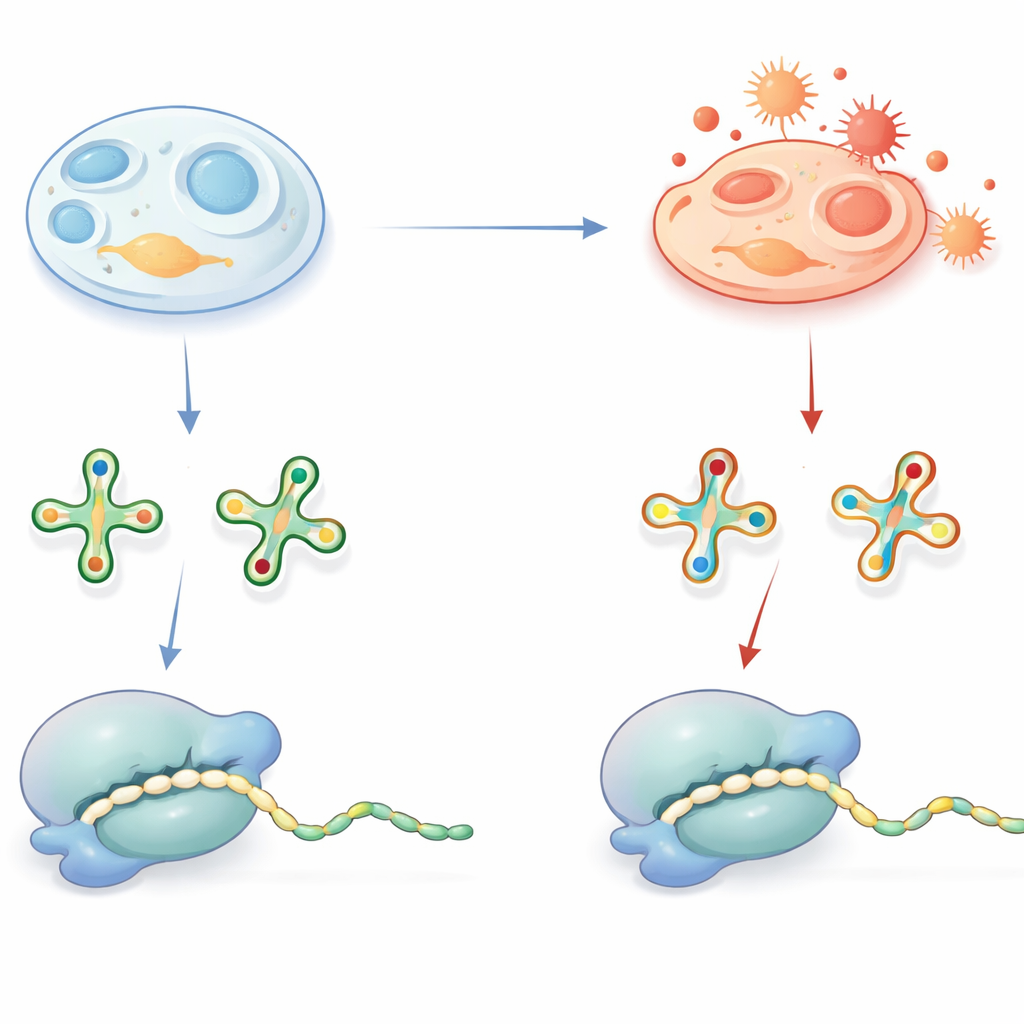
Små märken på tRNA med stora konsekvenser
tRNA fungerar som adaptrar som läser trebokstavs “ord” i budbärar-RNA och levererar motsvarande aminosyror under proteinsyntesen. För att göra detta arbete korrekt och effektivt bär många tRNA särskilda kemiska dekorationer, särskilt vid en nyckelposition som kontaktar den tredje bokstaven i varje kodon. En utbredd dekoration är en svavelhaltig grupp på en uridinbas, ofta skriven som en 2-thiouridin-derivat. Under friska förhållanden hjälper denna svavelgrupp tRNA att känna igen rätt kodon som slutar på bokstäverna A eller G och stöder snabb, felfri translation. Brister i dessa dekorationer är redan kända för att orsaka mänskliga sjukdomar, vilket betonar deras betydelse.
När oxidativ stress skriver om tRNA
Den svavelgrupp som förbättrar avkodningen har en nackdel: den är kemiskt känslig för oxidation. Gruppen frågade om denna grupp faktiskt tas bort inne i celler under oxiderande förhållanden, och vad det skulle innebära för proteinsyntesen. Med känslig masspektrometri identifierade de oxiderade, svavelfria versioner av dessa tRNA-baser—kallade h2U-derivat—i musvävnader, gris-mitokondrier, bakterier, jäst och en rad humana cellinjer. Ett smart spike-in-experiment med en bakteriell tRNA-tracer visade att dessa h2U-märken inte är artefakter skapade under provberedningen utan bildas inne i levande celler. Även om de oxiderade versionerna bara fanns i en bråkdel av tRNA, varierade deras förekomst mellan vävnader och celltyper, vilket tyder på att cellens redox-tillstånd och antioxidantkapacitet påverkar hur ofta denna omvandling sker.
Hur oxiderade tRNA bromsar monteringslinjen
Forskarna testade nästa hur dessa förändrade tRNA presterar under proteinsyntes. De omvandlade kemiskt den svavelbärande formen till den oxiderade h2U-formen i bulk-tRNA och använde ett fullständigt rekonstituerat humant translationssystem in vitro. Ett rapportprotein vars produktion starkt beror på dessa modifierade tRNA visade kraftigt minskad produktion när tRNA:na desulfuriserades, medan en kontrollrapportör som undviker de påverkade kodonen översattes utan problem. Biokemiska analyser visade varför: oxiderade tRNA för lysin, glutamin och glutamat laddades med sina aminosyror mycket mindre effektivt, medan motsvarande arginin-tRNA i stort sett undgick påverkan. Viktigt är att h2U-bärande tRNA fortfarande återfanns i ribosombundna (polysomala) fraktioner från celler, vilket indikerar att de deltar i translation men gör det dåligt.
En strukturell bild av försvagad avkodning
För att se exakt hur oxidation förändrar avkodningen använde teamet högupplöst kryogen elektronmikroskopi för att avbilda bakteriella ribosomer programmerade med humant lysin-tRNA och specifika kodon. I det normala, svavelbärande tillståndet bildade den modifierade basen vid tRNA:s “wobble”-position antingen ett standardbaspar med ett A-slutet kodon eller ett särskilt wobble-par med ett G-slutet kodon, båda väl inbäddade i ribosomens avkodningscenter. Efter desulfuration kunde samma bas endast göra en enda svag kontakt med det A-slutna kodonet och bildade ett mindre stabilt wobble-par med det G-slutna kodonet. Bindningsexperimenten stämde överens med dessa strukturer: oxiderat lysin-tRNA förlorade i princip förmågan att känna igen AAA-kodonet och kände igen AAG-kodonet mycket mindre effektivt. Tillsammans visar dessa fynd att en till synes liten kemisk justering kan översättas till kodon-specifika långsammare steg i proteinsyntesen.
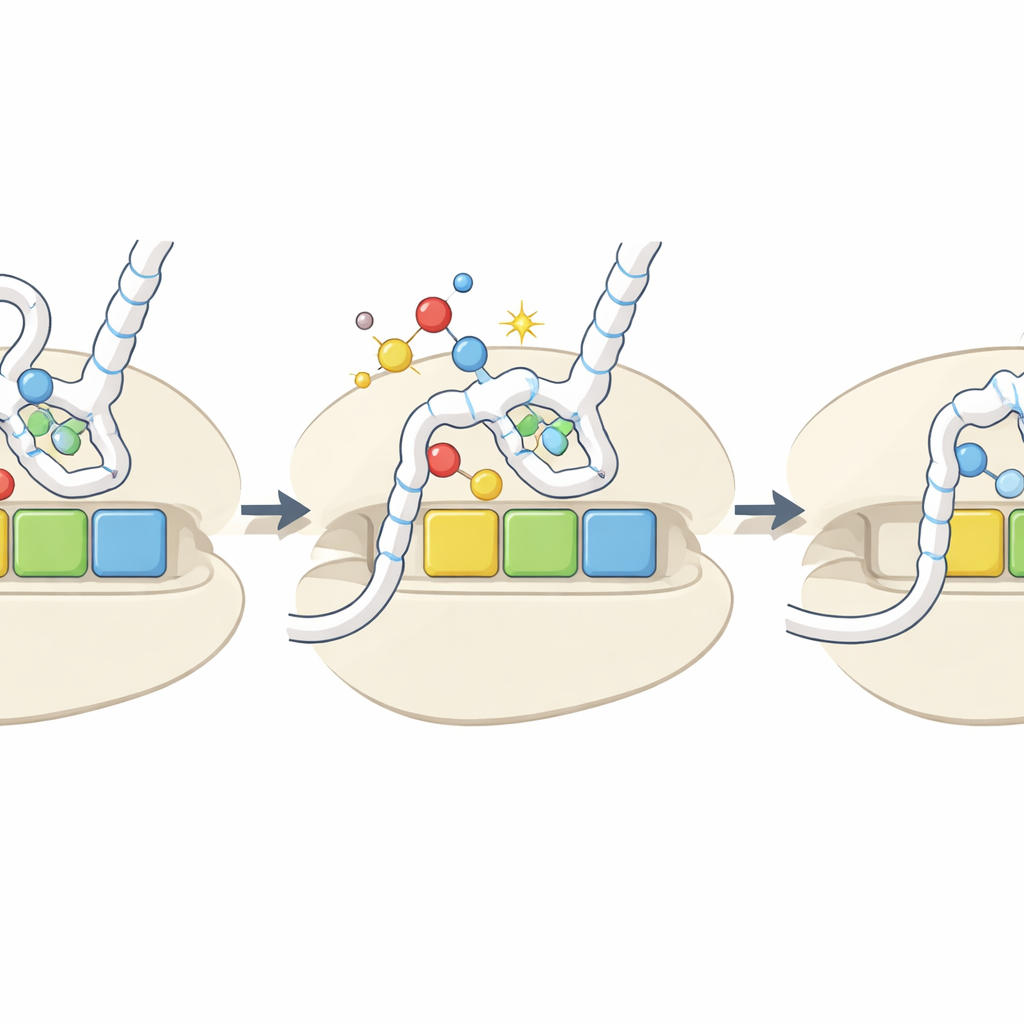
En signalskada som blir en regleringsvred
Sammanfattningsvis föreslår studien att oxidativ borttagning av svavel från nyckelbaser i tRNA fungerar som en inbyggd sensor för cellens redoxmiljö. Under oxidativ stress omvandlas fler tRNA till h2U-formen, vilka laddas dåligt och binder svagt till vissa kodon. Detta saktar selektivt ner translationen vid dessa kodon, vilket potentiellt kan förändra stabiliteten hos påverkade mRNA, ändra hur proteiner veckas och utlösa stresstransduktionsvägar när ribosomer fastnar. Även om de oxiderade märkena är relativt sällsynta och deras nivåer inte alltid stiger kraftigt under experimentell stress, innebär deras kodon- och aminosyra-specifika effekter att även måttliga förändringar kan omforma vilka proteiner som tillverkas och hur snabbt under svåra förhållanden.
Citering: Mo, Y., Ishiguro, K., Miyauchi, K. et al. Translational regulation by oxidative desulfuration of tRNA modifications. Nat Commun 17, 2125 (2026). https://doi.org/10.1038/s41467-026-70126-7
Nyckelord: tRNA-modifikation, oxidativ stress, proteinsyntes, translationsreglering, RNA-skada