Clear Sky Science · sv
Målstyrning av tRNA-beroende tyrosinanvändning avslöjar en metabolisk sårbarhet vid hepatocellulärt karcinom
Att svälta ut cancerceller från en vanlig byggsten
Leverceller som cancer, liksom alla snabbt delande celler, behöver en stadig tillförsel av aminosyror — de små byggstenarna i proteiner. Denna studie visar att hepatocellulärt karcinom, den vanligaste formen av levercancer, har en oväntad svaghet: det är starkt beroende av aminosyran tyrosin för både energiproduktion och överlevnad. Genom att selektivt begränsa hur cancerceller använder tyrosin kunde forskarna bromsa tumörtillväxt, skada cellernas kraftverk och utlösa en form av celldöd som kan utnyttjas för nya behandlingar.
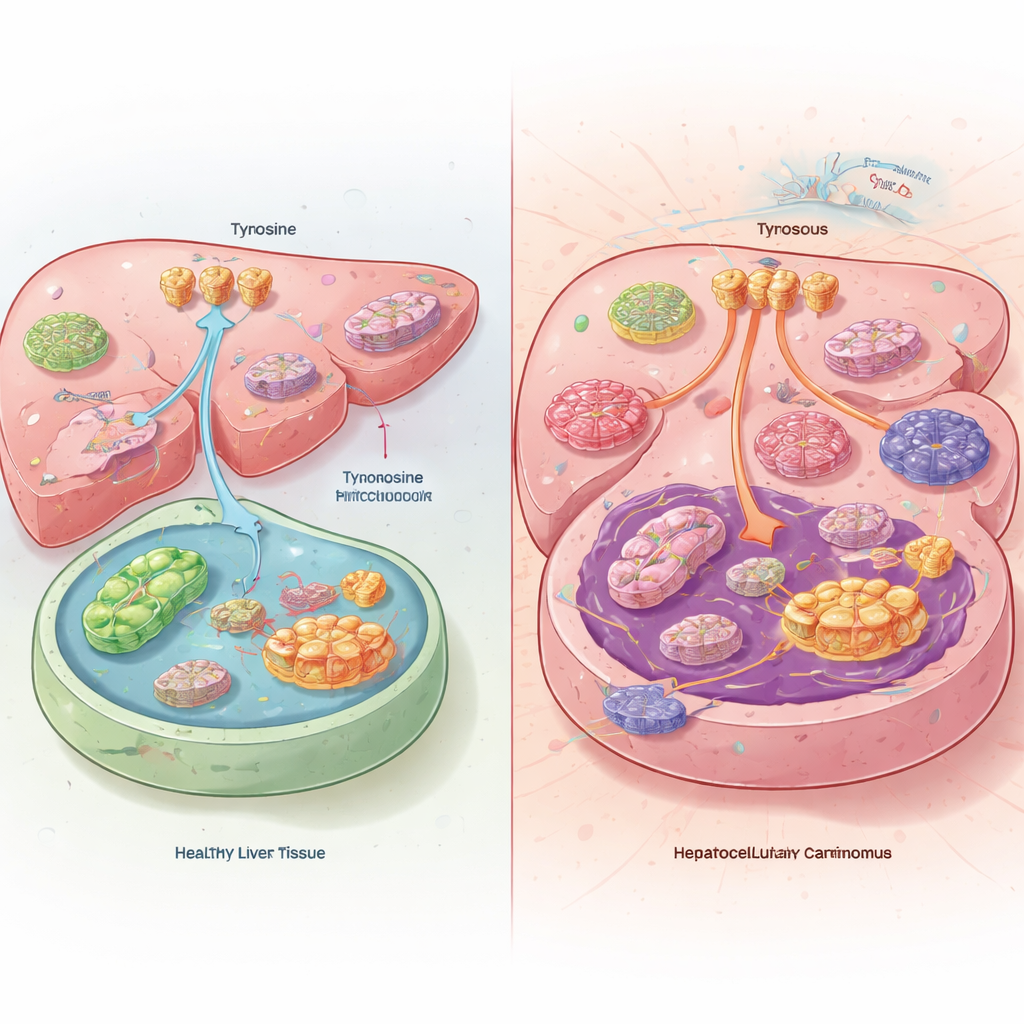
En dold obalans i levertumörer
När teamet jämförde levertumörer med frisk levervävnad från patienter och möss fann de något förbryllande. Inuti cancercellerna var nivåerna av tyrosin faktiskt låga, trots att tumörerna drog in mer tyrosin från blodomloppet och bröt ned mindre av det. Istället för att elda tyrosin som bränsle omdirigerade levertumörer det till proteinproduktion. Cancern uppnådde detta genom att öka aktiviteten hos tyrosintransportörer i cellmembranet och dämpa de enzymer som normalt bryter ned tyrosin i levern. Möss som fick en tyrosinfri diet utvecklade mindre tumörer och levde längre, medan extra tyrosin i kosten fick deras cancer att växa snabbare.
Hur cancern omkopplar proteinproduktionen
Forskarna spårade denna tyrosin-hunger till en kraftfull cancerdrivande gen kallad MYC. I levertumörer slår MYC på ett protein som heter YARS1, vilket kopplar tyrosin till ett specifikt transfer-RNA (tRNA-TyrGUA). Detta laddade tRNA är vad ribosomerna behöver för att bygga tyrosinrika proteiner. Studien visade att levercancrar ökar både YARS1 och dess matchande tRNA, vilket säkerställer en privilegierad pipeline av tyrosin in i proteinsyntesen. Att störa denna pipeline — antingen genom att sänka tyrosinnivåerna, slå ner YARS1 eller tRNA-TyrGUA, eller blockera tyrosinladdningen — gjorde levercancerceller mycket mindre livskraftiga i odlingar och i möss, och blottade en metabolisk sårbarhet tätt kopplad till deras höga behov av proteinproduktion.
Att slå ut kraftverken och fettbalansen
Genom att kombinera genomskafferi av RNA-, protein- och metabolitmätningar identifierade teamet två särskilt känsliga mål för tyrosinbegränsning. Det ena, NDUFB8, är en komponent i mitokondriellt komplex I, en central del av cellens energiproducerande maskineri. Det andra, SCD1, hjälper till att omvandla mättade fetter till enkelomättade fetter som är säkrare att lagra i cellmembran och droppar. När tyrosin för translation begränsades sjönk produktionen av NDUFB8 och SCD1, medan deras RNA-nivåer till stor del förblev oförändrade — tydligt bevis på att translationen, inte genuttrycket, påverkades. Det ledde till dåligt ihopbyggt komplex I, minskad cellandning, överskott av reaktiva syreföreningar och en förskjutning i fettsammansättningen från enkelomättade till mer sköra fleromättade former som lätt oxideras.
Tvinga cancerceller in i järn-driven död
Den kombinerade mitokondriella skadan och de instabila fetterna pressade levercancerceller mot ferroptos, en järnberoende form av celldöd driven av lipidperoxidation. Tumörerna försökte försvara sig genom att öka naturliga ferroptosblockerare såsom GPX4 och närliggande molekyler, men en stor CRISPR-genredigeringsskärm visade att försvagning av dessa skydd gjorde tyrosinbegränsningen ännu mer dödlig. I cell- och musmodeller gav kombinationer av tyrosinbegränsande strategier med läkemedel som hämmar GPX4 eller BCL2 — eller med befintliga levercancerläkemedel som sorafenib och venetoclax — starkare tumörkontroll, mindre tumörbörda och längre överlevnad.
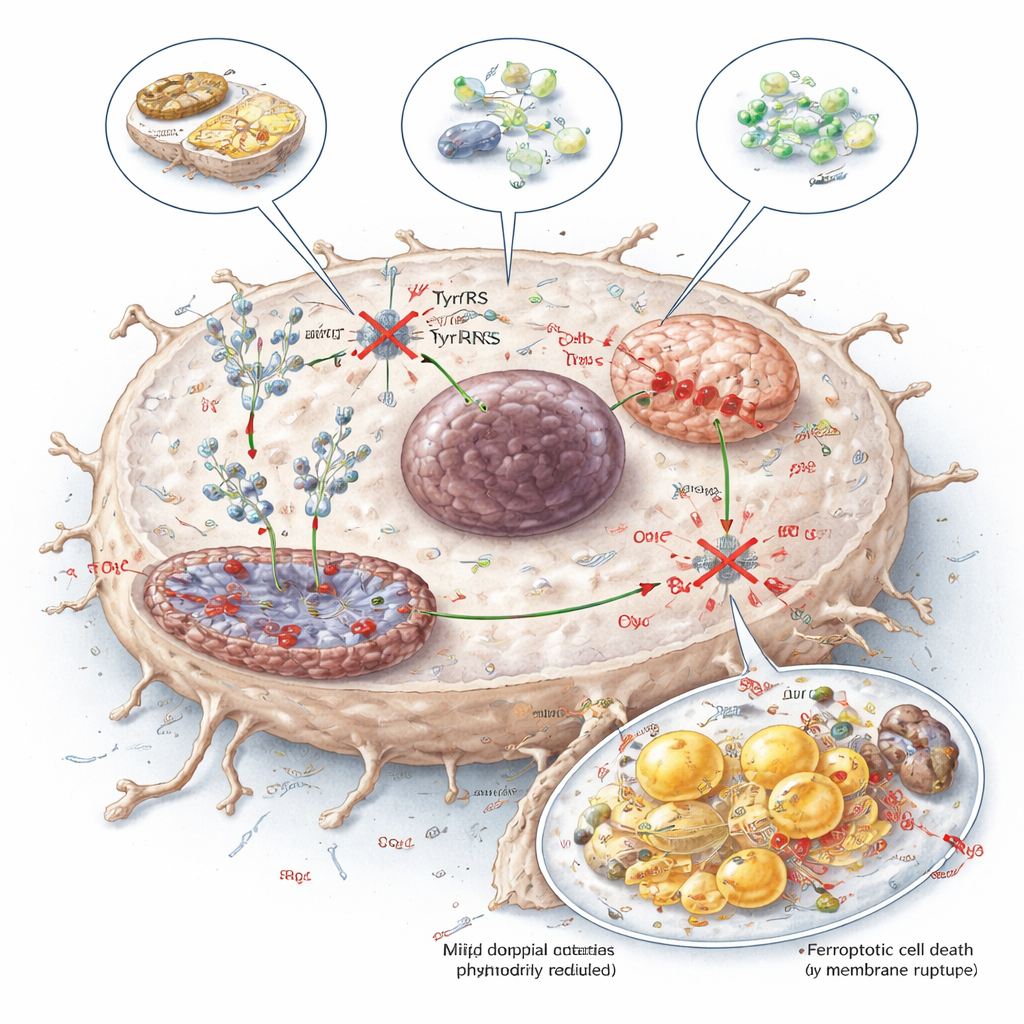
Att omvandla en metabolisk svaghet till terapi
För att utforska praktiska sätt att utnyttja denna svaghet testade forskarna tre angreppssätt: en tyrosinbegränsad diet, ett enzym (TAL) som enzymatiskt bryter ned tyrosin, och en liten molekyl kallad tyrosinol som konkurrerar med tyrosin om bindning till YARS1. Alla tre minskade tillgängligheten av tyrosin för proteinsyntes, sänkte nivåerna av NDUFB8 och SCD1, skadade mitokondriefunktionen och ökade ferroptos i levertumörer, samtidigt som de visade hanterbara effekter på normal vävnad i möss. För en lekman är budskapet att levercancer verkar vara beroende av tyrosin inte bara som näring, utan som ett precist bränsle för deras proteinskapande maskineri. Att rikta in sig på detta beroende — via kost, enzymer eller läkemedel — erbjuder ett lovande nytt sätt att försvaga tumörer och förstärka effekten av befintliga behandlingar.
Citering: Zhang, H., Wang, Z., Zhao, Y. et al. Targeting tRNA-dependent tyrosine usage unveils a metabolic vulnerability in hepatocellular carcinoma. Nat Commun 17, 2244 (2026). https://doi.org/10.1038/s41467-026-70112-z
Nyckelord: levercancer, aminosyrametabolism, tyrosin, mitokondrier, ferroptos