Clear Sky Science · sv
Optimera den rumsliga organiseringen av FtsZ‑ringar för storskalig sammandragning i syntetiska celler
Varför små ringar spelar roll för att bygga syntetiska celler
Föreställ dig att konstruera en enkel, artificiell cell som kan växa och dela sig självständigt. För att lyckas måste forskare lära sig hur man klämmer åt ett mjukt, tvålbubbel‑liknande membran på ett kontrollerat sätt med hjälp av bara några biologiska komponenter. Denna studie visar hur ett bakteriellt protein kan hjälpas att bilda stora, stabila ringar på jättefettbubblor, vilket gör att dessa modell»celler» kan dra ihop sig nästan ända till delning. Den avslöjar vilken typ av proteinarkitektur som krävs för att böja och omforma ett membran i cellskalans storlek.
Låna naturens uppsättning för delning
Många bakterier delar sig med hjälp av ett protein som heter FtsZ, en avlägsen släkting till tubulin som bygger våra egna cellers inre skelett. FtsZ sätter ihop sig till filament som samlas i en ring vid cellens mitt och markerar var cellen kommer att dela sig. I levande bakterier fäster en mängd hjälpproteiner den här ringen vid det inre membranet, positionerar den i mittcellen och länkar den till enzymer som omformar cellväggen. Tidigare försök i laboratoriet att återskapa denna maskineri i stora, cellstora vesikler lyckades bilda ringar och framkalla små inbuktningar i membranet, men inte en jämn, progressiv sammandragning som formar en jättevesikel till två nästan separata halvor.
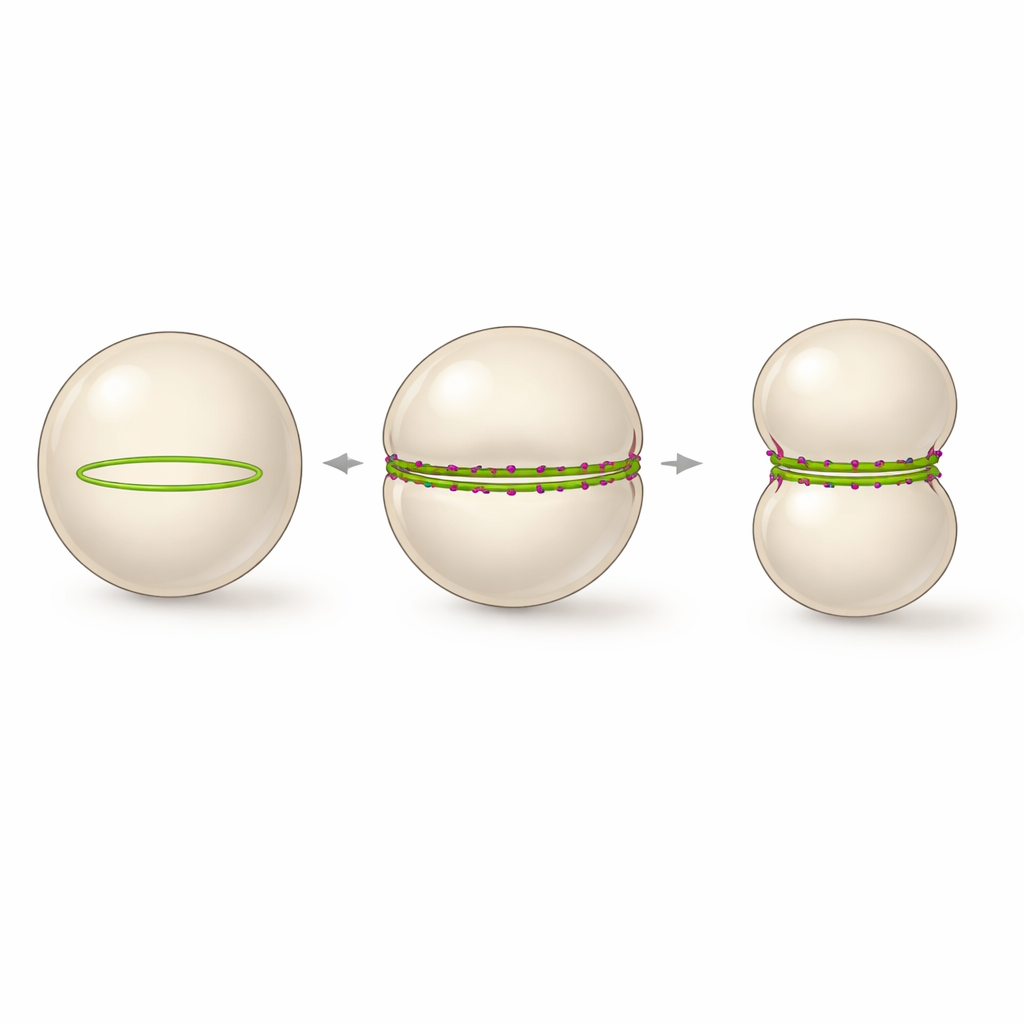
En minimalistisk väg till ett delande skal
Författarna undrade om de kunde skalas ner systemet till bara två delar: en variant av FtsZ som kan fästa direkt vid membran och en kort positivt laddad svans från ett annat delningsprotein, FtsN. De kapslade in dessa komponenter i jätte‑unilamellära vesikler — ihåliga lipidkulor som liknar förenklade celler — och tillförde energimolekylen GTP samt en långsamt verkande GTP‑mimet för att finjustera proteindynamiken. Utan FtsN‑svansen bildade FtsZ många små ringar och fläckar som bara orsakade lokala inbuktningar. Med ett överskott av FtsN‑fragmentet (kallat cytoFtsN) omorganiserades de små ringarna till en enda, stor ring som omslöt vesikeln nära ekvatorn och kunde dra ihop sig över flera timmar.
Från ett sammantrasslat nätverk till en enda kontraktila ring
För att förstå hur denna lilla peptid förändrar beteendet så dramatiskt observerade teamet FtsZ‑filament på platta, stödda membran med högupplöst mikroskopi. Vanligtvis bildar FtsZ på sådana ytor virvlande, böjda vortexar. När man tillsatte ökande mängder cytoFtsN suddades dessa spiraler gradvis ut och ersattes av rakare, mer ihopriktade buntar. Kvantitativ bildanalys bekräftade att nätverket blev mer koherent och ordnat när peptidkoncentrationen ökade. Fluorescensåterhämtningsförsök visade att subenheter inom dessa buntar byttes ut långsammare, vilket tyder på att peptiden stabiliserar filamenten och minskar deras omrörande dynamik.

Elektrostatisk »Velcro» som låser filamenten tillsammans
Biokemiska mätningar visade att cytoFtsN och FtsZ främst interagerar genom motsatta elektriska laddningar: FtsZ är överlag negativt laddat, medan peptiden bär kluster av positiva laddningar. Vid lägre saltsalter bundet peptiden starkare, främjade bildningen av tjockare FtsZ‑buntar i lösning och bromsade nedbrytningen av filament genom att dämpa proteinets GTP‑förbrukning. När forskarna förändrade nyckelresiduer med positiv laddning i peptiden eller ökade saltkoncentrationen för att skärma av elektrostatisk attraktion försvann effekterna på buntning och omorganisation. Detta pekar på en enkel fysisk mekanism där den positivt laddade peptiden fungerar som ett molekylärt »Velcro» som minskar repulsionen mellan FtsZ‑filament så att de kan packas sida vid sida till styva buntar.
Hur en enda ring omformar en jättevesikel
Inuti vesiklar får denna peptidstabiliserade buntning en slående följd. Istället för många små böjda ringar tvingas de utsträckta FtsZ‑buntarna följa vesikelns stora krökning och monterar sig i en kontinuerlig ring som spänner över hela omkretsen. Tidsförloppsavbildning visade att när en sådan helt sluten ring bildades deformeras vesikeln pålitligt från en sfär till en hantelform, med en snäv midja där ringen satt. Processen kunde följas i realtid när vesikelns diameter krympte och sammandragningen fördjupades, nästan så att utrymmet delades i två, även om slutlig snörning inte uppnåddes. Författarna föreslår att en stabil FtsZ‑ring som spänner över ekvatorn med fördröjd men fortfarande aktiv omsättning är den minimala arkitektur som krävs för att driva storskalig membransammandragning i en syntetisk cell.
Vad detta betyder för framtidens syntetiska liv
Genom att visa att en membranankrad FtsZ‑variant plus en kort kationisk peptid kan omforma jätte‑lipidvesikler nästan till delning fastställer arbetet en tydlig designregel för artificiella celler: en enda, sammanhängande proteinring som matchar cellens storlek och är mekaniskt stabil över tid räcker för att nypa åt en mjuk gräns i cellskala. Mer komplexa faktorer kan fortfarande krävas för att helt skära igenom membranet, men studien visar att kontrollerad storskalig sammandragning inte kräver en full uppsättning bakteriella delningsproteiner. Istället kan noggrann justering av filamentorganisation och dynamik förvandla ett enkelt proteinskelett till en effektiv kontraktil ring, vilket för de verkligt självdelande syntetiska cellerna ett steg närmare verklighet.
Citering: Panevska, A., Šakanović, A., Paccione, G. et al. Optimizing spatial organization of FtsZ rings for large-scale constriction in synthetic cells. Nat Commun 17, 2320 (2026). https://doi.org/10.1038/s41467-026-70091-1
Nyckelord: syntetisk celldelning, FtsZ‑ring, membransammandragning, minimalt divisom, cytoskelettens självorganisering