Clear Sky Science · sv
Subcellulär proteomik avslöjar en ritning för endosymbiontintegration i trypanosomatiden Angomonas deanei
Dolda partner i encelligt liv
Många encelliga organismer är inte egentligen ensamma. Vissa hyser bakterier som lever inuti dem som permanenta hyresgäster och byter näring och tjänster i relationer som påminner om hur våra egna mitokondrier uppstod. Denna studie undersöker ett sådant partnerskap i Angomonas deanei, en mikroskopisk insektparasits, för att visa hur en en gång fri levande bakterie blivit djupt invävd i värdcellens inre funktioner.
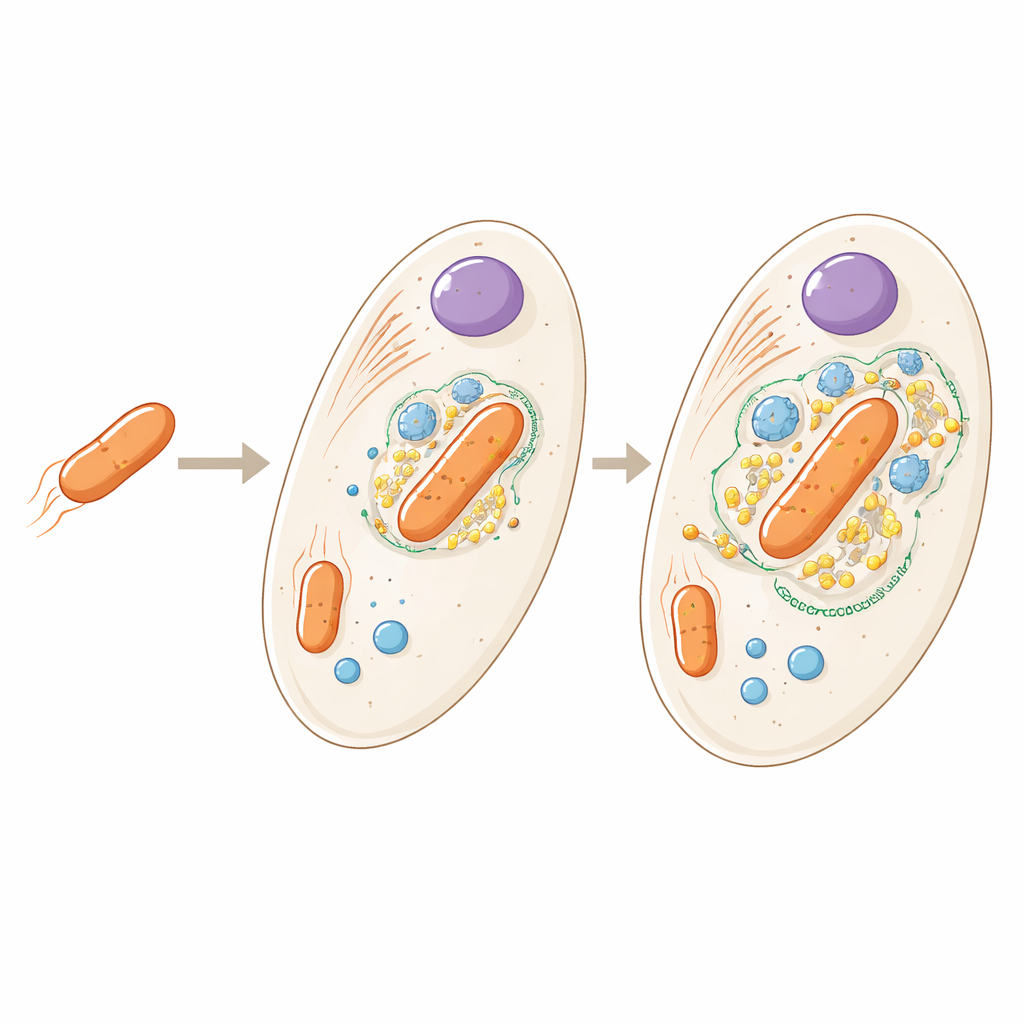
Från husgäst till inbyggd del
Bakterien som lever inne i Angomonas deanei är en avlägsen släkting till fritt levande jordmikrober, men här förekommer den som en enda kopia per värdcell och kan inte längre överleva på egen hand. Tidigare arbete visade att värden producerar särskilda proteiner som transporteras in i bakterien och till och med hjälper till att styra när den delar sig. Den nya studien ställer en bredare fråga: om vi tittar över hela cellen, var finns alla värd- och bakterieproteiner exakt, och vad säger det om hur tätt de två partnerna är integrerade?
Kartläggning av cellens innerstad
För att svara på detta bröt forskarna försiktigt upp stora mängder celler så att interna strukturer i huvudsak förblev intakta. De separerade sedan dessa delar genom att snurra dem i olika hastigheter och identifierade tusentals proteiner i varje fraktion med högupplöst masspektrometri. Genom att jämföra hur proteiner klustrade över fraktionerna och korskontrollera med kända markörer och fluorescensmikroskopi skapade de en detaljerad “adressbok” för cellen och tilldelade nästan 3 000 proteiner till 21 distinkta regioner såsom kärnan, mitokondrien, specialiserade lagringskroppar och själva den bakterieendosymbionten.
Värdens verktyg riktade mot den kvarboende bakterien
I denna atlas upptäckte teamet en uppsättning värdproducerade proteiner som konsekvent följde med endosymbionten och utvidgade den kända samlingen av så kallade endosymbionttargeterade proteiner. Ett nyligen bekräftat exempel, kallat ETP10, täcker bakterien på ett sätt som liknar ett tidigare protein, vilket tyder på ett skelett av värdfaktorer som omsluter den mikrobiella partnern. En annan liten grupp proteiner delade ett ovanligt fysikaliskt beteende med ett dynaminliknande protein som redan är känt för att knipa åt bakterien under delning. Tillsammans antyder dessa fynd en specialiserad, värdbyggd maskineri avsett för att positionera, forma och reproducera endosymbionten inne i cellen.
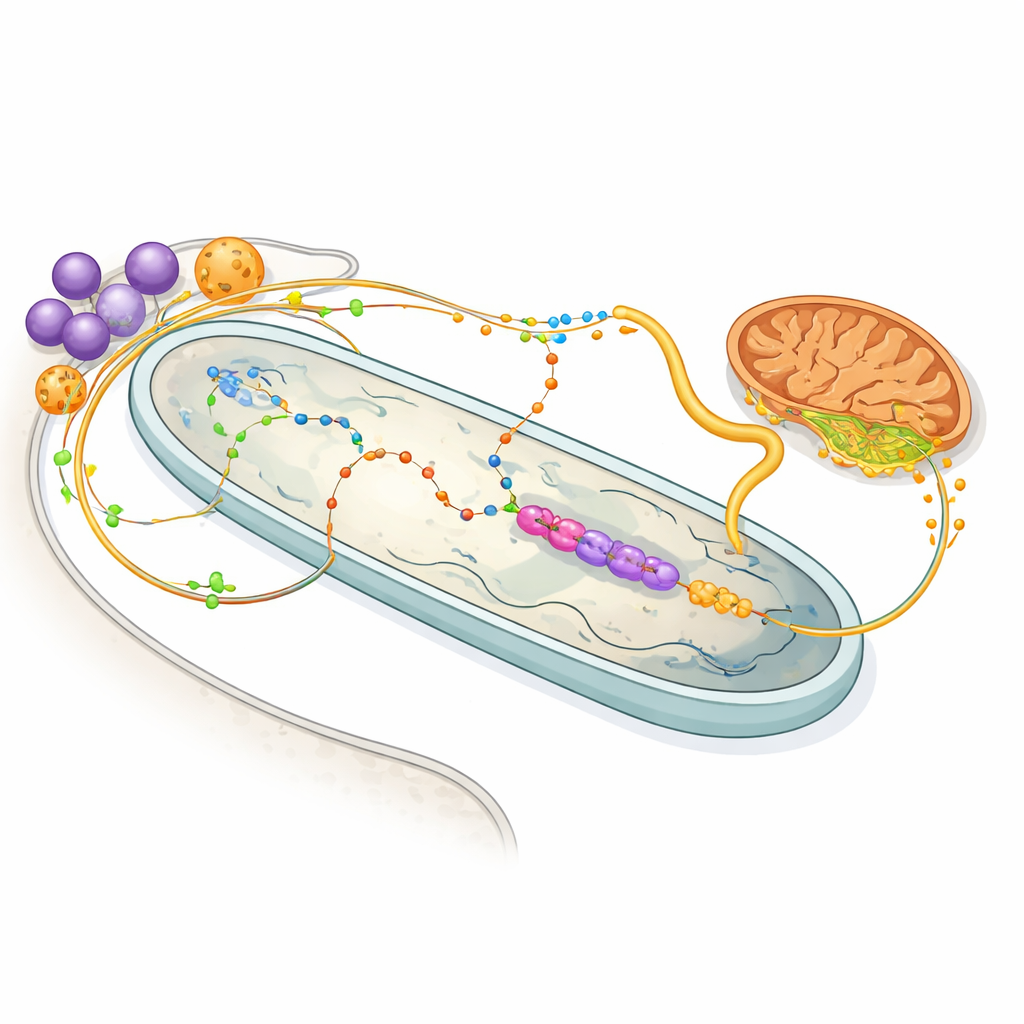
Energidelning och kemiska handelsvägar
Proteinmappen belyser också det livliga utbytet av molekyler mellan värd och bakterie. Enzymer i värdens glykosomer — organeller som hanterar socker- och aminosyrametabolism — verkar inriktade på att mata bakterien med aminosyran prolin och föreningen 2‑oxoglutarat, båda värdefulla energikällor. Inne i bakterien använder en avskalad uppsättning enzymer 2‑oxoglutarat för att generera NADH, som driver en minimal andningskedja, för att sedan lämna över succinat tillbaka till värdens mitokondrie. Andra vägar visar att bakterien utför de flesta stegen i syntesen av heme, ett nödvändigt pigment för värden, samtidigt som den bidrar med viktiga byggstenar för nukleotider. I praktiken har varje partner lagt över specifika metaboliska uppgifter på den andra och skapat ett delat, ömsesidigt beroende system.
Nya kommunikationslinjer inne i cellen
Utöver metabolismen avslöjar studien fysiska och sannolikt signaliserande länkar mellan endosymbionten och andra organeller. En särskild grupp av värdproteiner bildar det författarna kallar ett ”kontaktställe”-kluster, berikat på komponenter från kärnmembranet och det endoplasmatiska retiklet som fysiskt medsedimenterar med bakterien. Två typer av lagringsorganeller — glykosomer och acidokalcisomer — förekommer i två populationer: vissa förblir fria i cytoplasman medan andra konsekvent färdas med bakterien. Mikroskopi bekräftar att delmängder av dessa organeller ligger tätt intill endosymbionten. Acidokalcisomer är kända som kalcium- och fosfatreservoarer, så deras nära inpassning antyder en tvåvägs signal- och jontrafikruta som förbinder bakterien, dessa förråd och det närliggande endoplasmatiska retiklet.
En ritning för liv inbyggt i liv
Sammantaget ger detta arbete en rik, cellomfattande ritning för hur en bakterie kan bli funktionellt förenad med sin värd utan att ännu förvandlas till ett fullfjädrat organell som mitokondrien. Angomonas deanei är beroende av sin endosymbiont för viktiga näringsämnen, medan bakterien i sin tur är beroende av värdproducerade proteiner och energirika molekyler och är förankrad vid värdorganeller för kommunikation och kontroll. För icke-specialister är slutsatsen att evolutionen kan successivt hårdkoda samarbete mellan mycket olika livsformer, steg för steg, tills det blir omöjligt att separera dem. Detta system erbjuder en levande ögonblicksbild av den processen i arbete och hjälper forskare att bättre förstå hur komplexa celler som våra egna en gång uppstod från enklare början.
Citering: Hammond, M., Chmelová, Ľ., van Geelen-Kuenzel, N.A. et al. Subcellular proteomics reveals a blueprint for endosymbiont integration in trypanosomatid Angomonas deanei. Nat Commun 17, 2241 (2026). https://doi.org/10.1038/s41467-026-70084-0
Nyckelord: endosymbios, cellmetabolism, organellevolution, protistbiologi, värd-mikrob-interaktioner