Clear Sky Science · sv
Den dynamiska fördelningen av genetiska tandemförstärkningar i en heteroresistent Escherichia coli-population avslöjad genom ultradjup långtidssekvensering
Dolda överlevnadspockets
När läkare behandlar bakterieinfektioner med antibiotika antar de att hela mikrobsvärmen reagerar på samma sätt. Men ibland motstår en mycket liten del av populationen i tysthet, överlever behandlingen och banar väg för behandlingsmisslyckande eller återfall. Denna studie avslöjar hur sådana sällsynta överlevare uppstår och förändras över tid i Escherichia coli, och introducerar ett kraftfullt sätt att följa dessa genetiska förändringar ända ner på cellnivå.
Små genetiska upprepningar, stora konsekvenser
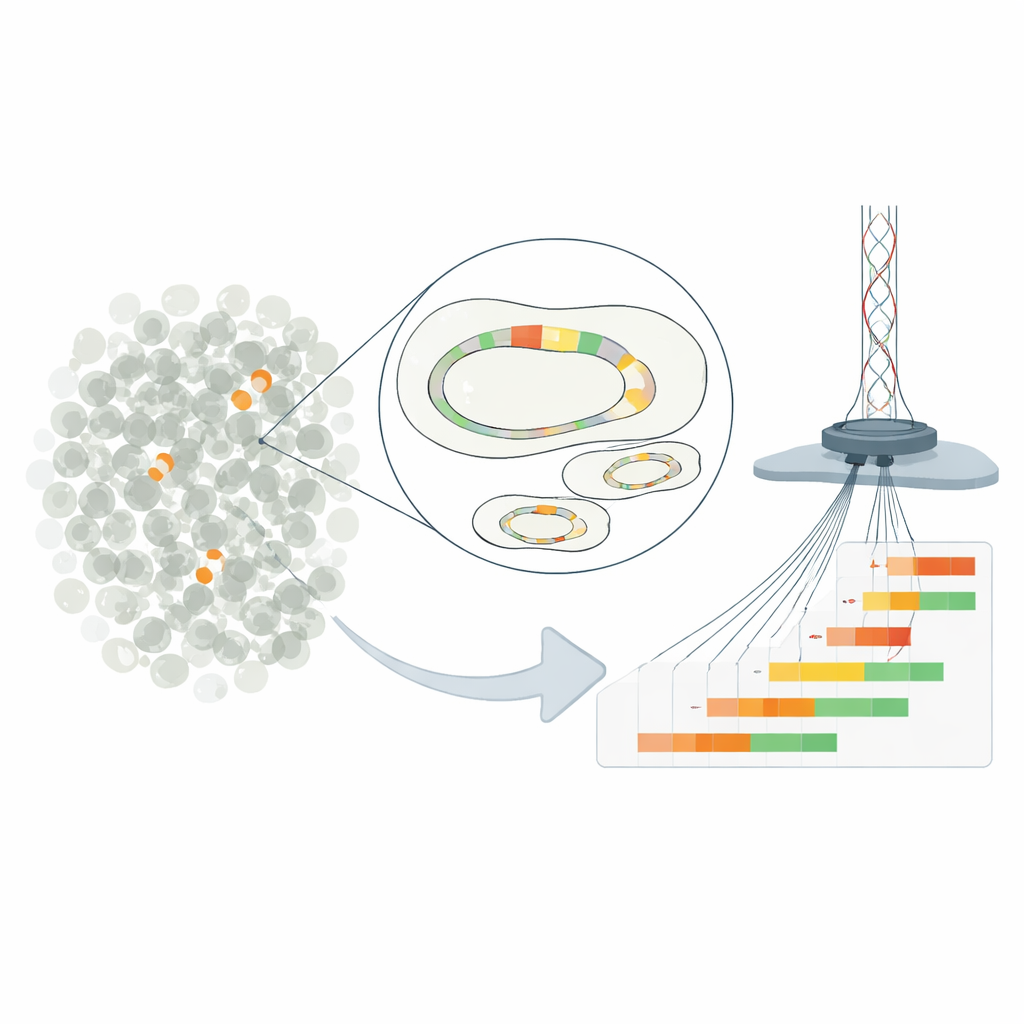
Arbetet fokuserar på "heteroresistens", ett tillstånd där de flesta bakterier i ett prov verkar känsliga för ett läkemedel, men en liten minoritet klarar betydligt högre doser. I den studerade E. coli-stammen beror detta beteende på upprepade kopior av en resistensgen som finns på en plasmid — en liten DNA-cirkel separat från kromosomen. Genom att duplicera ett kort DNA-avsnitt som innehåller en beta-laktamasgen kan bakterierna öka produktionen av ett enzym som bryter ned antibiotikat piperacillin-tazobactam. Ju fler upprepningar en cell bär, desto mer enzym produceras och desto bättre är chanserna att överleva i läkemedlets närvaro.
Avläsning av DNA-cirklar i enastående detalj
Traditionella metoder kan bara uppskatta det genomsnittliga antalet genkopior över en hel bakteriepopulation och döljer därmed den rika variationen mellan enskilda celler. För att komma runt detta konstruerade forskarna den kliniska plasmiden så att den kunde klippas på en bestämd plats och sedan isoleras från resten av genomet. De använde ultradjup Nanopore långläsningssekvensering för att läsa hela plasmidmolekyler från ände till ände och räkna exakt hur många upprepade resistensenheter varje plasmid innehöll. Denna metod nådde en upplösning ned till en cell på 100 000 och avslöjade plasmider med allt från noll till mer än ett dussin genkopior som samexisterade i samma kultur. Jämförelser med andra tekniker bekräftade att den nya metoden i genomsnitt rapporterade korrekta kopieringsantal.
Hur antibiotika omformar populationen
Med detta verktyg följde teamet vad som hände när de utsatte E. coli-kulturer för ökande doser av piperacillin-tazobactam och sedan tog bort läkemedlet. När antibiotikanivåerna steg skiftade den övergripande fördelningen mot plasmider med fler kopior av resistensgenen, men celler med färre kopior försvann aldrig helt. När läkemedlet drogs tillbaka och bakterierna odlades under hundratals generationer gled populationen bara gradvis tillbaka mot lägre kopieringsantal och återgick aldrig helt till utgångstillståndet. Separata tillväxttester visade att varje extra genkopia gav ett mätbart steg upp i läkemedelstolerans, vilket tätt kopplade de observerade genetiska fördelningarna till det synliga heteroresistensmönstret i standardlaboratorieanalyser.

Skydd från grannar och dolda kostnader
För att förklara varför celler med låg kopiaantal kvarstod även under stark behandling byggde författarna en matematisk modell som kombinerade bakterietillväxt, enzymatisk nedbrytning av antibiotika och slumpmässiga händelser som lägger till eller tar bort genkopior. Simulationerna visade att "indirekt resistens" spelar en viktig roll: mycket resistenta celler pumpar ut tillräckligt med beta-laktamas för att sänka läkemedelskoncentrationen i den delade omgivningen och därigenom ofrivilligt skydda mindre resistenta grannar. Så länge de extra genkopiorna endast medför en liten tillväxtkostnad när inget läkemedel är närvarande hjälper denna skyddande effekt till att upprätthålla ett brett spektrum av kopieringsantal och fördröjer återgången till en fullt känslig population. Modellen visade också hur vanlig anpassning till odlingsmediet — orelaterade mutationer som förbättrar tillväxt — kan låsa in specifika kopieringsnadsstater genom att göra vissa subpopulationer mer fit än andra.
Varför detta betyder något för patienter och vidare
För icke-experter är budskapet att en bakteriekultur inte är en enhetlig fiende: den är en ständigt föränderlig blandning av individer med olika förmåga att överleva antibiotika. Genom att direkt räkna genkopior på tusentals enskilda DNA-molekyler kopplar denna studie den dolda mångfalden till behandlingsrelevant resistens på ett kvantitativt sätt. Sådana insikter kan förbättra hur genomssekvensering används för att förutsäga svårupptäckt heteroresistens, hjälpa till att identifiera bakteriella stammar som är särskilt benägna att orsaka behandlingsmisslyckanden och vägleda bättre diagnostiska tester. Eftersom tandemförstärkningar av gener också driver snabb anpassning i virus, tumörer och andra organismer kan samma strategi anpassas långt utanför E. coli och erbjuda ett nytt fönster in i hur upprepade DNA-bitar hjälper livet att överlista hot.
Citering: Jonsson, S., Guliaev, A., Berryhill, B.A. et al. The dynamic distribution of genetic tandem amplifications in a heteroresistant Escherichia coli population revealed by ultra-deep long read sequencing. Nat Commun 17, 2113 (2026). https://doi.org/10.1038/s41467-026-70044-8
Nyckelord: antibiotikaheteroresistens, genförstärkning, Escherichia coli, långläsningssekvensering, beta-laktamas