Clear Sky Science · sv
Enstaka-molekylers dynamik avslöjar att ATP-bindning ensam driver substratomvandring av en ABC‑transportör
Varför små cellulära pumpar spelar roll
Varje cell i din kropp är beroende av mikroskopiska maskiner som förflyttar molekyler över membran och därigenom påverkar allt från näringsupptag till immunsvar. En huvudklass av dessa maskiner, kallade ABC‑transportörer, använder cellens kemiska bränsle ATP för att föra gods uppåt, mot dess naturliga gradient. Ändå har forskare under decennier diskuterat en grundläggande fråga: räcker det att ATP binder för att driva transportsteget, eller frigörs energin först när ATP bryts ner? Denna studie zoomar in på en enskild transportör, molekyl för molekyl, för att avgöra den debatten.
Att iaktta en transportör åt gången
I stället för att mäta den kombinerade beteendet hos miljontals molekyler byggde forskarna en uppställning som låter dem följa individuella transporthändelser i realtid. De fokuserade på TmrAB, en bakteriell kusin till den mänskliga TAP‑transportören som lastar immunpeptider för visning för mördarceller. TmrAB sitter i ett membran och för korta proteinfragment (peptider) från ena sidan till den andra med hjälp av ATP. För att se varje transportsteg fångade teamet en enskild TmrAB‑molekyl i en artificiell membranbubbla (en liposom) och placerade inuti bubblan en specialkonstruerad ”sensor”‑protein som ändrar sin fluorescens när det fångar en peptid. Med hjälp av ett högkänsligt mikroskop kunde de då se, som korta hopp i ljussignalen, de exakta ögonblicken när en peptid efter en annan anlände in i bubblan.
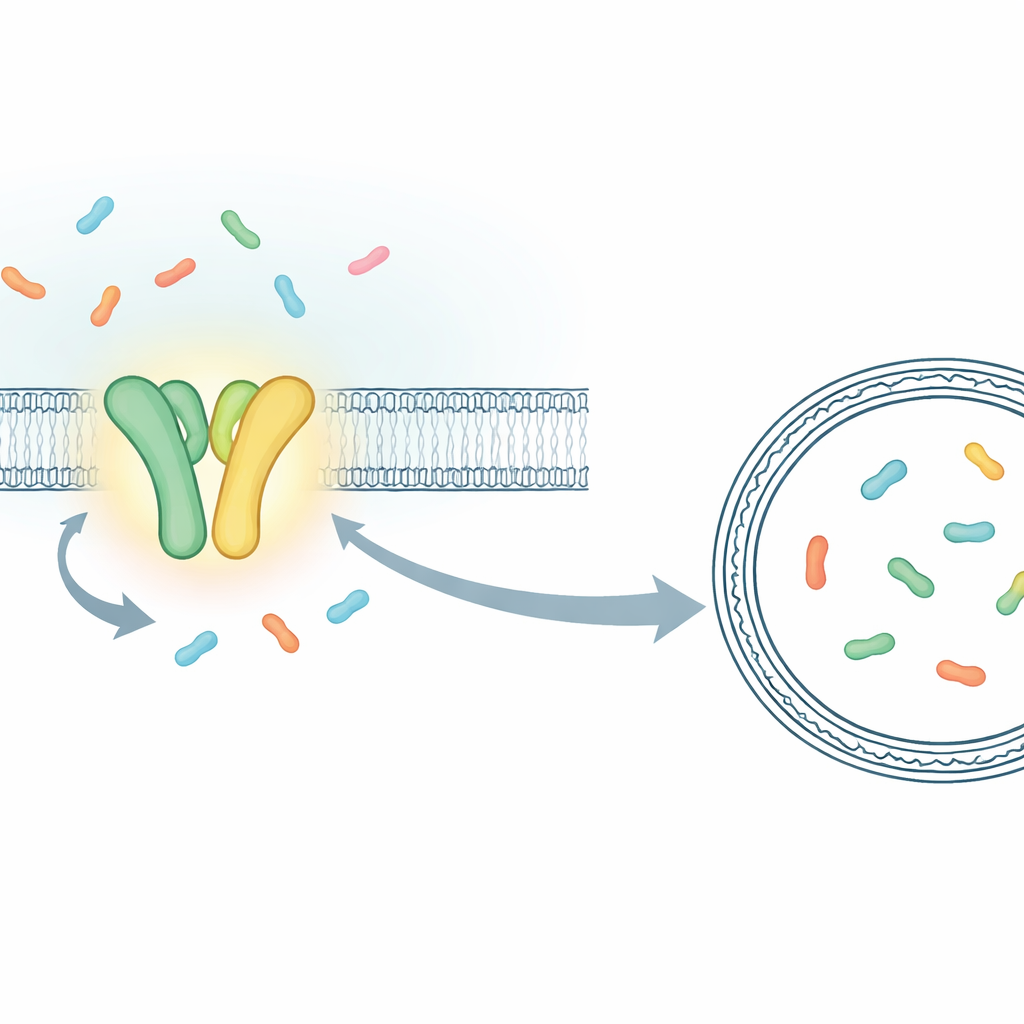
Bevisa att en ATP‑bindning flyttar en peptid
Med denna enstaka‑molekylsassay i hand jämförde forskarna normal TmrAB med en modifierad, långsamt snurrande variant vars cykler är utdragna i tiden. Den långsamma varianten gjorde det möjligt att urskilja individuella händelser som annars skulle smälta samman. De visade att när ATP och peptider var närvarande tillsammans skiftade sensorn inne i liposomen från sitt ”tomma” till sitt ”fyllda” tillstånd i diskreta steg, var och ett förenligt med att en enda peptid transporterades. Genom att analysera hur snabbt sensorn slöt sig kring peptiderna och uppskatta den lilla volymen inne i varje liposom kunde de till och med översätta dessa ljusförändringar till ungefärliga peptidkoncentrationer. Siffrorna stämde överens med vad man skulle förvänta om en, sedan två peptider ackumulerades i bubblor på omkring 100 nanometers diameter, vilket bekräftade att de nu räknade transporthändelser en efter en.
ATP‑bindning ensam vänder den molekylära strömbrytaren
Den centrala kontroversen rör magnesiumjoner (Mg2+), som normalt följer med ATP i celler och är kända för att krävas för effektiv ATP‑hydrolys. Vissa modeller föreslog att Mg2+ också kan behövas för att ATP ska binda eller för att transportören ska stängas. För att bena ut dessa roller tog forskarna bort Mg2+ med en kelateringsagent men tillförde fortfarande ATP. Under dessa förhållanden kunde både den normala och den långsamma transportören utföra exakt ett transportsteg per molekyl, men upphörde sedan. Det beteendet indikerar att ATP fortfarande kan binda och tvinga transportören att växla från en inåtvänd till en utåtvänd form och föra en peptid, även utan Mg2+. Utan Mg2+ kan transportören dock inte effektivt klyva ATP och kan därför inte återställa sig för en ny omgång.
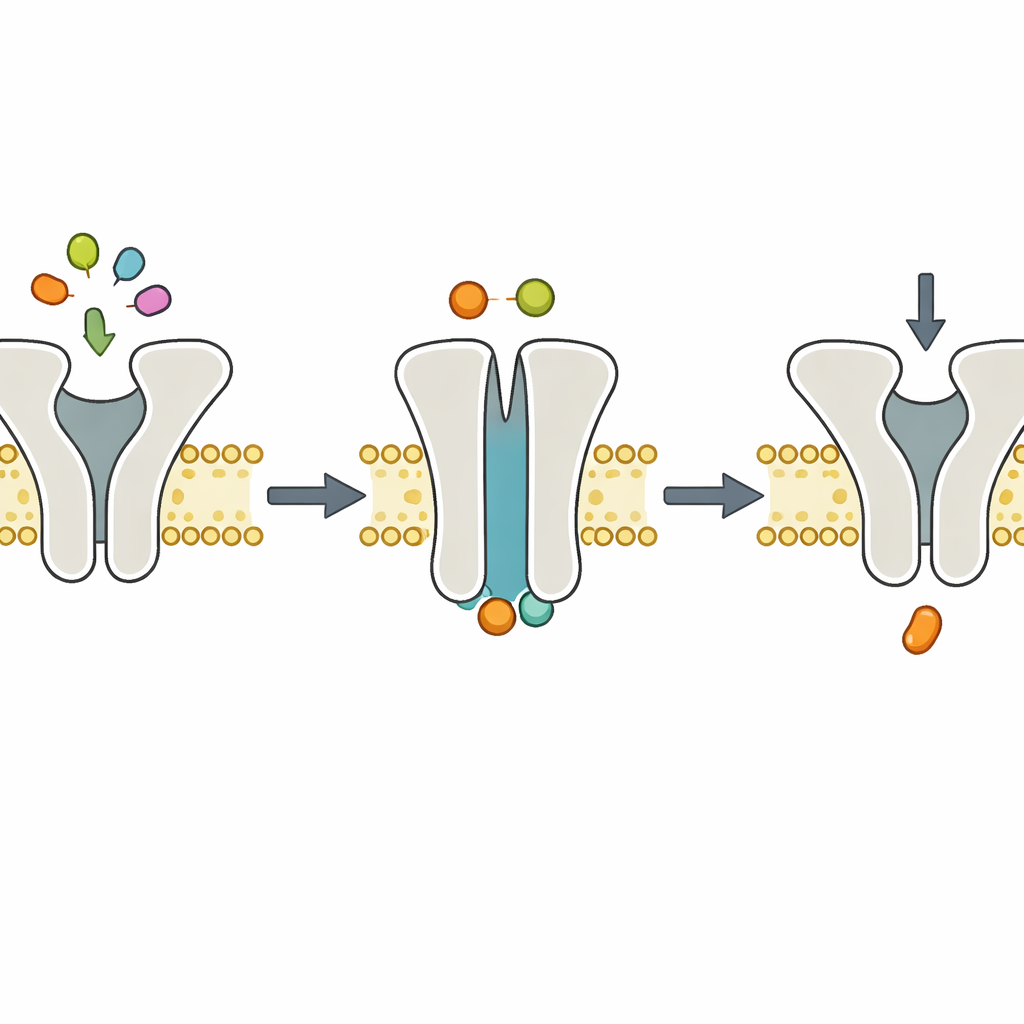
Strukturella ögonblicksbilder stöder dynamiken
För att se hur maskinen ser ut under detta Mg2+‑fria steg vände sig teamet till kryo‑elektronmikroskopi, som avbildar blixtfrusna molekyler med närapå atomär detalj. De rekonstituerade TmrAB i lipiddiskar, tillsatte ATP utan Mg2+ och frös komplexen. De resulterande strukturerna visade TmrAB i en utåtvänd, ”ockluderad” konformation med ATP kilat i båda sina inre bindningsfickor, men utan synligt Mg2+. Dessa ögonblicksbilder var i praktiken omöjliga att skilja från tidigare strukturer erhållna med ATP och Mg2+ närvarande. Tillsammans med biokemiska analyser som visar att ATP‑klyvning helt stannar av utan Mg2+ stödjer bilderna en enkel arbetsfördelning: ATP‑bindning driver konformationsbytet som flyttar peptiden, medan Mg2+‑beroende ATP‑hydrolys utför återställningssteget.
En tydligare bild av hur cellulära pumpar fungerar
Genom att iaktta enskilda transportörer och lösa deras strukturer besvarar detta arbete en längestående fråga om ABC‑transportörer: det mekaniska kraftslaget som för en peptid är utlösts av ATP‑bindning i sig, inte av den efterföljande kemiska nedbrytningen av ATP. Mg2+ går in i handlingen främst för att möjliggöra ATP‑klyvning, vilket i sin tur återställer transportören så att den kan arbeta igen. Utöver att klargöra en grundläggande del av cellbiologin erbjuder denna enstaka‑molekylsmetod en arbetsmodell för att dissekera andra membranmaskiner som ligger bakom immunitet, läkemedelsresistens och många sjukdomar — en molekyl och ett transportsteg i taget.
Citering: Nocker, C., Pečak, M., Nocker, T. et al. Single-molecule dynamics reveal ATP binding alone powers substrate translocation by an ABC transporter. Nat Commun 17, 3038 (2026). https://doi.org/10.1038/s41467-026-70021-1
Nyckelord: ABC‑transportörer, ATP‑bindning, single‑molecule FRET, membrantransport, TAP och TmrAB