Clear Sky Science · sv
Prussian blue-nanopartiklar som riktar in sig på flera PANoptosom-medierade PANoptoser för terapi av myokardiell ischemireperfusionsskada
Varför det är viktigt att skydda det läknande hjärtat
När en person får en hjärtinfarkt skyndar läkare för att öppna den blockerade artären och återställa blodflödet. Detta livräddande ingrepp har dock en dold kostnad: den plötsliga återföringen av syre kan i sig skada hjärtat, döda celler och bana väg för hjärtsvikt. Denna studie undersöker en uppfinningsrik nanomedicin som syftar till att skydda hjärtat under denna sårbara period genom att blockera flera sammanflätade celldöds‑vägar samtidigt, vilket potentiellt kan leda till mildare återhämtning efter hjärtinfarkt.
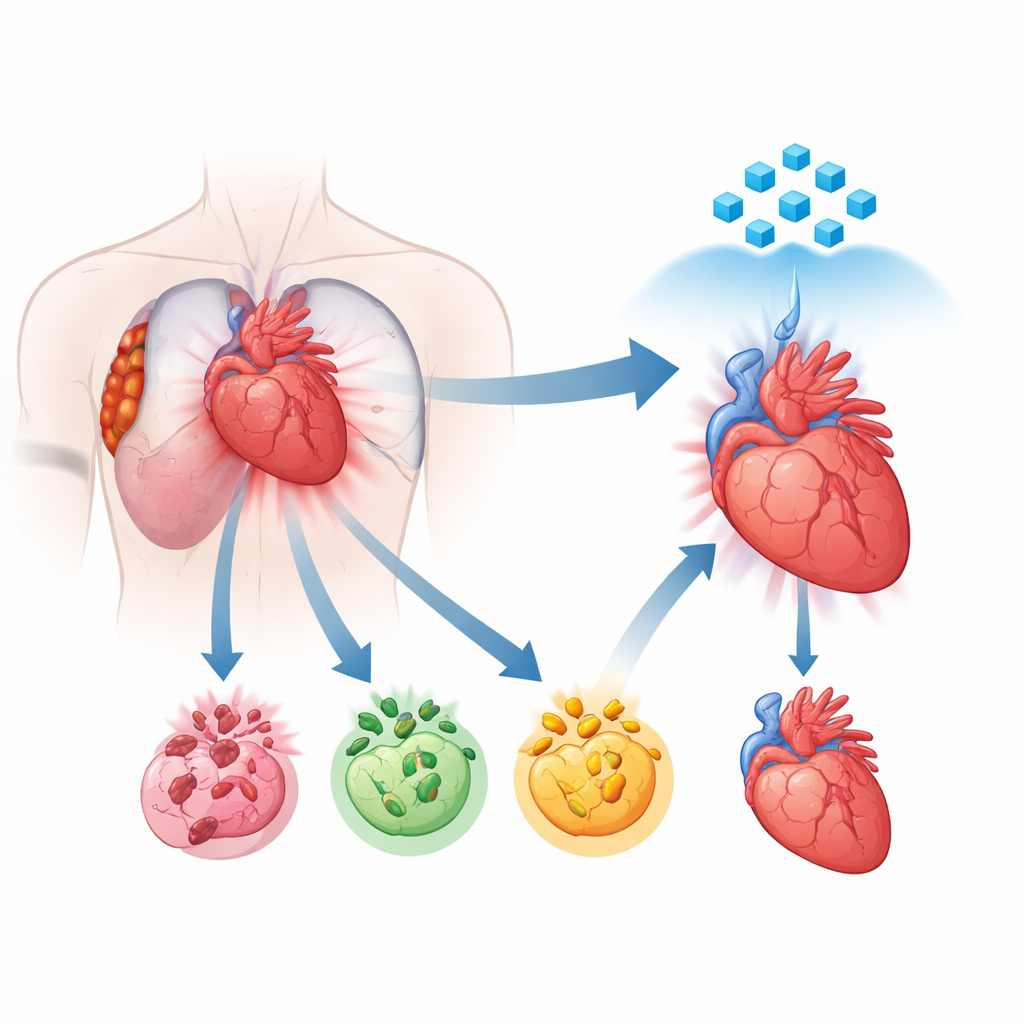
En ny syn på hur hjärtceller dör
I åratal har forskare vetat att skadade hjärtceller kan dö genom olika programmerade vägar, inklusive apoptos, nekroptos och pyroptos. Var och en följer sitt eget molekylära manus, men växande bevis visar att dessa vägar inte fungerar isolerat. Istället kommunicerar de med varandra och kan förenas i en kombinerad, okontrollerad process kallad PANoptos. I detta läge aktiveras flera dödsprogram samtidigt, vilket gör terapier som blockerar bara en väg frustrerande svaga. Författarna använde enkärnig RNA‑sekvensering av mänsklig hjärtvävnad från patienter med nyligen inträffade hjärtinfarkter för att kartlägga var och hur starkt dessa dödsprogram är påslagna. De fann att i de mest skadade regionerna visade hjärtmuskelceller en kraftig förskjutning mot detta kombinerade dödstillstånd, vilket pekar på PANoptos som en central drivkraft för skadan.
Att designa ett litet multiverktyg för det skadade hjärtat
För att tackla en så komplex process vände sig teamet till Prussian blue, en länge godkänd medicinsk förening mest känd som ett motgift mot vissa metallförgiftningar. I nanoskala beter sig Prussian blue‑partiklar som små katalytiska robotar som kan släcka skadliga molekyler och påverka cellbeteende. Genom datorsimuleringar visade forskarna att dessa nanopartiklar direkt kan fästa vid tre nyckelprotein‑nav — RIPK1, ZBP1 och AIM2 — som hjälper till att montera det molekylära maskineriet för PANoptos. Genom att binda till dessa nav på olika sätt förutspåddes partiklarna störa konstruktionen av de dödsframkallande komplexen som samordnar de tre celldöds‑vägarna.
Vägledning av nanopartiklar direkt till skadad hjärtvävnad
Nanopartiklar fungerar bara om de når rätt plats, så teamet klädde Prussian blue‑partiklar i naturliga membran avlägsnade från trombocyter, de blodceller som söker sig till skadade blodkärl. Denna beläggning skapade PB@PM, en biomimetisk bärare som cirkulerar som en trombocyt men levererar en terapeutisk last. I möss som utsattes för en kontrollerad hjärtinfarkt och återöppning av artären visade avbildning att PB@PM ackumulerades avsevärt mer i den skadade hjärtregionen än obelagda partiklar, samtidigt som de i stor utsträckning undvek friska organ. Viktigt är att de belagda partiklarna tolererades väl: blodprover och vävnadsundersökningar visade ingen uppenbar toxicitet, vilket stöder deras potential för vidare utveckling.
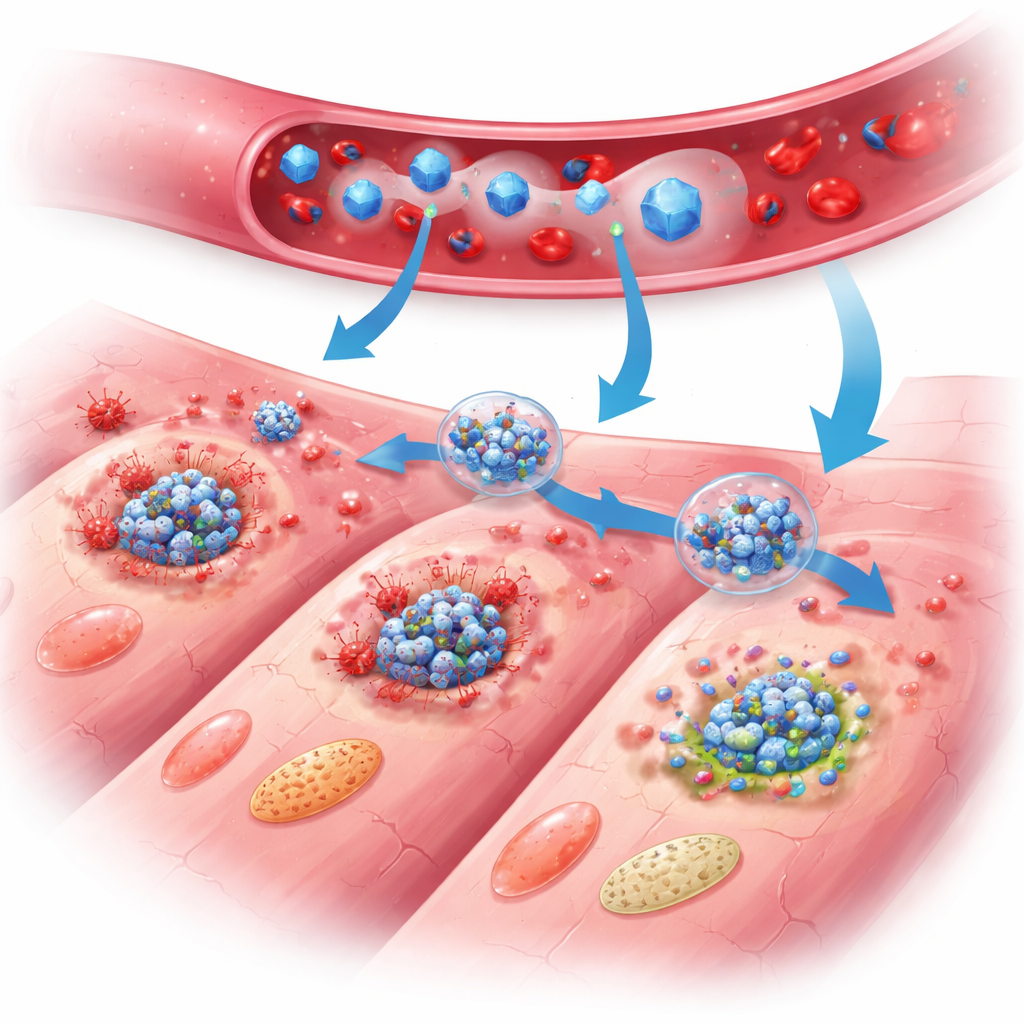
Hur nano‑skölden skyddar hjärtat
I behandlade möss blev fördelarna med PB@PM tydliga över dagar och veckor. Hjärtats pumpfunktion förbättrades, ärrstorleken minskade och hjärtväggen tunnades ut i mindre grad jämfört med obehandlade djur. Detaljerade vävnadsstudier avslöjade färre döende hjärtceller, lugnare inflammatoriska celler och bättre strukturerad reparationsvävnad med friskare blodkärlstillväxt och mindre onormal förstoring av överlevande celler. På molekylär nivå visade bred genuttrycksprofilering och proteinmätningar att PB@PM dämpade de tre stora programmerade dödsvägarna samtidigt, störde sammankopplingen av de multiprotein PANoptos‑komplexen och minskade nivåerna av signalmolekyler som driver inflammation. Partiklarna rensade också skadliga reaktiva syrearter, stabiliserade mitokondrier — cellens kraftverk — och återställde en mer normal energimetabolism, vilket avlägsnade viktiga triggers som annars skulle driva celler mot självförstörelse.
Vad detta kan innebära för framtida vård vid hjärtinfarkt
Enkelt uttryckt visar detta arbete att en smart designad nanopartikel kan fungera som en mångsidig sköld för hjärtat, dämpa en trasslig väv av destruktiva dödssignaler istället för att jaga en väg i taget. Genom att rikta in sig på skadad hjärtvävnad, binda centrala kontrollproteiner och mildra oxidativ och inflammatorisk stress minskade PB@PM kraftigt kedjereaktionen av cellförlust och ärrbildning som ofta följer på återöppningen av en blockerad artär. Även om omfattande tester återstår innan denna strategi kan nå patienter, erbjuder studien ett konceptbevis för att rikta in sig på PANoptos som helhet — och göra det med smarta, biologiskt inspirerade partiklar — kan öppna ett nytt kapitel i att skydda hjärtat efter en hjärtinfarkt.
Citering: Xu, L., Jiang, L., Wu, R. et al. Prussian blue nanoparticles targeting multiple PANoptosome-mediated PANoptosis for myocardial ischemia-reperfusion injury therapy. Nat Commun 17, 2329 (2026). https://doi.org/10.1038/s41467-026-70012-2
Nyckelord: myokardiell ischemireperfusion, nanopartikelterapi, programmerad celldöd, hjärtinflammation, mitokondrieskydd