Clear Sky Science · sv
RPA stimulerar direkt Mer3‑helikasens processivitet för att säkerställa normal överkorsbildning i meios
Hur celler blandar DNA för att skapa friska ägg och spermier
Varje gång en växt, ett djur eller en människa bildar ägg eller spermier måste cellerna omfördela kromosomer så att varje avkomma får en ny blandning av föräldradna DNA. Denna genetiska omfördelning bygger på noggrant placerade DNA‑utbyten, eller överkorsningar, mellan kromosompar. Den aktuella studien avslöjar hur två nyckelproteiner, Mer3 och RPA, samarbetar som en mikroskopisk maskin för att säkerställa att dessa överkorsningar bildas effektivt och säkert — en process som har betydelse för fertilitet, evolution och möjligen även cancer.
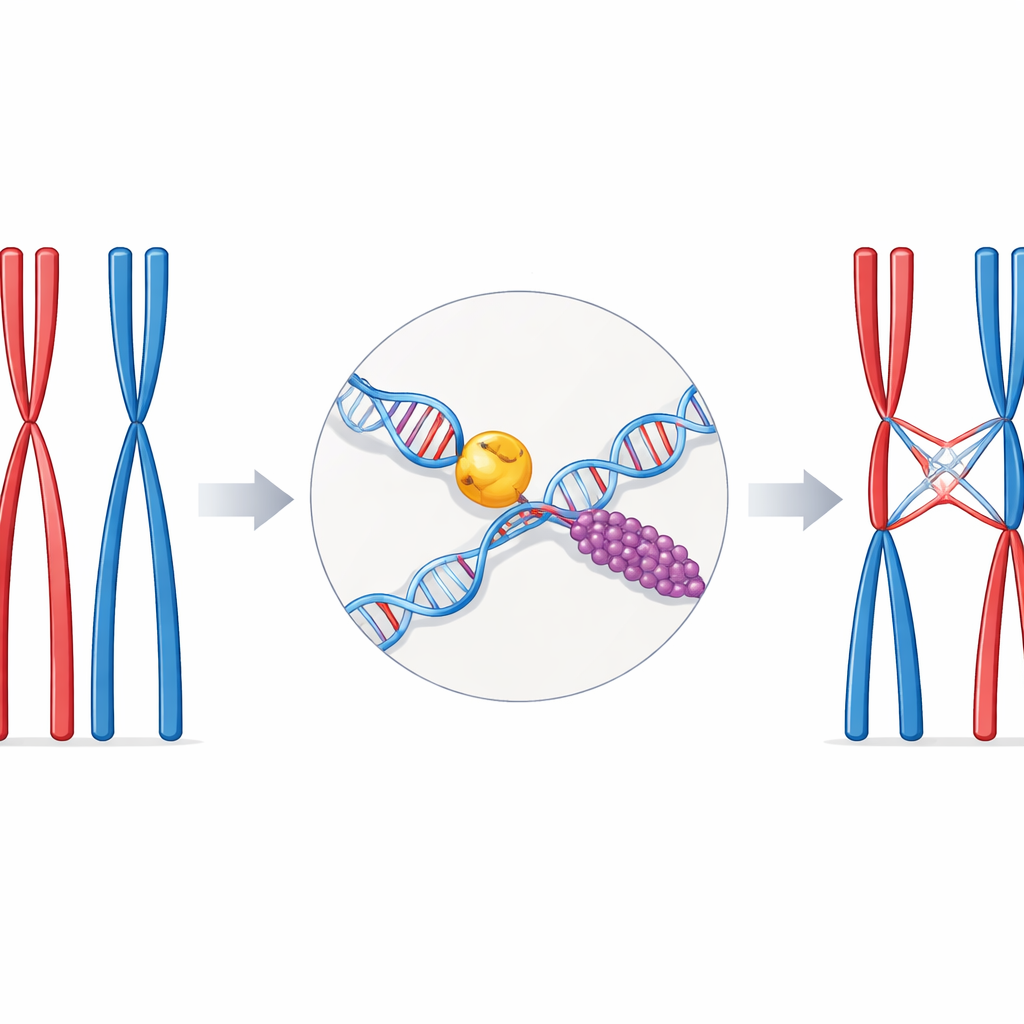
En känslig balansakt i könlig fortplantning
Under den särskilda celldelningen som kallas meios kommer kromosomerna i matchande par, en från varje förälder. För att dessa par ska separera korrekt måste de vara fysiskt länkade på några väl utvalda platser längs sin längd. Dessa länkar är överkorsningarna — sektioner där DNA‑strängar från en kromosom byts mot dem från dess partner. För få överkorsningar ökar risken för felaktig kromosomfördelning och infertilitet; för många eller felplacerade överkorsningar kan skada genomet. Cellerna förlitar sig därför på specialiserade reparationsvägar och hjälpproteiner för att omvandla ett farligt DNA‑brott till en kontrollerad överkorsning.
Möt Mer3 och RPA, ett DNA‑upprullningsteam
Forskarna fokuserade på Mer3, en molekylär motor som upplindar DNA och främjar överkorsningsbildning. Den mänskliga motsvarigheten, HFM1, är känd för att vara viktig för fertiliteten. De upptäckte att Mer3 binder direkt till RPA, ett proteinkomplex som normalt täcker exponerat enkelsträngat DNA för att skydda det och rekrytera andra reparationsfaktorer. Genom biokemiska tester, strukturell modellering och interaktionsanalyser kartlade gruppen en specifik dockningsplats där en kort svans på Mer3 passar in i en fåra på en RPA‑subenhet. Detta gränssnitt är bevarat från jäst till däggdjur, vilket tyder på att det är en långvarig lösning som evolutionen återanvänt för att kontrollera DNA‑reparation under meios.
Att se en enskild DNA‑motor i arbete
För att se vad detta partnerskap faktiskt gör använde forskarna enskilda‑molekyl magnettångar — ett instrument som håller en enskild DNA‑hårslinga som en liten fjäder och mäter hur en enda Mer3‑molekyl upplindar den över tid. De fann att Mer3 rör sig längs DNA med jämn hastighet även på egen hand. Men under förhållanden som efterliknar den relativt låga fysiska spänningen inne i celler tenderar Mer3 att släppa DNA efter att ha upplindat endast en kort sträcka. När en liten mängd RPA finns närvarande blir Mer3 plötsligt mycket mer uthållig: den kan upplinda mycket längre DNA‑sträckor utan att lossna, särskilt när DNA är benäget att vika tillbaka på sig själv. En muterad version av Mer3, konstruerad för att störa RPA‑bindande svansen, lyckas inte få denna ökade kvarhållningsförmåga, vilket visar att direktkontakt med RPA är vad som ökar Mer3:s processivitet.
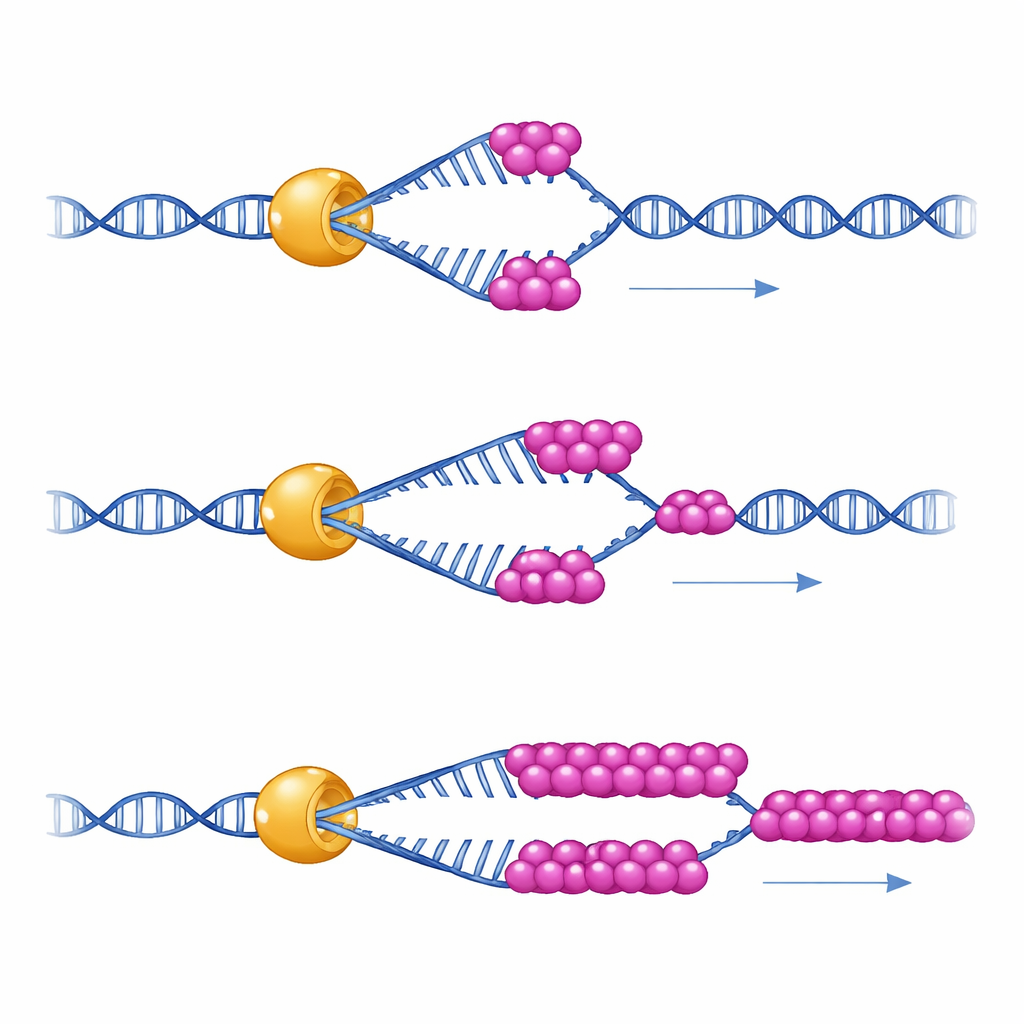
Konsekvenser för överkorsningar i levande celler
Gruppen frågade sedan vad som händer i faktiska jästceller när Mer3 inte kan greppa RPA ordentligt. De ersatte den normala MER3‑genen med den RPA‑bindande mutanten och övervakade meiosen. Dessa celler kunde fortfarande dela sig och bilda sporer, men deras fertilitet sjönk och det totala antalet överkorsningar längs vissa kromosomregioner minskade. Detaljerade DNA‑analyser visade fler reparationshändelser som slutade som icke‑överkorsningar och en ansamling av olösta rekombinationsintermediärer. Genom att kartlägga Mer3:s plats över hela genomet visade det sig att den mutanta proteinet rekryterades mindre stabilt till platser där programmerade DNA‑brott uppstår, även om dess tidiga association med kromosomaxlarna såg normal ut. Med andra ord, utan stark RPA‑bindning stannar Mer3 inte tillräckligt länge vid brottplatserna för att pålitligt driva dem mot överkorsningsutfall.
Vad detta betyder för fertilitet och genomstabilitet
Sammantaget visar studien att RPA gör mer än att bara täcka löst DNA; den finjusterar direkt beteendet hos en viktig meioshelikas. Genom att docka på RPA blir Mer3 en mer beslutsam DNA‑upprullare, kapabel att utöka och stabilisera de gemensamma DNA‑strukturer som mognar till överkorsningar. När denna interaktion försvagas växlar cellerna mot säkrare men mindre användbara reparationsutfall och lämnar fler intermediärer olösta, vilket subtilt underminerar kromosomfördelningen. Eftersom samma molekylära aktörer finns hos människor — och mutationer i HFM1 kopplats till infertilitet — ger detta arbete en molekylär förklaring till hur små förändringar vid ett proteingränssnitt kan sprida sig och påverka reproduktiv hälsa och genetisk mångfald i framtida generationer.
Citering: Altmannova, V., Orlić, L., Carrasco, C. et al. RPA directly stimulates Mer3 helicase processivity to ensure normal crossover formation in meiosis. Nat Commun 17, 2621 (2026). https://doi.org/10.1038/s41467-026-69985-x
Nyckelord: meios, genetisk rekombination, DNA‑helikas, fertilitet, kromosomövergång