Clear Sky Science · sv
Störning av DNA‑skadereaktionen av fosforotiolat antisensoligonukleotider
När hjälpsamma genbehandlingar lurar cellens reparationspersonal
Antisensoligonukleotider, eller ASO:er, är en växande klass av precisionsläkemedel utformade för att slå av eller på enskilda gener. De används redan för att behandla vissa sällsynta genetiska sjukdomar och testas för många fler tillstånd. Denna studie avslöjar en oväntad nackdel med en vanlig kemisk modifiering som gör dessa läkemedel mer stabila: under vissa förhållanden kan den få cellen att tro att dess DNA är skadat, störa reparationsmaskineriet och äventyra genomet på lång sikt.
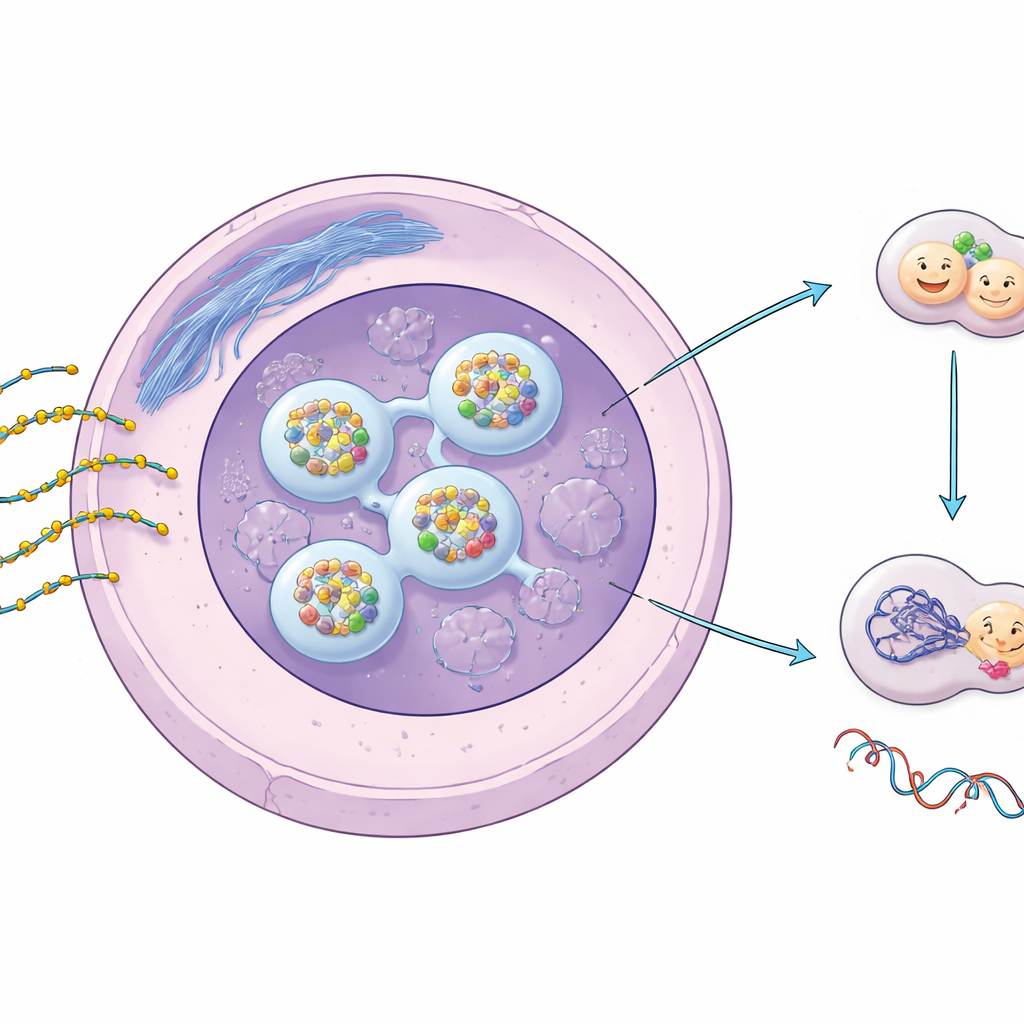
Designade genomkopplare och deras kemiska uppgradering
ASO:er är korta, enkelsträngade nukleinsyrafragment byggda för att känna igen och binda specifiska RNA‑budskap i våra celler, och därigenom tysta eller ändra dem. För att överleva i kroppen och ta sig in i celler effektivt bär de flesta terapeutiska ASO:er en fosforotiolat (PS)‑modifiering, där en svavelatom ersätter en syreatom i ryggraden av kedjan. Denna lilla förändring ökar dramatiskt deras stabilitet och deras benägenhet att interagera med proteiner. Tidigare arbete visade att PS‑ASO:er samlas i distinkta fläckar i cellkärnan och kan stressa vissa nukleära strukturer, men vad detta innebär för DNA‑reparation och långsiktig säkerhet har varit oklart.
Artificiella droppar som liknar verkliga reparationsplatser
Författarna följde fluorescensmärkta PS‑ASO:er i humana celler och fann att de vid vanliga experimentella doser snabbt ackumuleras i kärnan och bildar nya sfäriska strukturer kallade PS‑kroppar. Dessa kroppar bildas i en koncentrationsberoende takt och beter sig som vätskedroppar som fusionerar, löser upp sig och är beroende av svaga molekylära krafter—kännetecken för vätske–vätske‑fasseparation. Avgörande är att de inte befinner sig där faktiska DNA‑brott uppstår och inte innehåller de vanliga markörerna för brutet DNA. Istället visar studien att nyckelenzym för DNA‑reparation—inklusive DNA‑PKcs, ATM, ATR och PARP1—binder direkt till PS‑ASO:erna och blir starkt förhöjda inne i dessa artificiella droppar, trots att det underliggande DNA:t är intakt.
Falska larm som aktiverar cellens skadesignaler
När dropparna väl bildats gör ASO‑initierade strukturer mer än att passivt fånga upp proteiner: de slår på reparationsenzymerna. Inom en timme efter ASO‑inträde aktiveras enzymerna i dessa droppar och börjar modifiera närliggande kromatin, prydda histonproteiner med kemiska markörer som normalt ses efter äkta DNA‑skada. Detta utlöser hela DNA‑skaderesponsen—ytterligare reparationsfaktorer rekryteras, kontrollpunktsignalering slås på och aktiviteten hos cellcykelns motorer, CDK:er, dämpas. Som ett resultat bromsar eller stoppar celler sin progression genom viktiga faser av cellcykeln, särskilt vid punkten där de normalt kontrollerar att deras DNA är intakt innan delning. I möss hjärnor som exponerats för kliniskt relevanta ASO‑leveranser observerade forskarna även ökad DNA‑skadesignalering i regioner med högre ASO‑upptag, vilket indikerar att dessa effekter inte är begränsade till cellodlingar.
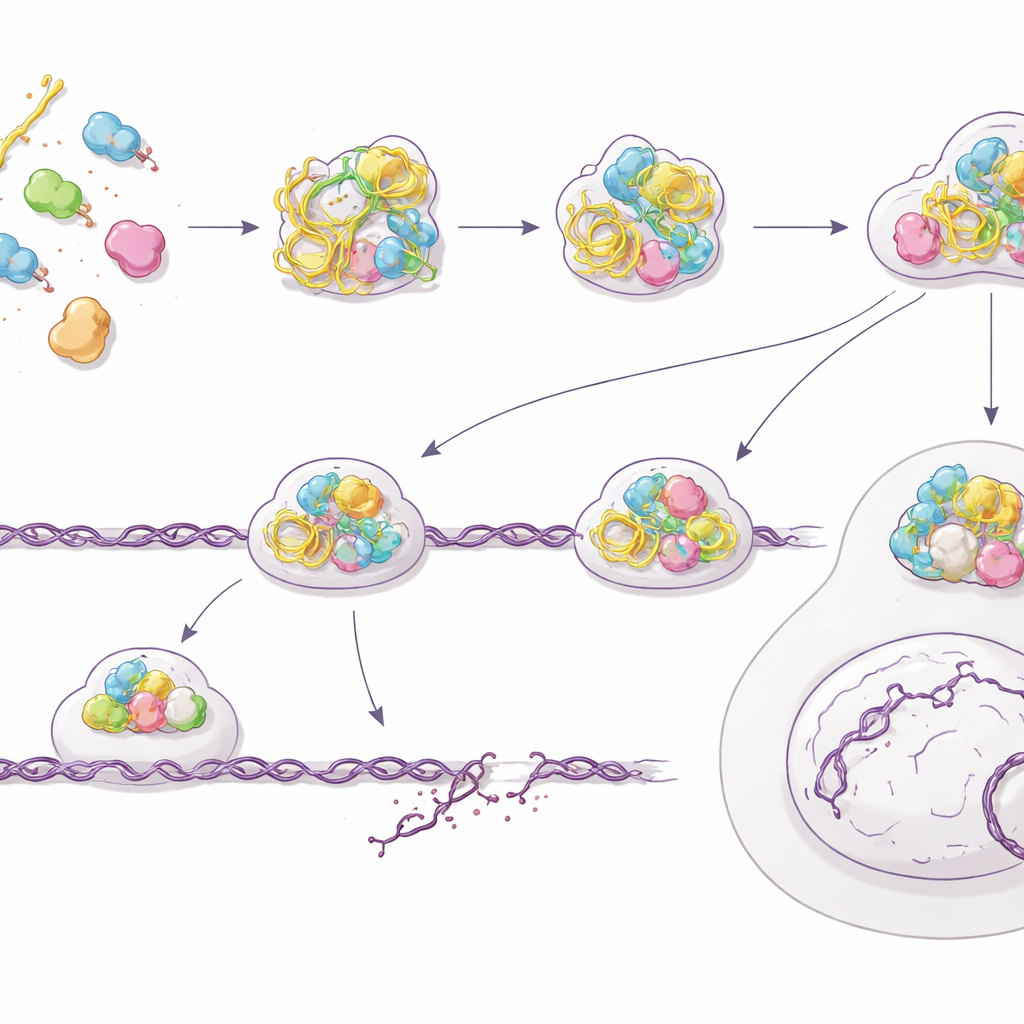
Reparation som går fel och en växande last av DNA‑brott
Paradoxalt nog, medan cellens larmsystem ljuder, försämras dess faktiska förmåga att reparera farliga DNA‑brott. Gruppen visade att celler förbehandlade med PS‑ASO:er har svårt att rensa skador efter bestrålning och till och med ackumulerar fler spontana brott, mätt med komet‑assay och persistenta reparationsfoci. En närmare granskning av en av cellens mest precisa reparationsvägar—homolog rekombination—avslöjade problemet: nyckelproteiner som BRCA2 och RAD51 misslyckas med att samlas korrekt vid brutna DNA‑ändar, medan tidigare markörer för bearbetning vid dessa ändar fortfarande syns. Med ett genetiskt rapportörsystem kvantifierade författarna en ungefärlig 60% minskning i effektivitet för homolog rekombination efter PS‑ASO‑exponering. Celler blir överlag mindre livskraftiga och avsevärt mer känsliga för strålning, vilket stämmer överens med ett reparationssystem som signaleras men inte korrekt sätts in.
Vad detta betyder för framtiden för genriktade läkemedel
Sammantaget tyder studien på att PS‑modifierade ASO:er kan nukleera artificiella vätskedroppar i kärnan som koncentrerar och aktiverar DNA‑reparationsenzymer även när det inte finns någon skada att åtgärda. Detta kroniska falsklarm stör normalt reparationsval, särskilt den korrekta homolog rekombinationen, vilket leder till bestående DNA‑lesioner, kontrollpunktaktivering och celldöd. Även om de starkaste effekterna ses vid höga nukleära ASO‑nivåer typiska för transfektionsexperiment, är subtil aktivering av skadesignalering detekterbar även vid lägre, läkemedelslika doser. För patienter och läkemedelsutvecklare är budskapet tydligt: de kemiska egenskaper som gör ASO:er till effektiva läkemedel kan i vissa sammanhang störa cellens mest fundamentala skydd—förmågan att bibehålla ett stabilt genom—vilket understryker behovet av att designa säkrare ryggrader och att övervaka DNA‑reparationsvägar under behandling.
Citering: Hjelmgren, L., Zhou, Q., Schmidli, S. et al. Dysregulation of the DNA damage response by phosphorothioate antisense oligonucleotides. Nat Commun 17, 2111 (2026). https://doi.org/10.1038/s41467-026-69980-2
Nyckelord: antisensoligonukleotider, DNA‑skadereaktion, vätske‑fasseparation, homolog rekombination, genomstabilitet