Clear Sky Science · sv
Kirala peptidoglykan‑mimikry riktar in sig på bakteriell väggbiosyntes för patogenintervention
Ett nytt sätt att jaga skadliga mikrober
Infektioner som är resistenta mot antibiotika ökar runt om i världen, samtidigt som kliniker saknar verktyg som exakt kan upptäcka och angripa farliga bakterier utan att skada våra egna celler. Denna studie presenterar en smart molekylär ”lockbete” som imiterar en viktig byggsten i bakteriens cellvägg. Dessa designade molekyler kan både belysa infektioner för avbildning och föra antibiotika direkt till mikroberna, vilket erbjuder en ny strategi för att bekämpa svårbehandlade patogener.
Att efterlikna det bakteriella pansaret
Bakterier är omslutna av ett robust nätverk kallat cellväggen, uppbyggt av sockerarter och ovanliga spegelvända aminosyror som våra egna celler i stort sett inte använder. Forskarna utnyttjade denna skillnad genom att skapa långa sockerkedjor dekorerade med en specifik spegelvänd form av alanin, en vanlig aminosyra. Dessa kedjor, kallade kirala peptidoglykan‑mimikry, är designade för att starkt likna de naturliga byggstenar bakterier använder för att bygga sina väggar, men saknas i däggdjursvävnad. Genom att finjustera hur mycket av denna D‑form av alanin som fästes producerade teamet varianter som tydligt föredrog bakterier framför humana celler.
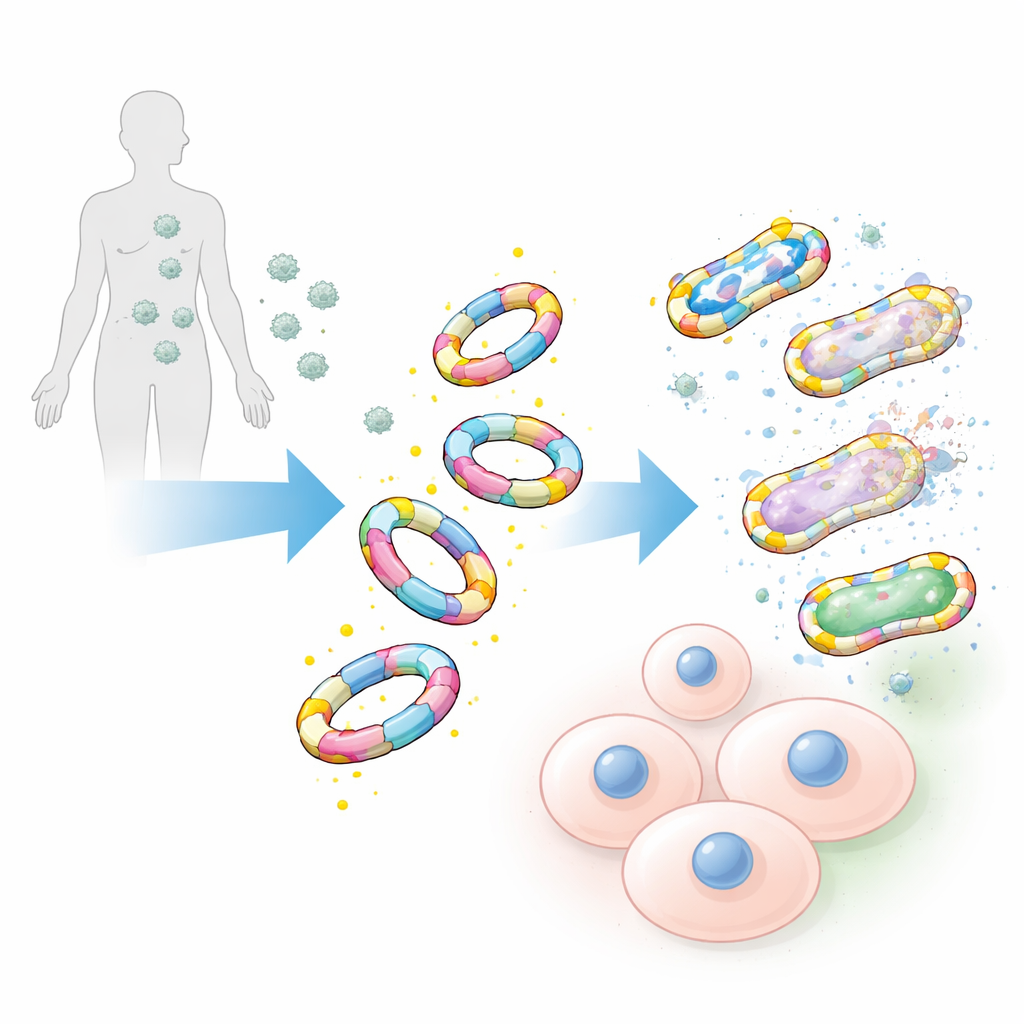
Fäster vid bakterier, inte våra celler
När de testades mot ett brett spektrum patogener, inklusive ökända hospitalsstammar som meticillinresistent Staphylococcus aureus och andra ESKAPE‑bakterier, band de D‑alanin‑dekorerade mimikerna till bakterieytor med slående effektivitet. Deras spegelvända motsvarigheter byggda av L‑alanin, liksom de ursprungliga sockerkedjorna ensamma, visade endast svag eller försumbar bindning. Teamet jämförde också dessa stora mimiker med traditionella små kemiska prober baserade på enstaka D‑alaninmolekyler. Även när de små proberna gjordes extremt ljusstarka märkta de fortfarande långt färre bakterier och gav svagare signaler, vilket understryker styrkan i den större, mer livlika designen.
Kapning av cellväggens monteringslinje
För att förstå hur igenkänningen blir så stark undersökte forskarna hur mimikerna interagerar med den bakteriella maskineriet för väggbyggnad. De fann att D‑alanin‑baserade kedjor inte bara fäster på utsidan; de tas upp som om de vore äkta byggstenar och matas in i samma enzymatiska steg som normalt fogar samman cellväggskomponenter. Kemisk analys upptäckte nya intermediära molekyler som uppstår endast när dessa mimiker är närvarande, och datorbaserade simuleringar visade att nyckel‑enzymerna för väggbyggnad greppar mimikerna ännu hårdare än de naturliga substraten. Över flera tillväxtrundor ackumulerades mimikerna i väggen, vilket gradvis förvrängde dess struktur och gjorde den läckande.
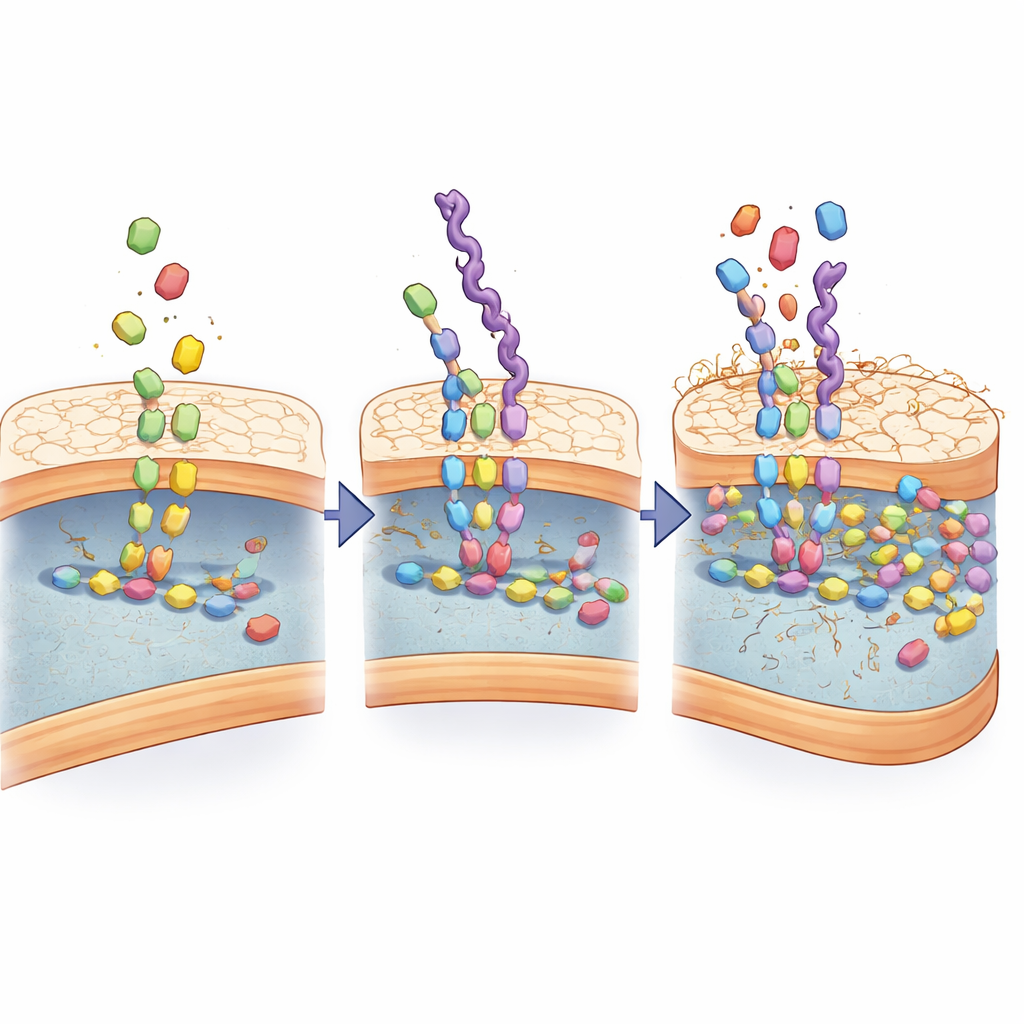
Gör mimiker till smarta läkemedelsbärare
Eftersom dessa kedjor naturligt samlas i små partiklar i vatten och bär många kemiska fästpunkter använde teamet dem som skelett för avbildningsfärgämnen och antibiotika. Fluorescerande varianter tydliggjorde bakterier i cellkulturer, samtidigt som de knappt interagerade med däggdjursceller odlade sida vid sida. Forskarna lastade sedan in antibiotikumet tetracyklin i mimik‑baserade partiklar. I laboratorietester gjorde denna förpackning tetracyklin flera gånger mer effektivt och dödade även resistenta stammar vid betydligt lägre doser än det fria läkemedlet. Mikroskopi visade att antibiotikalastade mimiker samlades tätt på bakterierna, trängde in i deras höljen och utlöste omfattande celldöd jämfört med otargeterade formuleringar.
Bekämpa infektioner i kroppen
De mest krävande testerna genomfördes i musmodeller av lokala hudsår och livshotande bukinfektioner. I infekterade sår sökte de fluorescerande mimikerna upp bakterier djupt i vävnaden och när de bar tetracyklin rensade de nästan fullständigt bort mikroberna. Detta ledde till snabbare sårläkning, tjockare ny hud, mer ordnad kollagenavsättning och rikare tillväxt av små blodkärl. I modeller för systemiska infektioner ackumulerades mimikerna specifikt i infekterade organ såsom mjälten och lungorna, där de kraftigt reducerade bakteriemängder när de var lastade med antibiotikum. Viktigt är att höga doser av mimikerna ensamma visade god säkerhet, utan tydliga skador på större organ eller blodkemiska parametrar.
Vad detta kan innebära för framtida behandlingar
Genom att bygga en nära kemisk liknelse av bakteriens egna byggstenar visar detta arbete ett nytt sätt att ”smälta in” i en patogens metabolism i stället för att enbart angripa utifrån. Dessa kirala mimiker fungerar både som högprecisionssignaler för avbildning och som smarta fordon som styr antibiotika direkt till sina mikrobiella mål, inklusive resistenta stammar, samtidigt som däggdjursceller skonas. Om de kan översättas till kliniska verktyg kan sådana biomimetiska plattformar hjälpa läkare att exakt se var infektioner döljer sig och behandla dem mer effektivt med lägre läkemedelsdoser, vilket erbjuder ett lovande vapen mot den växande utmaningen med antimikrobiell resistens.
Citering: Deng, K., Zou, D., Zeng, Z. et al. Chiral peptidoglycan mimics target bacterial wall biosynthesis for pathogen intervention. Nat Commun 17, 3258 (2026). https://doi.org/10.1038/s41467-026-69967-z
Nyckelord: antibiotikaresistens, bakteriers cellvägg, riktad läkemedelsleverans, molekylär avbildning, nanomedicin