Clear Sky Science · sv
Omarbetning av gener mellan arter med hjälp av ortologinformation och generativ modellering
Varför det spelar roll att omarbeta gener mellan arter
Modern bioteknik behöver ofta flytta gener från en mikroorganism till en annan för att framställa läkemedel, enzymer eller verktyg för miljörengöring. Men en gen som fungerar väl i sin ursprungliga mikroorganism kan släpa i en ny värd och ge låg proteinproduktion. Denna artikel presenterar ett nytt artificiellt intelligenssystem, OrthologTransformer, som lär sig av evolutionen själv för att skriva om gener så att de känns ”inhemska” i en annan art, vilket ökar deras prestanda och öppnar nya möjligheter för grön teknologi och industri.
Begränsningar i dagens genjusteringsknep
I årtionden har forskare förlitat sig på en strategi som kallas kodonoptimering för att hjälpa främmande gener att fungera i nya värdar. Idén är enkel: den genetiska koden har flera trebokstavskodon som kan koda samma aminosyra, och olika arter föredrar olika kodon. Traditionella verktyg byter ut sällsynta kodon mot föredragna utan att ändra proteinets aminosyrasekvens. Det hjälper ofta, men förbiser många andra egenskaper som påverkar genens funktion, såsom RNA-folning, regulatoriska signaler och tajmning i proteinproduktion. I vissa fall kan överoptimering av kodon till och med skada proteinavkastningen. Samtidigt löser naturen artövergripande anpassning på ett rikare sätt: besläktade gener i olika arter, så kallade ortologer, visar ofta aminosyraförändringar och små insättningar eller deletioner utöver kodonbyten, samtidigt som funktionen bevaras.
Lära sig naturens handbok för gengenomskrivning
OrthologTransformer behandlar generedesign som en form av språköversättning: givet en DNA-sekvens från en bakterie så ”översätter” den hur den genen sannolikt skulle se ut i en annan art. Modellen bygger på Transformer-arkitekturen som används i moderna språkinstrument, men här arbetar den på kodonnivå istället för ord. Den tränas på miljontals naturligt parade ortologa gener från över tvåtusen bakteriella arter, med specialtoken som anger vilken art den konverteras från och till. Genom att se hur evolutionen redan har balanserat funktion och värdsanpassning lär sig systemet när enkla kodonbyten räcker och när subtila aminosyraförändringar eller längdanpassningar tolereras. I tester som omfattade 45 bakteriearter och hundratals källa–mål-kombinationer liknade de AI-omdesignade generna målartens inhemska ortologer mer än både konventionell kodonoptimering och en ledande neuralt baserad kodonoptimerare, samtidigt som hög likhet på proteinnivå bibehölls. 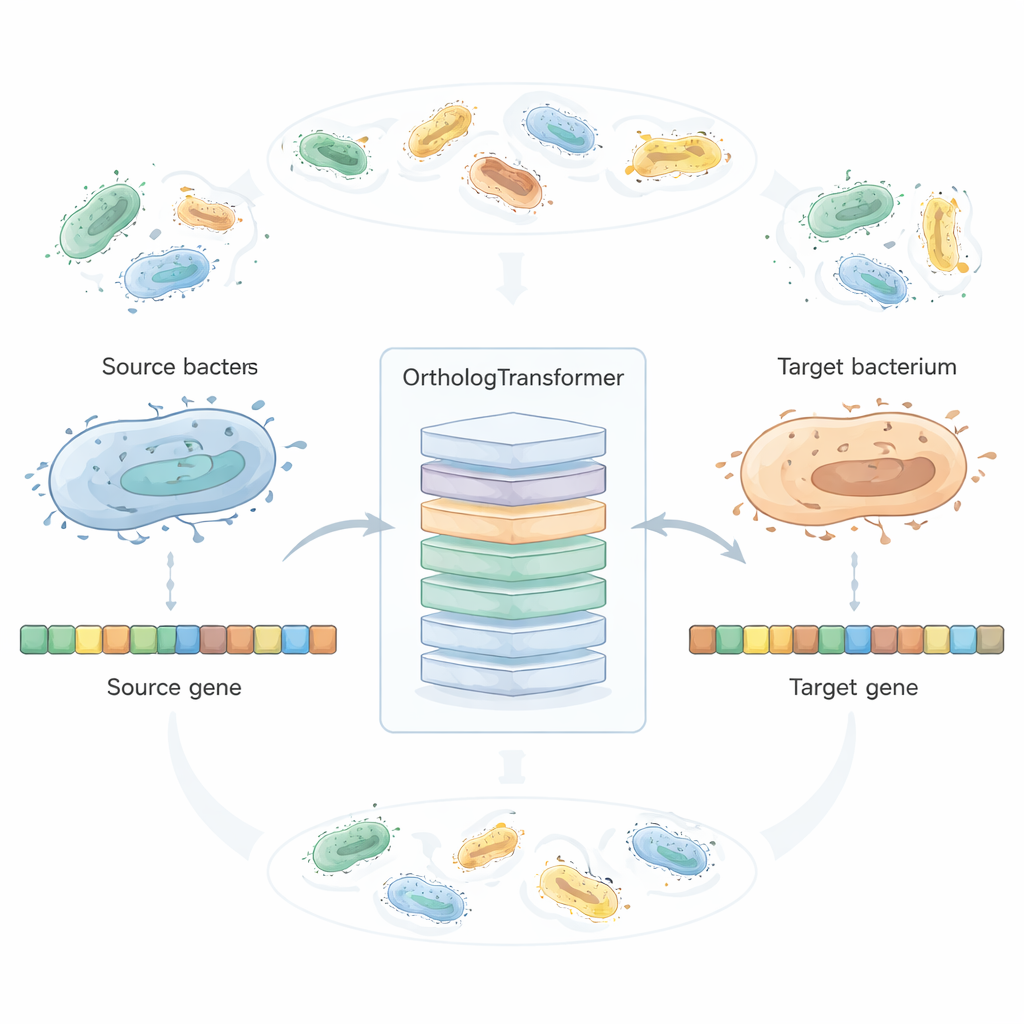
Sätta AI-designade plastätande enzymer i arbete
För att visa att detta är mer än ett rent datorspel fokuserade teamet på PETas, ett enzym från bakterien Ideonella sakaiensis som kan bryta ner PET-plast, materialet i de flesta dryckesflaskor. Ideonella växer långsamt och är inte idealisk för industriell användning, så forskarna bad OrthologTransformer skriva om PETas-genen för en snabbväxande värd, Bacillus subtilis. De genererade ett panel med tolv omdesignade genvarianter, där de utforskade olika träningsinställningar och en extra sökprocedur som sköt sekvenser mot Bacillus-lik DNA-sammansättning och gynnsam RNA-struktur. Trots att vissa varianter bar många DNA-förändringar och några aminosyraförändringar förutsade datormodeller att enzymets kärn-3D-form bevarades. När dessa konstruktioner byggdes och testades i levande Bacillus-celler producerade flera stora mängder utsöndrat PETas, och samtliga uppvisade mätbar plastnedbrytande aktivitet.
En AI-design som överträffar standardoptimering
En AI-designad sekvens, kallad AI-L2, stack ut. Bacillus-celler med denna gen utsöndrade särskilt stora mängder PETas och producerade ungefär tre gånger mer plastnedbrytningsprodukt än någon annan stam i ett sju dagars test, och omkring tio gånger mer än typiska kodonoptimerade kontroller när det mättes via reaktionsprodukter. Mikroskopibilder av PET-filmer exponerade för AI-L2-celler visade djupa gropar och hål där plasten hade ätits bort, mycket mer dramatiskt än i andra förhållanden. Detaljerade enzymtester visade att AI-L2-versionen av PETas inte bara producerades effektivare utan också bearbetade sitt substrat snabbare, vilket gav högre katalytisk effektivitet än både originalet och kodonoptimerade enzymer. Ett parallellt experiment i Escherichia coli visade att en OrthologTransformer-designad version av PETas, även när den endast ändrade kodonanvändning och inte aminosyrasekvensen, fortfarande överträffade en frekvensbaserad kodonoptimerad gen, vilket understryker att modellen fångar subtila, värdspecifika preferenser som traditionella metoder missar. 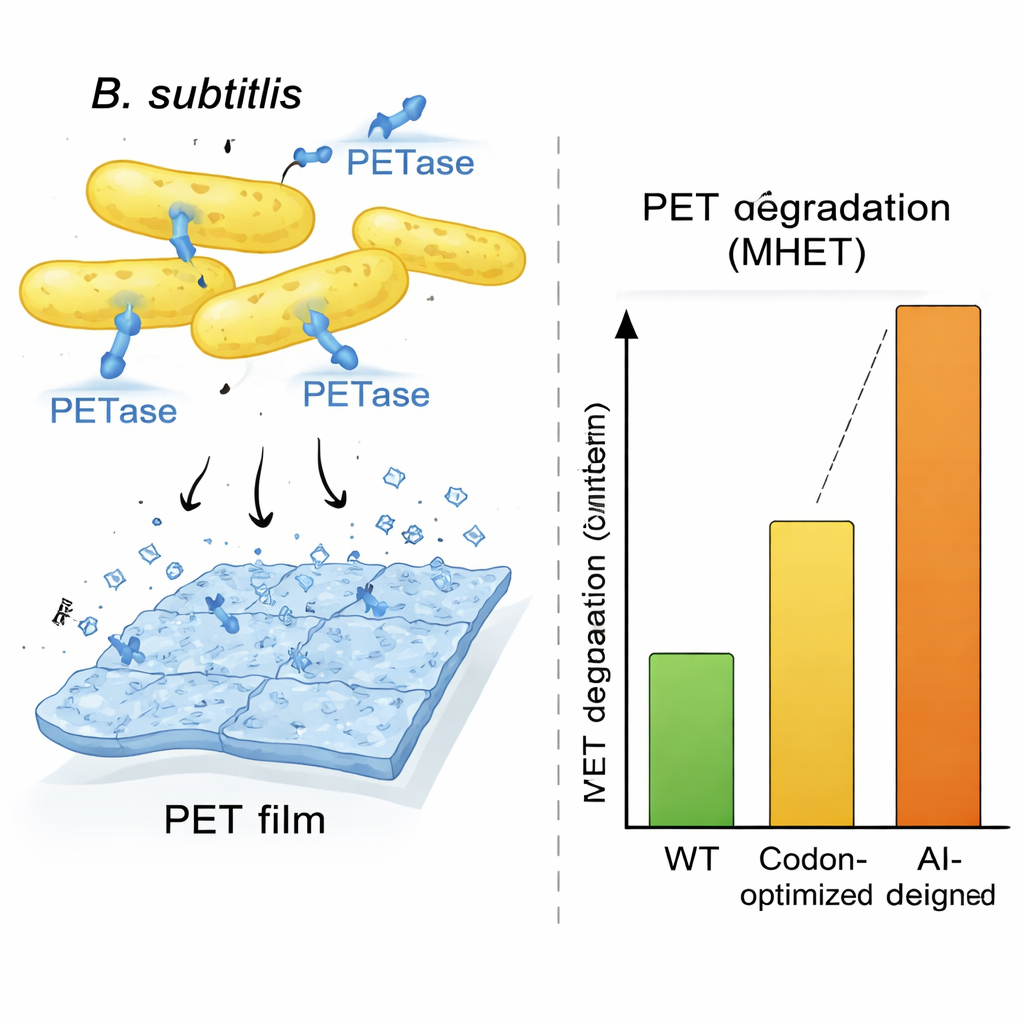
Vad detta betyder för framtidens biologi och teknologi
I vardagliga termer är OrthologTransformer som en expertöversättare som inte bara skriver om en gens ”stavning” för en ny mikroorganism utan också gör små, evolutionärt informerade ändringar i själva ”meningen” när den vet att de kommer att vara säkra eller fördelaktiga. Genom att lära sig direkt från hur gener naturligt har anpassat sig över tusentals bakteriella arter kan den föreslå omdesignad DNA som fungerar bättre i nya värdar än designer begränsade till kodonbyten. Den lyckade skapelsen av ett kraftfullare plastätande enzym i Bacillus subtilis tyder på att sådan AI-styrd generedesign kan påskynda utvecklingen av industriella biokatalysatorer, miljörengöringsmikrober och till slut även medicinska genbehandlingar, så att organismer kan läsa och använda främmande gener som om de vore sina egna.
Citering: Akiyama, M., Tashiro, M., Huang, Y. et al. Cross-species gene redesign leveraging ortholog information and generative modeling. Nat Commun 17, 2120 (2026). https://doi.org/10.1038/s41467-026-69966-0
Nyckelord: generedesign, syntetisk biologi, ortologa gener, AI inom bioteknik, plastnedbrytande enzymer