Clear Sky Science · sv
Th17-celler kräver DNA-reparationssensorn xeroderma pigmentosum komplementationsgrupp C för att kontrollera oxidativ DNA-skada i en murin modell
Våra immundefenders väktare
Hjälpar-T-celler av typen 17, eller Th17-celler, är en särskild sort vita blodkroppar som patrullerar kroppens barriärer, såsom tarm och hud, för att stå emot bakterier och svampar. Men de är också inblandade i autoimmuna sjukdomar när deras svar går fel. Denna studie ställer en förenklat formulerad fråga: hur håller dessa högaktiva celler sitt eget DNA säkert från den kemiska stress de själva skapar när de bekämpar infektioner? Svaret kretsar kring en DNA-skadesensor kallad XPC, mest känd för att skydda hudceller mot solljus. Här visar forskarna att XPC också är avgörande för att hålla Th17-celler friska, energifyllda och effektiva.
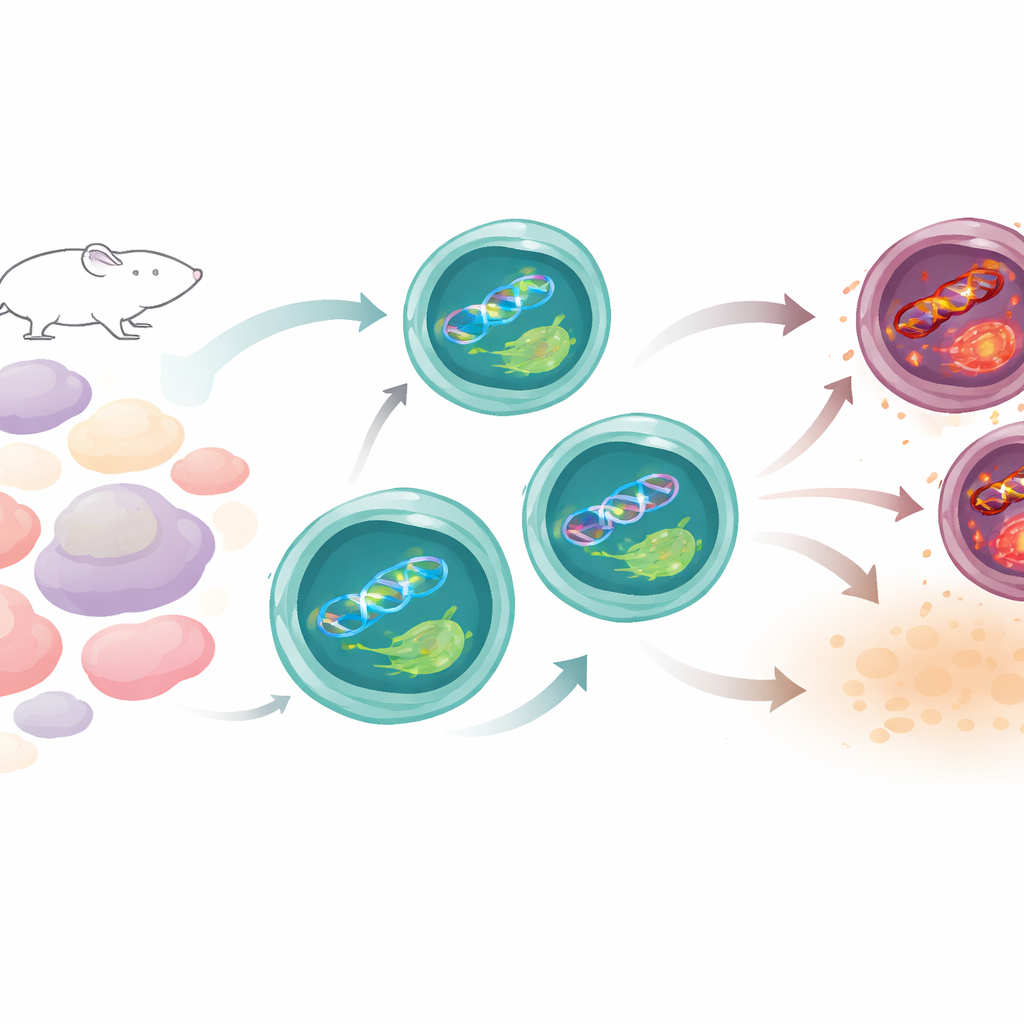
Hur Th17-celler normalt håller balansen
Th17-celler lever ett farligt liv. För att fungera skruvar de upp sin ämnesomsättning och producerar reaktiva syreföreningar—kemiskt reaktiva molekyler som kan skada DNA. Forskarna jämförde Th17-celler med andra T-cells-typer hos möss och fann att, trots deras intensiva aktivitet, ackumulerar Th17-celler mindre DNA-skada än många av sina släktingar. En viktig ledtråd var att gener involverade i DNA-reparation, särskilt de i en väg som vanligtvis lagar solljusskador, var starkare påslagna i Th17-celler. Bland dessa fanns XPC, ett protein som skannar DNA efter strukturella skador. När Th17-celler mognade ökade XPC-nivåerna och lokaliserade till skadade platser i kärnan, vilket tyder på att det var ständigt på patrull för att bibehålla deras genetiska integritet.
Vad händer när DNA-sensorn saknas
För att förstå hur viktig XPC verkligen är använde forskarna möss konstruerade för att sakna detta protein. Vid första anblick såg deras immunsystem mestadels normalt ut: totala T-cellsantalet och många T-cellsundergrupper var oförändrade. Men när teamet fokuserade på Th17-celler framträdde ett slående fel. Utan XPC producerade betydligt färre celler det karakteristiska Th17-molekylen IL-17, och viktiga identitetsmarkörer och signalomkopplare som driver Th17-programmet var nedreglerade. I odlingar hade naiva T-celler från dessa möss svårt att utvecklas till fullt mogna Th17-celler. I en standardmodell där överförda T-celler utlöser tarminflammation lyckades XPC-defekta T-celler inte framkalla kolit, vilket speglar en dämpad inflammatorisk kapacitet. Samtidigt blev regulatoriska T-celler, som dämpar immunsvar, mer talrika, vilket antyder ett förskjutet balansläge mellan aggression och återhållsamhet.
DNA-skada, energifabriker och kemisk stress
Genom att gräva djupare fann teamet att Th17-celler utan XPC bar fler brutna DNA-strängar och fler oxiderade DNA-baser, ett kännetecken för angrepp av reaktiva syreföreningar. Gener som normalt känner av DNA-skada och stoppar cellcykeln var också minskade, vilket tyder på ett försvagat alarmsystem. Cellernas energimetabolism omformades: de förlorade en del av förmågan att använda snabbbrytande sockerbanor och blev mer beroende av mitokondrierna, de små kraftverken inne i cellerna. Ändå läckte dessa mitokondrier mer reaktiva syreföreningar och visade tecken på belastning, vilket skapade en ond cirkel av ökande kemisk stress och växande DNA-skada. Anmärkningsvärt nog återställde behandling av cellerna med en antioxidant IL-17-produktionen och minskade DNA-skadan, vilket direkt kopplar oxidativ stress till det observerade funktionella felet.
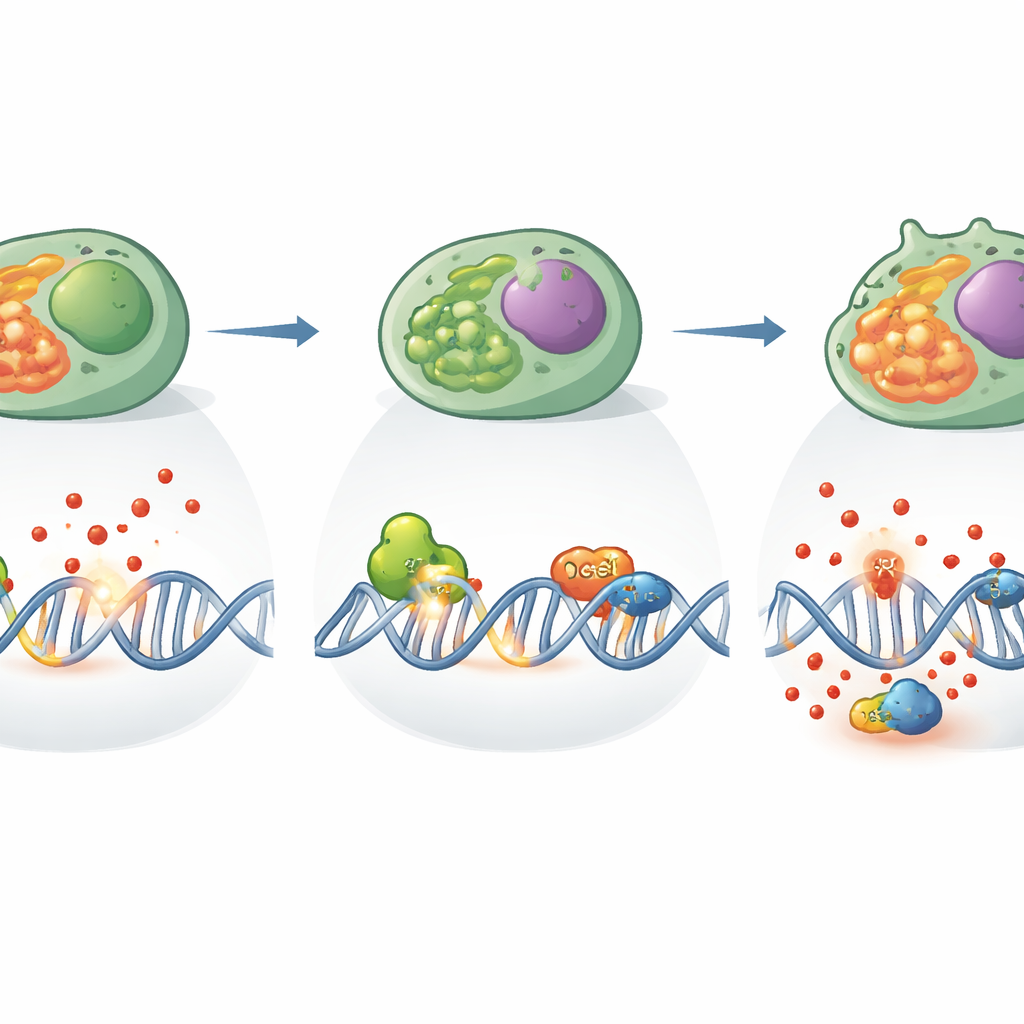
En laginsats för att reparera skadat DNA
Bortom sin klassiska roll samarbetade XPC också med ett annat reparationsprotein kallat OGG1, som känner igen en vanlig oxiderad DNA-bas. Forskarna visade att dessa två proteiner fysiskt associerar i Th17-celler och hjälper till att koordinera borttagningen av skadade baser. När XPC saknades ökade OGG1:s klyvningsaktivitet faktiskt, som om den försökte kompensera för den ökade skadan. Men denna överaktivitet skedde i en miljö med hög oxidativ stress och störda reparationsnätverk, och den räckte inte för att återställa normal Th17-funktion. Genetiska och strukturella analyser föreslog att XPC fungerar som en nav som kopplar samman olika reparationsvägar och redoxkontroll, vilket säkerställer att skador inte bara upptäcks utan också bearbetas på ett sätt som tillåter cellen att fortsätta dela sig och producera skyddande molekyler.
Varför detta är viktigt för sjukdom och terapi
För en lekmannaläsare är huvudbudskapet att immunceller behöver sina egna interna livvakter för att hålla sig friska medan de skyddar oss. Denna studie visar att XPC, tidigare berömt för att skydda hudceller mot UV-ljus, också är en viktig väktare för Th17-celler och håller deras DNA intakt och deras energisystem i balans under oxidativ stress. När XPC saknas blir Th17-celler genetiskt och metabolt sårbara, producerar mindre inflammatoriskt utflöde och kan förskjuta immunbalansen mot reglering snarare än attack. Eftersom Th17-celler är centrala i tillstånd som inflammatorisk tarmsjukdom, psoriasis och multipel skleros, kan vägar som kontrolleras av XPC bli nya mål för att finjustera immunresponsen—antingen för att dämpa skadlig inflammation eller förstärka försvaret där det är för svagt—genom att modulera hur dessa celler reparerar sitt DNA och hanterar oxidativ stress.
Citering: Leite, J.A., Bos, N.N., Menezes-Silva, L. et al. Th17 cells require the DNA repair sensor xeroderma pigmentosum complementation Group C to control oxidative DNA damage in a murine model. Nat Commun 17, 3157 (2026). https://doi.org/10.1038/s41467-026-69914-y
Nyckelord: Th17-celler, DNA-reparation, oxidativ stress, XPC-protein, autoimmun sjukdom