Clear Sky Science · sv
VAMP7-beroende sen endosomal sekretion av ER- och mitokondriella proteiner påverkar tumörmikromiljön och makrofagengagemang
Hur stressade celler signalerar om hjälp
Cancerceller har ett hårt liv. Utsatta för syre- och näringsbrist samlar de på sig skador i cellernas små kraftverk (mitokondrier) och proteinfabriker (endoplasmatiska retiklet, ER). Denna studie avslöjar ett oväntat sätt på vilket stressade celler kastar ut skadade delar av dessa inre strukturer till omgivningen. I hjärntumörer som kallas glioblastom visar det sig att detta cellulära ”soporexport”-system, drivet av ett protein som heter VAMP7, påverkar hur immunceller uppfattar och tränger in i tumören.
Dolda transportsystem inne i celler
De flesta proteiner som lämnar en cell följer en klassisk väg: de går in i ER, passerar genom en central sorteringsstation kallad Golgi-apparaten och packas sedan i små blåsor som smälter samman med cellmembranet. Men celler förlitar sig också på okonventionella vägar som kringgår Golgi. En sådan väg använder sena endosomer—inre säckar som kan förenas med ytan och släppa ut sitt innehåll. Författarna koncentrerar sig på ett molekylärt ”blixtlås”-protein, VAMP7, redan känt för att hjälpa sena endosomer att smälta samman med cellens yttermembran och frigöra små extracellulära vesikler, mikropaket som transporterar innehåll mellan celler.
Flytta utslitna delar till utgången
Genom att använda genmodifierade råttnjure- och gliomceller som saknar VAMP7 följde forskarna vad som händer med proteiner som normalt finns i ER och mitokondrier. De visade att utan VAMP7 släppte cellerna ut mycket mindre av en kort form av det ER-formande proteinet RTN3 och av VDAC, en kanal på mitokondriens yta. Samtidigt blev sena endosomer felplacerade och små vesikler rika på markören CD63 sekretorerades dåligt. Högupplöst avbildning och närhetsanalyser visade att RTN3 och mitokondriellt material fysiskt associerar med CD63-positiva sena endosomer innan de släpps ut, och att denna överlämning beror på VAMP7 och dess partner-fusionsproteiner. Dessa fynd stöder en modell där stressade ER och mitokondrier knoppas av små vesikler som smälter samman med sena endosomer, vilka sedan exporterar sitt last ut ur cellen. 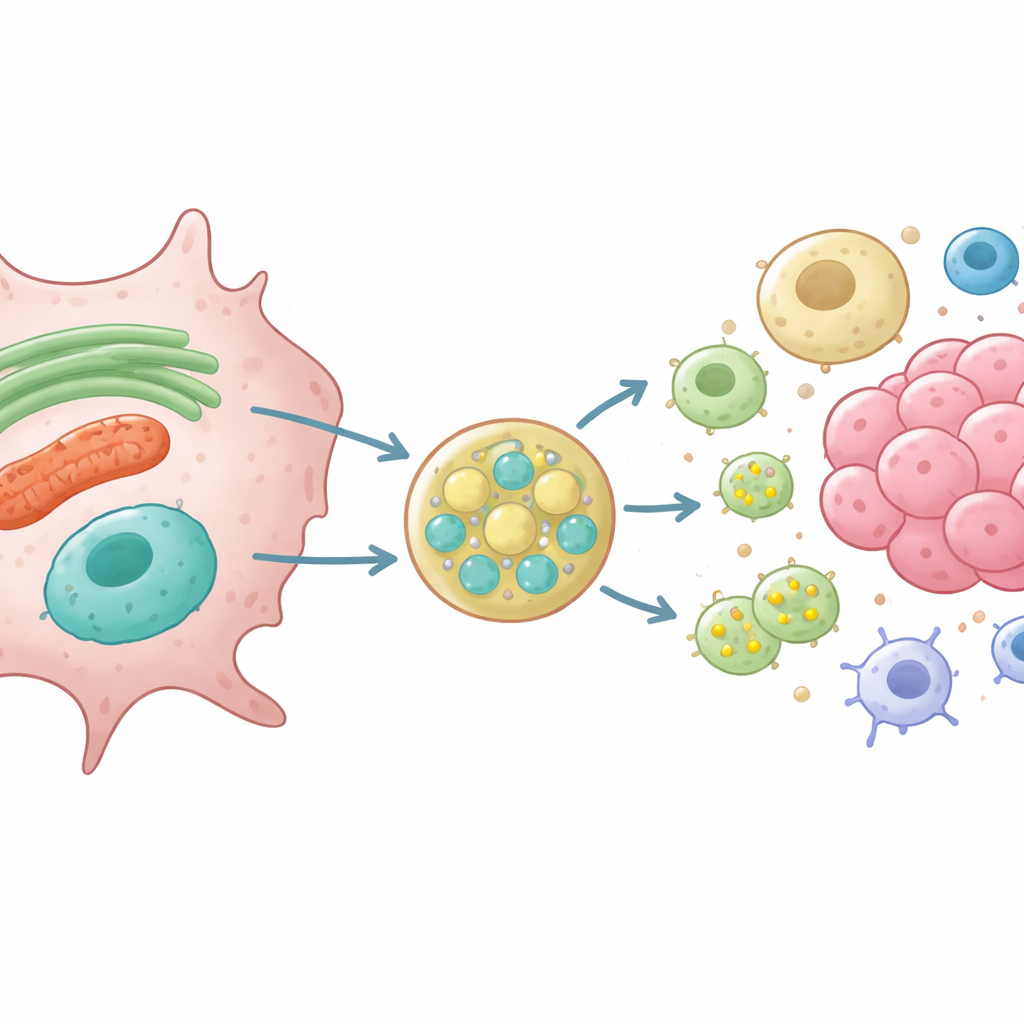
Stresslindring och kvalitetskontroll
Celler som saknade VAMP7 förlorade inte den allmänna återvinningsvägen som kallas autophagi, men de visade tydliga tecken på belastning. Genuttrycksmönster pekade på aktivering av stressresponser i ER och förändringar i mitokondrierelaterade gener. Mikroskopi avslöjade abnorma ”virvlar” av ER-membran och överdrivet förenade, förlängda mitokondrier—båda kännetecken på organeller som kämpar för att bibehålla balans. Mätningar av syreförbrukning visade att trots ökad mitokondriell massa hade celler utan VAMP7 eller utan ett nyckelprotein i autophagi (ATG5) svagare energiproduktion. När forskarna medvetet framkallade ER- eller mitokondriell stress med läkemedel ökade celler med intakt VAMP7 utsöndringen av RTN3 respektive VDAC. Denna ökning försvann när VAMP7 togs bort, vilket antyder att sen endosomal sekretion fungerar som en tryckventil för att göra sig av med skadade komponenter och sända ut cellens inre tillstånd.
Formar tumörnärmiljön
För att pröva betydelsen av denna väg i sjukdom vände teamet sig till en råttmodell av glioblastom, en mycket aggressiv hjärntumör. De implanterade normala, VAMP7-defekta eller ATG5-defekta gliomceller i råtthjärnor. Tumörer som uppstod från VAMP7-borttagna celler växte sig stora och innehöll mycket mer död vävnad, men var infiltrerade av färre makrofager—de immunceller som fagocyterar skräp och kan påverka om en tumör växer eller avstannar. Däremot var tumörer utan ATG5 överlag mindre men visade inte samma selektiva minskning i makrofaginträde i tumörens kärna. Analyser av mänskliga hjärntumördatasätt visade vidare att lägre uttryck av VAMP7 (och RTN3) är kopplat till sämre patientöverlevnad, vilket tyder på att denna stresskopplade sekretionsväg naturligt kan verka för att hämma tumörprogression genom att forma det immunologiska landskapet. 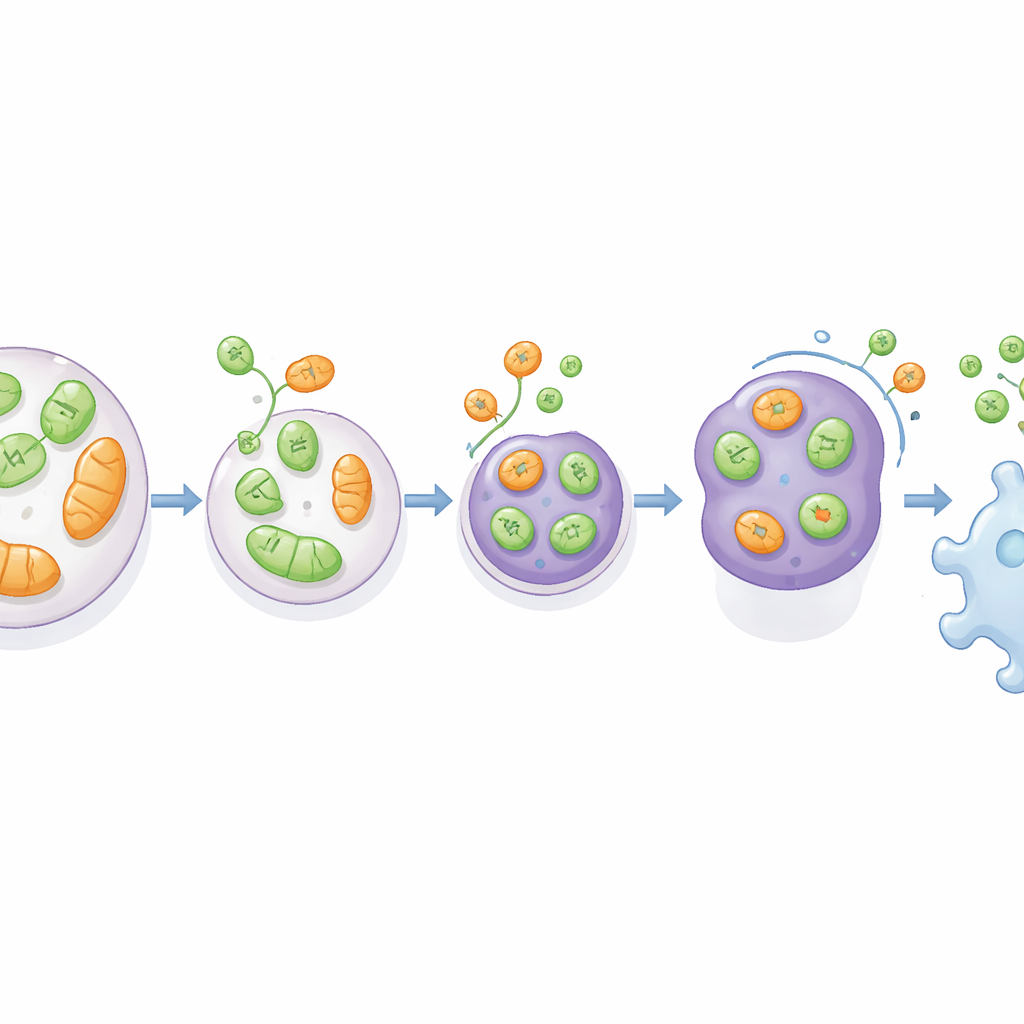
Varför detta spelar roll för cancer och immunitet
Enkelt uttryckt föreslår studien att VAMP7 hjälper celler att paketera och exportera skadade delar av sitt inre maskineri via sena endosomer, särskilt under stress. I glioblastom verkar denna utåtström av ER- och mitokondrieavledet material fungera som en nödsignal som uppmuntrar makrofager att gå in i tumören och rensa upp skräp, vilket bidrar till en mer tumörhämmande miljö. När VAMP7 saknas försvagas signalen, organellskador ackumuleras, tumörer blir mer nekrotiska och makrofagengagemang minskar. Att förstå och potentiellt justera detta sekretoriska kvalitetskontrollsystem kan öppna nya möjligheter att göra svårbehandlade tumörer mer synliga för och mottagliga för immunsystemet.
Citering: Vats, S., Dionisio, P., Lemercier, Q. et al. VAMP7-dependent late endosomal secretion of ER and mitochondrial proteins impacts the tumor microenvironment and macrophage engagement. Nat Commun 17, 3012 (2026). https://doi.org/10.1038/s41467-026-69900-4
Nyckelord: okonventionell proteinkomsekretion, VAMP7, glioblastom, tumörmikromiljö, extracellulära vesikler