Clear Sky Science · sv
Eukaryot initieringsfaktor 6 påverkar plasticiteten hos småcellig lungkarcinom via integrin‑FAK‑signaleringsaxeln
Varför denna lungcancerforskning är viktig
Småcellig lungkarcinom (SCLC) är en av de dödligaste formerna av lungcancer. Tumören svarar ofta väl på kemoterapi initialt, men återkommer nästan alltid, snabbt och aggressivt. Denna studie ställer en central fråga: vad gör att SCLC‑celler kan "byta personlighet" och bli läkemedelsresistenta, och kan den formskiftningen bromsas eller blockeras?
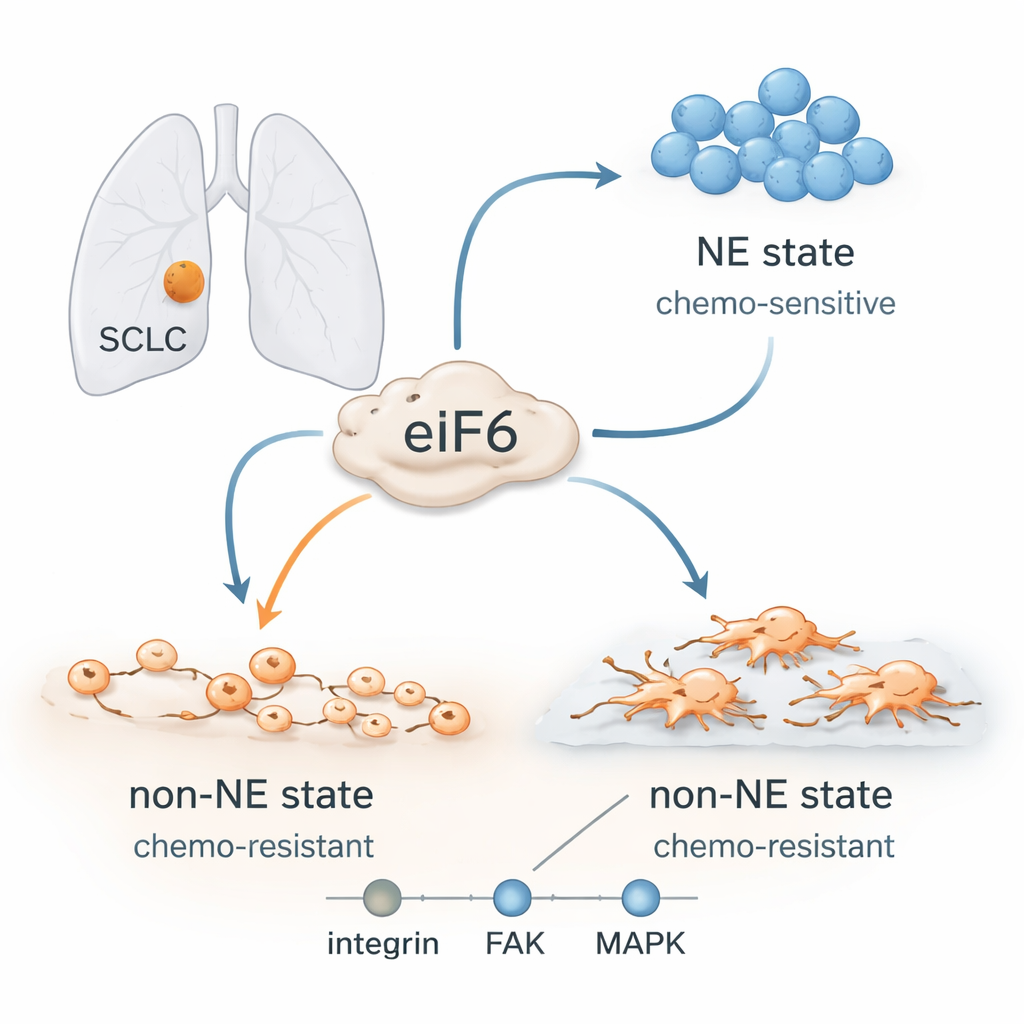
Formskiftande cancerceller
Läkare trodde tidigare att SCLC var en enhetlig sjukdom, men det är nu tydligt att dessa tumörer innehåller olika celltyper. Vissa celler har en stark ”neuroendokrin” identitet: de växer i täta flytande kluster, svarar bra på platina‑baserad kemoterapi och är ofta rika på vissa nervliknande proteiner. Andra tappar denna identitet och antar ett ”icke‑neuroendokrint” tillstånd: de sprider sig, fäster vid omgivande vävnad, visar drag av mer rörliga, invasiva celler och är mycket svårare att döda med läkemedel. Patienters tumörer utvecklas ofta från det känsliga tillståndet till det resistenta under eller efter behandling, trots att deras DNA inte förändras mycket. Det pekar på flexibla cellprogram snarare än nya mutationer som drivkraft för återfall.
En translationsfaktor med dubbelliv
Författarna fokuserade på ett protein kallat eIF6, mest känt för att hjälpa till vid ribosomuppbyggnad, cellens proteintillverkningsmaskineri. Genom att studera patientprover, musemodeller och flera humana SCLC‑cellinjer fann de att nivåerna av eIF6 konsekvent ökade när celler skiftade till det läkemedelsresistenta, icke‑neuroendokrina tillståndet. Överraskande nog följde denna ökning en samtidig minskning i total proteintillverkning, vilket antyder att eIF6 kan göra mer än sin läroboksuppgift. Detaljerade analyser av hur budbärar‑mRNA binder till ribosomer visade att de grundläggande ribosomdelarna inte förändrades mycket. Istället omformades hur budskap valdes ut och bearbetades för translation när cellerna bytte identitet.
Bryter sig loss för att kopplas till överlevnadssignaler
När teamet grävde djupare upptäckte de att i resistenta celler lossnar eIF6 delvis från ribosomerna och associerar med en ytsignaleringsknutpunkt byggd kring integriner och ett protein kallat focal adhesion kinase (FAK). Integriner hjälper celler att känna av och fästa vid sin omgivning; FAK förmedlar dessa signaler inåt och aktiverar ofta vägar som stödjer rörelse, överlevnad och läkemedelstolerans. Biokemiska pull‑downs och proximitetsanalyser i cell visade att eIF6 fysiskt interagerar med integrinpartnern CD104 och med FAK, och att dessa komplex är mer rikliga i icke‑neuroendokrina celler. Denna eIF6–integrin–FAK‑sammansättning ökar i sin tur aktiviteten i MAPK‑signaleringsvägen, en välkänd drivare av tillväxt och stresstolerans.
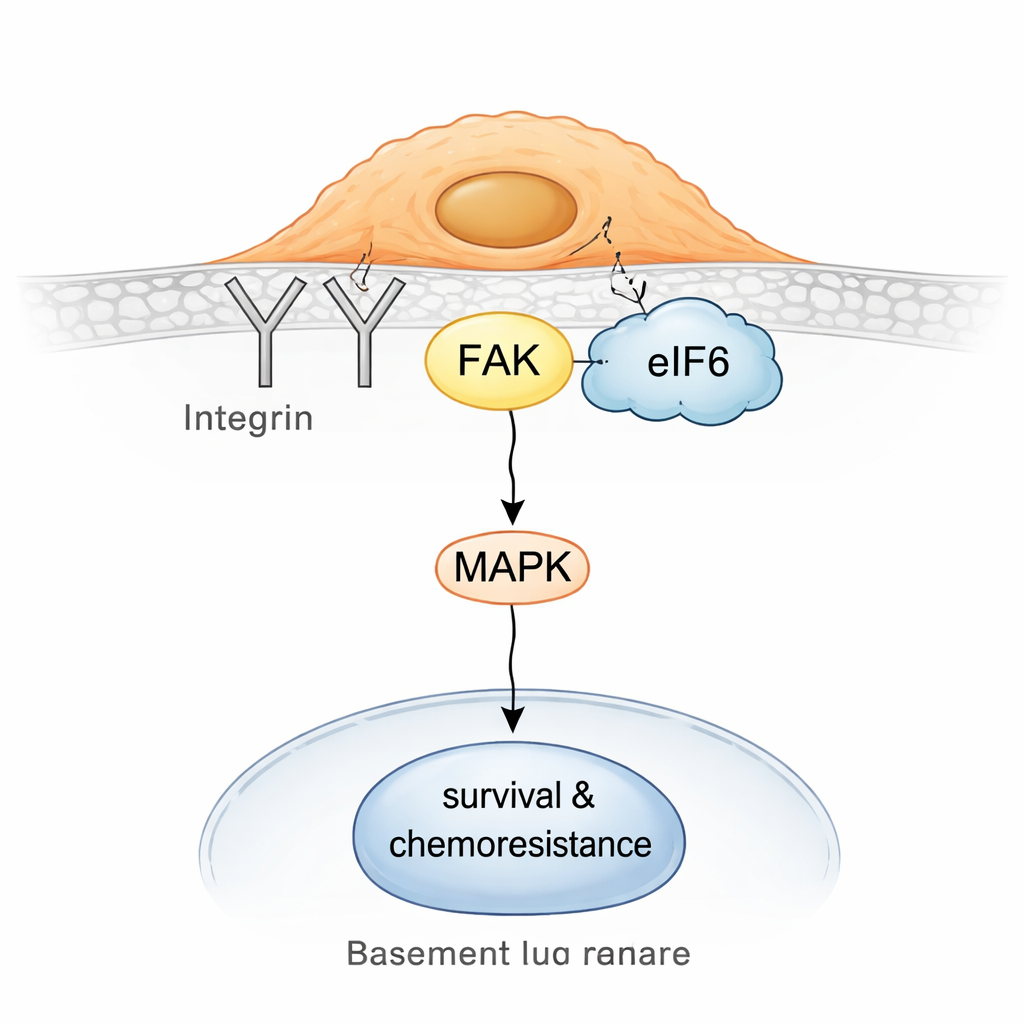
Göra resistenta tumörer sårbara igen
Forskarna frågade sedan om manipulation av eIF6 kunde ändra SCLC:s beteende. När de minskade eIF6‑nivåerna i resistenta celler sänktes genuttryck kopplat till ett rörligt, ärrbildande (epitel‑mesenkymalt) program, samtidigt som klassiska neuroendokrina gener delvis återställdes. Dessa förändringar återställde inte fullt ut cellernas ursprungliga tillstånd, men de bromsade övergången mot det resistenta tillståndet. Viktigt är att celler med mindre eIF6 blev mer känsliga för standardkemoterapin karboplatin–etoposid i odling och i musstumörer, med färre överlevande kolonier och mer varaktig krympning. Eftersom eIF6 i nuläget saknar specifika läkemedel testade teamet FAK‑hämmare som redan är under klinisk utveckling. Blockering av FAK‑signalering återkänsliggjorde resistenta celler för kemoterapi och i möss gav kombinationsbehandlingen det starkaste tumörkontrollen.
Från laboratorieinsikt till framtida patientverktyg
Slutligen undersökte författarna tumörprover från patienter med begränsad SCLC som genomgått kirurgi. Med en känslig färgningsteknik som lyser upp proteiner endast när de är nära varandra mätte de hur ofta eIF6 sitter i komplex med CD104 eller FAK inne i tumörceller. Höga nivåer av dessa komplex — mer än eIF6 ensam — kopplades till tidigare återfall och kortare överlevnad, vilket gör dem till lovande prognostiska markörer. Sammanfattningsvis visar detta arbete att eIF6 kan "moonlighta" bort från ribosomer för att hjälpa koppla cancerceller till kraftfulla överlevnadscircuiter. Genom att kartlägga denna eIF6–integrin–FAK‑axel föreslår studien sätt att identifiera patienter med högre återfallsrisk och stöder kombinationen av FAK‑hämmare med kemoterapi för att motverka SCLC:s farliga plasticitet.
Citering: Peng, H., Wang, Z., Wang, M. et al. Eukaryote initiation factor 6 modulates small-cell lung carcinoma plasticity via the integrin-FAK signaling axis. Nat Commun 17, 2048 (2026). https://doi.org/10.1038/s41467-026-69899-8
Nyckelord: småcellig lungcancer, läkemedelsresistens, cellplasticitet, eIF6, integrin FAK‑signalering