Clear Sky Science · sv
Kontextberoende översättningshämmning som en cancerterapeutisk metod
Att vända proteinfabrikerna mot cancer
Cancerceller överlever genom att ständigt producera stora mängder kortlivade ”drivar”‑proteiner som håller dem växande och delande. Denna studie undersöker ett nytt sätt att bekämpa cancer genom att subtilt blockera cellens proteinproducerande maskineri—ribosomerna—bara när de försöker bygga specifika proteinsekvenser, särskilt sådana som återfinns i svår‑att‑läkemedelsätta onkogener som MYC. Denna selektiva störning skulle kunna döda tumörceller samtidigt som den i stort sett sparar normal proteinproduktion.
Hur celler bygger proteiner—och var det kan gå fel
Varje cell är beroende av ribosomer, små molekylära fabriker som läser genetiska budskap (mRNA) och fogar samman aminosyror till proteiner. De flesta befintliga läkemedel som riktar sig mot ribosomer, såsom antibiotika eller äldre cancerläkemedel, fungerar som trubbiga verktyg: de stänger överlag av proteinsyntesen, vilket kan skada friska celler och orsaka allvarliga biverkningar. Författarna resonerade att eftersom varje nysyntetiserad proteinkedja har sin egen unika sekvens och kemiska karaktär, kan det vara möjligt att designa små molekyler som bara blockerar ribosomen när en specifik sekvens befinner sig i maskinen, och lämnar resten av cellens proteinproduktion i stort sett intakt.
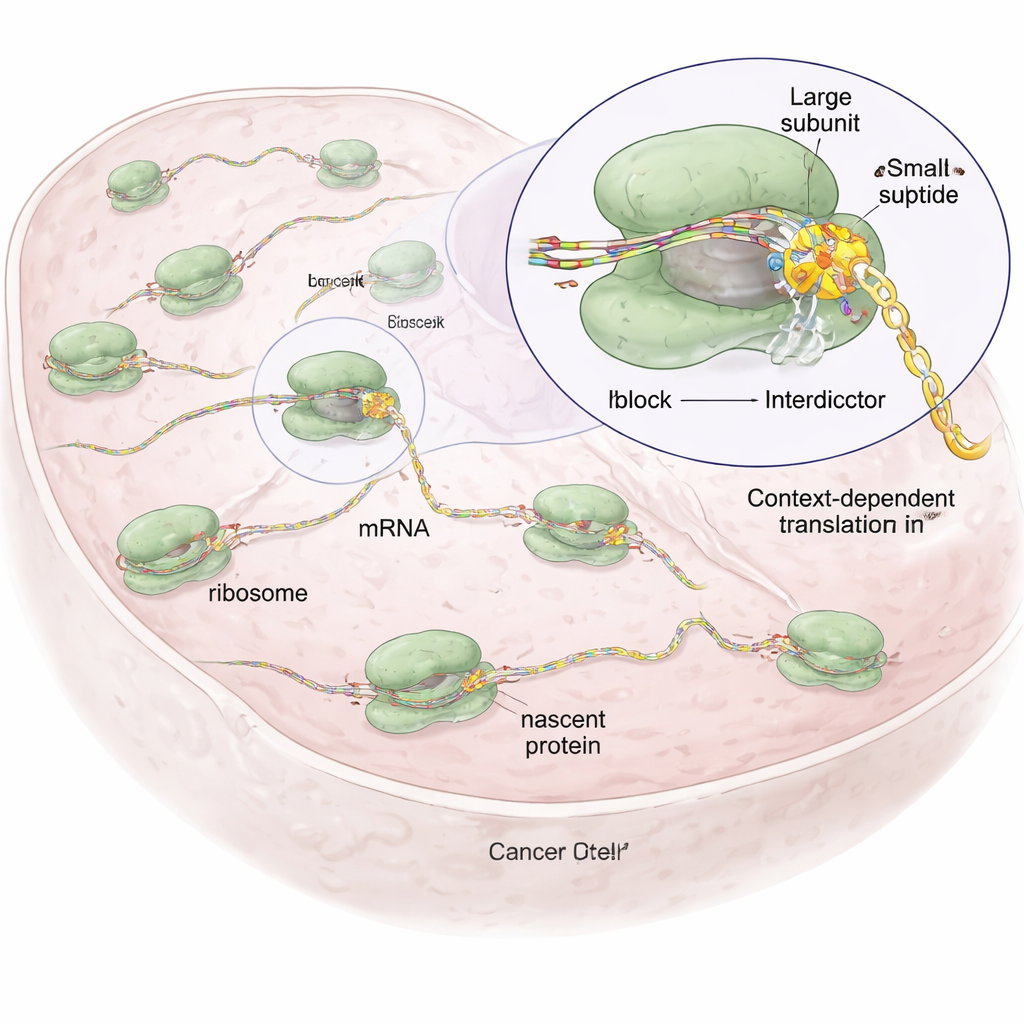
Designade molekyler som endast stannar vissa proteinsekvenser
Byggt på en naturlig förening kallad anisomycin, som binder till ribosomens katalytiska centrum där peptidbindningar bildas, skapade forskarna en familj syntetiska molekyler som de kallar ”interdictors”. Alla delar en kärnskallett som förankrar dem inne i ribosomen, men de skiljer sig åt i sidogrupper som pekar mot den växande proteinkedjan. Dessa sidogrupper är anpassade för att gynna särskilda typer av aminosyror—till exempel attraheras en interdictor (IDB‑001) av negativt laddade restgrupper, medan en annan (IDB‑002) föredrar små, oljiga (hydrofoba) rester. Med en teknik som kallas ribosomprofilering, vilken globalt kartlägger var ribosomer stannar på mRNA i celler, visade teamet att varje förening orsakar pauser vid distinkta korta motiv i den nysyntetiserade kedjan, ofta vid den näst sista (−1) aminosyran, vilket visar sekvensberoende verkan snarare än godtycklig nedstängning.
Att se läkemedlet och ribosomen mötas atom för atom
För att förstå hur denna selektivitet fungerar i fysisk detalj frös författarna mänskliga ribosomer mitt i översättningen av designade peptidsekvenser och avbildade dem med kryogen elektronmikroskopi i nästan atomupplösning. De observerade interdictorn insluten i ribosomens aktiva säte och såg precisa kontakter med de sista aminosyrorna i den nysyntetiserade kedjan. I en struktur ligger en hydrofob sidogrupp på IDB‑002 inbäddad av små icke‑skrymmande rester i peptiden, vilket förklarar varför större sidokedjor där är missgynnade. I en annan struktur svänger en sur sidokedja från en MYC‑härledd rest för att bilda en saltkolv med en positivt laddad grupp på IDB‑001. Läkemedlets närvaro skjuter också närliggande ribosomalt RNA‑baser till nya positioner som snävnar av det aktiva sätet och delvis blockerar inträdet av nästa tRNA, vilket hjälper till att frysa elongationen vid dessa favoriserade sekvenser.
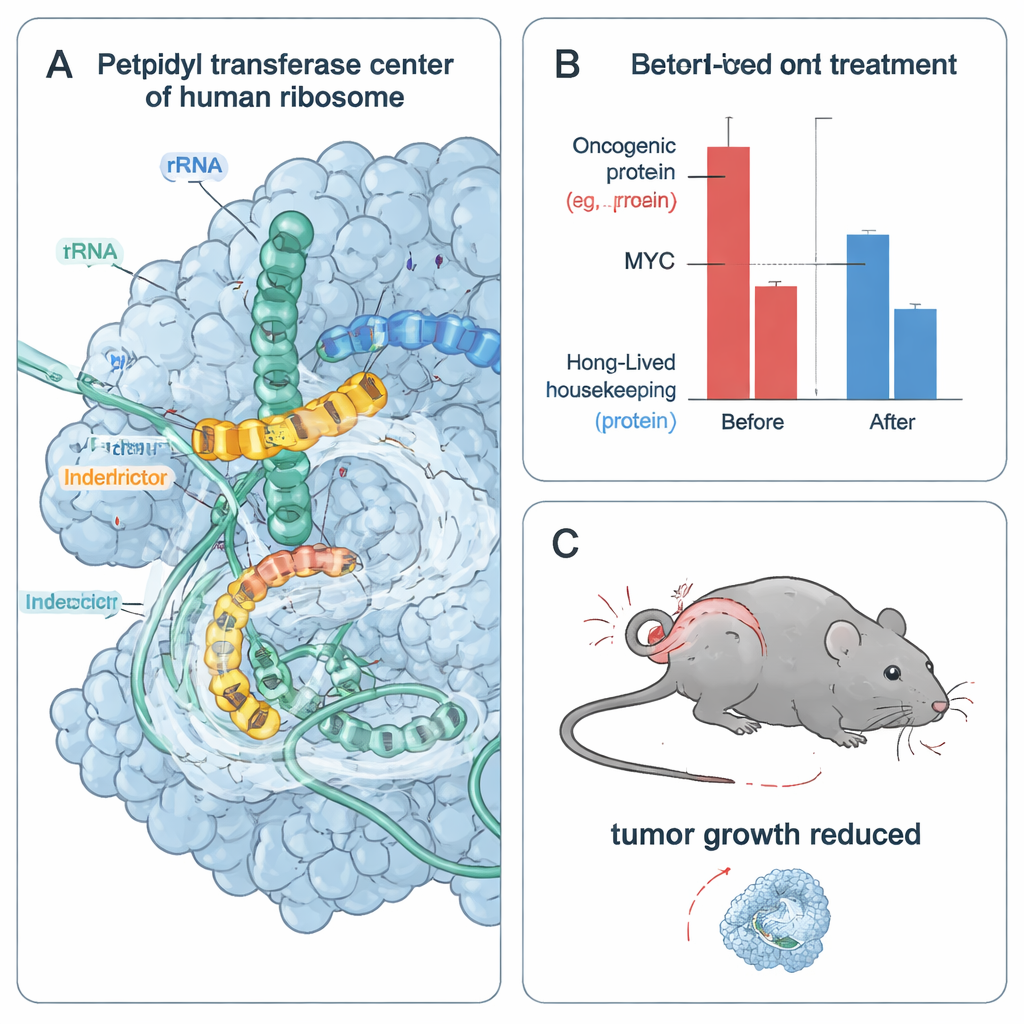
Från stillastående ribosomer till stressade och döende tumörceller
Där snabbt delande cancerceller är starkt beroende av kortlivade onkogena proteiner som MYC och CCND1 testade teamet hur interdictors påverkar tumörcellers överlevnad. I flera MYC‑beroende cancercellslinjer minskade IDB‑001 och IDB‑002 cellviabiliteten vid nanomolära till lågmikromolära koncentrationer. En vidareoptimerad analog, IDB‑003, var ännu potenter och lämpad för oral dosering. I celler tömde dessa föreningar snabbt MYC och andra snabbvändande onkoproteiner medan längrelevande hushållsproteiner förblev relativt stabila under samma tidsfönster. Läkemedlen utlöste också cellulära stressresponser kopplade till kolliderade ribosomer, men blockering av dessa stress‑signalvägar eliminerade inte viabilitetsförlusten, vilket tyder på att direkt deprivation av väsentliga onkogena proteiner är en huvudorsak till tumörcelldöd.
Bevis på koncept i en svår bröstcancersmodell
För att testa om detta tillvägagångssätt fungerar i djur behandlade författarna möss med human trippelnegativ bröstcancer tumörer med oralt administrerad IDB‑003. Under 28 dagar växte behandlade tumörer betydligt långsammare än i kontrollgrupperna, med upp till 80 % hämning av tumörtillväxt vid högre doser och inga allvarliga toxicitetsrapporter i denna studie. Genuttrycksanalyser av tumörerna visade stark nedreglering av MYC‑målprogram, i linje med minskad MYC‑aktivitet in vivo. Tillsammans visar dessa resultat att selektivt stanna ribosomer på specifika proteinsekvenser kan försvaga tumörer som är beroende av instabila onkogena drivkrafter samtidigt som man potentiellt undviker den breda toxiciteten hos klassiska translationsblockerare.
Varför detta är viktigt för framtida cancerbehandlingar
Detta arbete introducerar en ny typ av småmolekylärt läkemedel: ett som inte verkar genom att binda ett färdigt protein, utan genom att avlyssna det medan det tillverkas och endast när en kort ”adress‑tagg”‑sekvens är närvarande. Eftersom många cancerfrämjande proteiner är lösa, kortlivade eller saknar uppenbara fickor för konventionella läkemedel, kan riktning mot deras syntes direkt vid ribosomen öppna en väg för behandling av tumörer drivna av hittills ”otlätbara” gener som MYC. Studien antyder också att genom att finjustera interdictors kemi kan framtida läkemedel utformas för att fokusera på olika sekvensmotiv och sjukdomsmål, vilket skulle kunna utvidga strategin bortom onkologi till andra tillstånd där nedreglering av specifika proteiner kan återställa hälsa.
Citering: Diamond, P.D., Sauer, P.V., Holm, M. et al. Context-dependent translation inhibition as a cancer therapeutic modality. Nat Commun 17, 1963 (2026). https://doi.org/10.1038/s41467-026-69891-2
Nyckelord: ribosom‑riktad cancerterapi, hämning av translation, MYC‑drivna tumörer, kontextberoende små molekyler, trippelnegativ bröstcancer