Clear Sky Science · sv
TRIM13 in situ‑modifiering ökar CAR‑makrofagers antiinflammatoriska kapacitet för leverfibrosterapi
Omskolning av leverns städpatrull
Leverfibros, en ärrbildningsprocess som kan leda till cirros och leversvikt, drabbar miljoner människor och har i dag få effektiva behandlingar. Denna studie undersöker ett sätt att utnyttja och omprogrammera leverns egna immunceller så att de inte bara avlägsnar ärrbildande celler utan också dämpar skadlig inflammation — vilket potentiellt kan erbjuda en säkrare och mer kraftfull terapi för kronisk leversjukdom.
Varför leverärr är svåra att stoppa
När levern skadas om och om igen — av virus, alkohol eller metabola sjukdomar — försöker den läka genom att lägga ner ärrvävnad. Specialiserade celler som kallas leverstellatceller (hepatiska stellatceller) övergår till ett ”aktiverat” tillstånd och producerar kraftiga fibrer, ungefär som byggarbetare som häller ut betong. Med tiden förvränger denna ärrbildning, känd som fibros, organets struktur och försämrar dess funktion. Immunceller kallade makrofager sitter i centrum av denna process. I en skadad lever kan de agera som ett tveeggat svärd: i ett läge driver de inflammation och aktiverar stellatceller, medan de i ett annat, mer läkande läge, hjälper till att bryta ned ärrvävnad och återställa balans.
Att vända skadliga signaler till hjälpsamma
Forskarna fokuserade på en nyckelsignal vid skadade leverceller: mitokondriellt DNA som läcker ut från skadade celler. Makrofager känner igen detta DNA via en väg känd som cGAS‑STING, vilket skjuter dem mot ett proinflammatoriskt, ärrfrämjande tillstånd. Ett protein kallat TRIM13 hjälper normalt till att hålla STING i schack genom att märka det för nedbrytning. Gruppen antog att en förstärkning av TRIM13 inne i levermakrofager skulle kunna få dem att återgå till ett lugnande, vävnadsreparerande läge. Samtidigt ville de att dessa celler direkt skulle söka upp och ta bort de ärrbildande stellatcellerna. För det ändamålet använde de konceptet chimerisk antigenreceptor (CAR) hämtat från cancerterapi: en syntetisk receptor som låter immunceller känna igen ett valt mål — i detta fall ett protein kallat FAP som är rikligt uttryckt på aktiverade stellatceller.
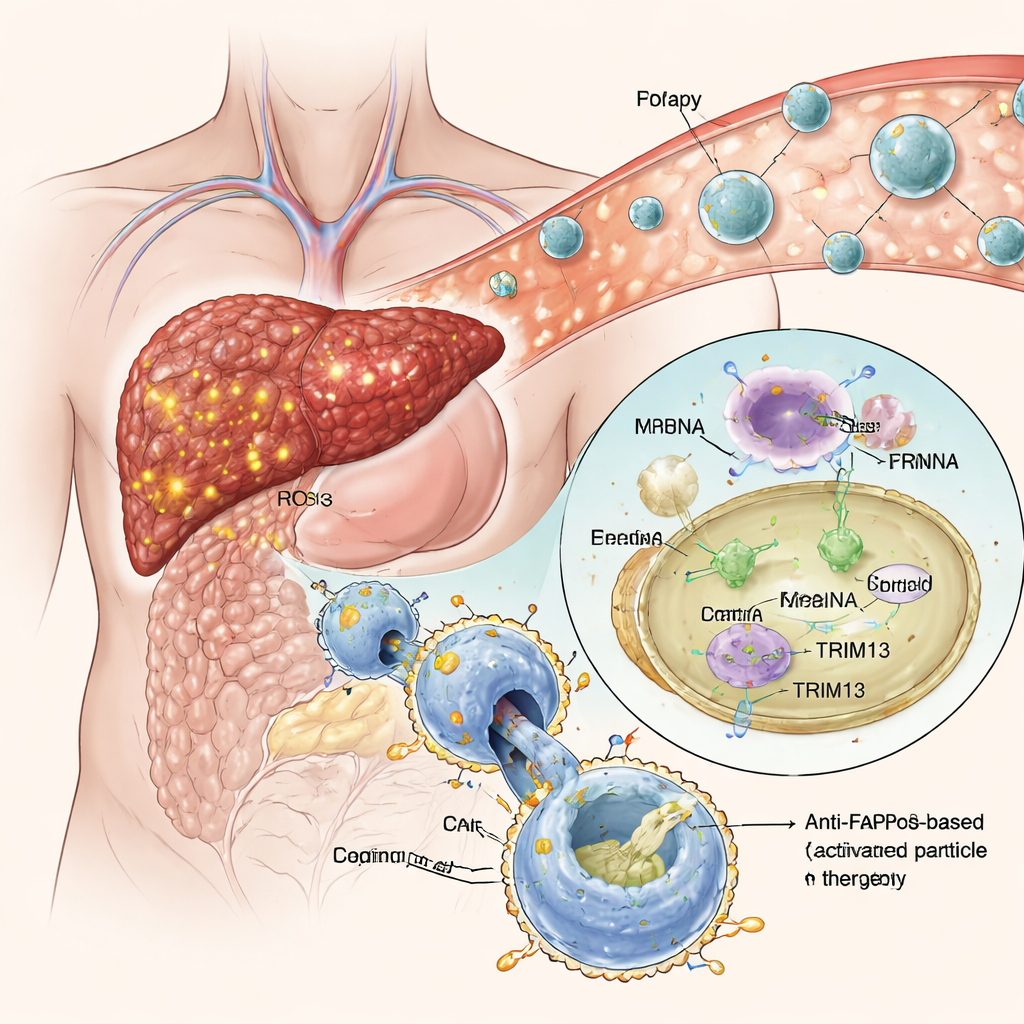
Smarte nanopartiklar som söker sig till sjuk vävnad
I stället för att modifiera makrofager utanför kroppen byggde teamet ”efferocytos‑utlösta” lipidnanopartiklar — små fettbaserade sfärer som bär genetiska instruktioner som budbärar‑RNA (mRNA). Dessa partiklar är täckta med en förklädd form av fosfatidylserin, en naturlig ”ät‑mig” signal som döende celler visar för att locka makrofager. I den högoxidativa miljön i fibrotisk levervävnad avlägsnas förklädnaden och signalen blottläggs, vilket får närliggande makrofager att omsluta nanopartiklarna. När de väl är inne släpps mRNA ut och läses av cellen, vilket leder till produktion av både TRIM13 och anti‑FAP‑CAR. I cellkulturer drev denna strategi framgångsrikt makrofager mot ett antiinflammatoriskt tillstånd samtidigt som den gav dem en stark, selektiv aptit för FAP‑positiva ärrbildande celler, utan att störa deras normala förmåga att rensa annat skräp.
Från sjuk till regenererande lever hos möss
Teamet testade sedan strategin i musmodeller av leverfibros framkallad antingen av en toxisk kemikalie eller av en fettrik, näringsfattig diet. Systemiskt injicerade nanopartiklar nådde effektivt levern och togs, särskilt i fibrotiska djur, främst upp av makrofager. Där visade de modifierade cellerna reducerad aktivitet i STING‑vägen och lägre produktion av inflammatoriska molekyler, tillsammans med ökad förmåga att döda aktiverade stellatceller. Vävnadsanalyser visade på markanta minskningar av kollagen och andra ärrmarkörer, en finare och mer normal extracellulär matrixstruktur samt förbättrade blodvärden för leverfunktion. Leverna hos behandlade möss visade fler prolifererande celler och återvunnen, hälsosammare arkitektur, vilket tyder på verklig organreparation snarare än bara en tillfällig dämpning av inflammation.
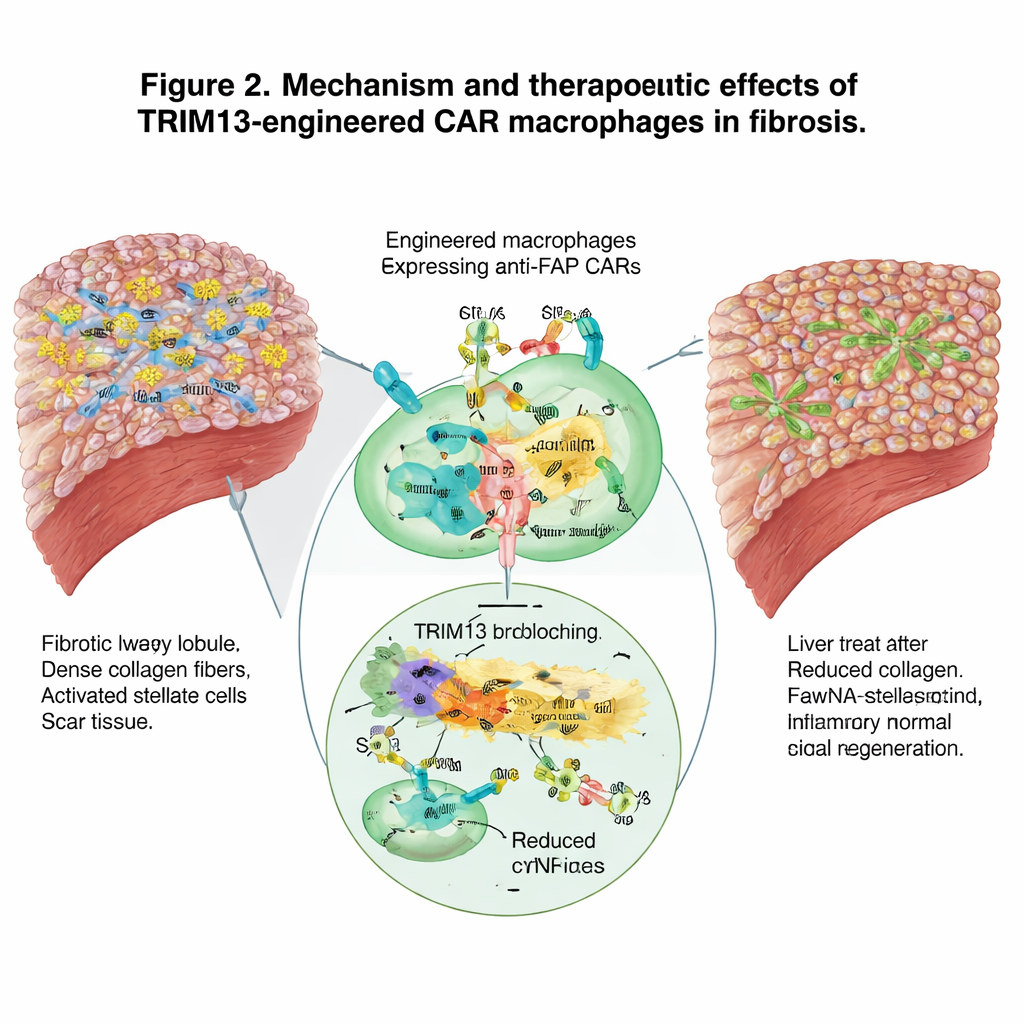
Mobilisering av det bredare immunsystemet
Förutom direkt ärrborttagning omformade de ingenjörade makrofagerna det bredare immunsystemets landskap. De skiftade från en aggressiv, skadefrämjande profil till en mer lösande, läkande sådan och minskade inflammatoriska signaler i blodet. Samtidigt, genom att förtära ärrbildande celler, verkade de fungera som lärare för det adaptiva immunsystemet genom att dra till sig neutrofiler, dendritiska celler och T‑celler och uppmuntra ett samordnat svar mot den fibrotiska vävnaden. Enkelcells‑RNA‑sekvensering av leverns immunceller bekräftade en förskjutning bort från proinflammatoriska genprogram och mot en ökad kapacitet för att omsluta och rensa skadliga celler och skräp.
Vad detta kan innebära för patienter
För en allmän läsare är slutsatsen att detta arbete pekar på ett sätt att ”omskola” leverns egna städande celler så att de både demonterar ärrvävnad och stänger av de kroniska larmsignaler som upprätthåller skadan. Genom att använda kortlivade mRNA‑instruktioner förpackade i smarta nanopartiklar undviker terapin att permanent förändra celler och begränsar aktiviteten till sjuka regioner, vilket kan minska biverkningar. Mycket mer testning krävs innan detta kan prövas på människor, men strategin utgör en lovande ritning för att behandla leverfibros — och potentiellt andra fibrotiska sjukdomar — genom att vända kroppens eget immunsystem från en drivkraft för ärrbildning till en aktiv partner i läkning.
Citering: Gao, J., Yang, Z., Song, Y. et al. TRIM13 in situ engineering boosts anti-inflammatory capacity of CAR-Ms for liver fibrosis therapy. Nat Commun 17, 2077 (2026). https://doi.org/10.1038/s41467-026-69858-3
Nyckelord: leverfibros, makrofagterapi, nanopartikel mRNA‑leverans, chimerisk antigenreceptor, TRIM13 STING‑väg