Clear Sky Science · sv
Radiomärkning av oligopeptider genom selektiv väteisotoputbyte med deuterium och tritium i vattenbuffertar
Spåra läkemedel på atomnivå
Moderna läkemedel innehåller allt oftare komplexa biologiska molekyler som peptider och små proteiner. För att förstå vart dessa läkemedel tar vägen i kroppen och hur länge de kvarstår byter forskare ofta ut ett par vanliga atomer mot sällsynta eller radioaktiva varianter som kan spåras. Denna artikel presenterar ett sätt att ”tagga” peptidläkemedel med sådana spårbara atomer direkt i vattenbaserade lösningar, mycket närmare riktiga biologiska förhållanden än de flesta tidigare metoder.
Varför små atombyten spelar roll
Att ersätta vanligt väte med tyngre former som deuterium eller tritium förvandlar vardagliga molekyler till kraftfulla vetenskapliga spårämnen. Dessa märkta varianter beter sig nästan som det ursprungliga läkemedlet men kan följas med känsliga instrument som detekterar massa eller strålning. För små läkemedelsmolekyler finns idag ett stort verktygslåda för att framställa sådana märkta föreningar. Däremot är metoderna för att märka större, känsliga biologiska molekyler—som peptider och proteiner—sparsamma, ofta komplicerade och illa lämpade för vattenbaserade miljöer som liknar blod eller cellvätskor. Författarna ville åtgärda detta gap: en enkel, selektiv metod för att införa deuterium eller tritium i peptidbyggstenar direkt i vattenbuffertar.
En enstegs märkningsstrategi i vatten
Gruppen koncentrerade sig på en typ av reaktion som kallas väteisotoputbyte, där en väteatom i en molekyl byts mot sin tyngre motsvarighet från en gas som deuterium (D2) eller tritium (T2). De byggde en in situ-katalys baserad på iridium och ett noggrant utvalt fosfinhjälpmedel. När detta blandas i en svagt basisk buffert och värms aktiverar systemet specifika kol–vätebindningar på aminosyror och små peptider och ersätter dessa väten med deuterium eller tritium från gasen. Viktigt är att detta sker i ett enda steg, i vattenrika medier och med mycket låga metallmängder—förhållanden som är vänligare mot känsliga peptidläkemedel och mer praktiska i laboratoriet. 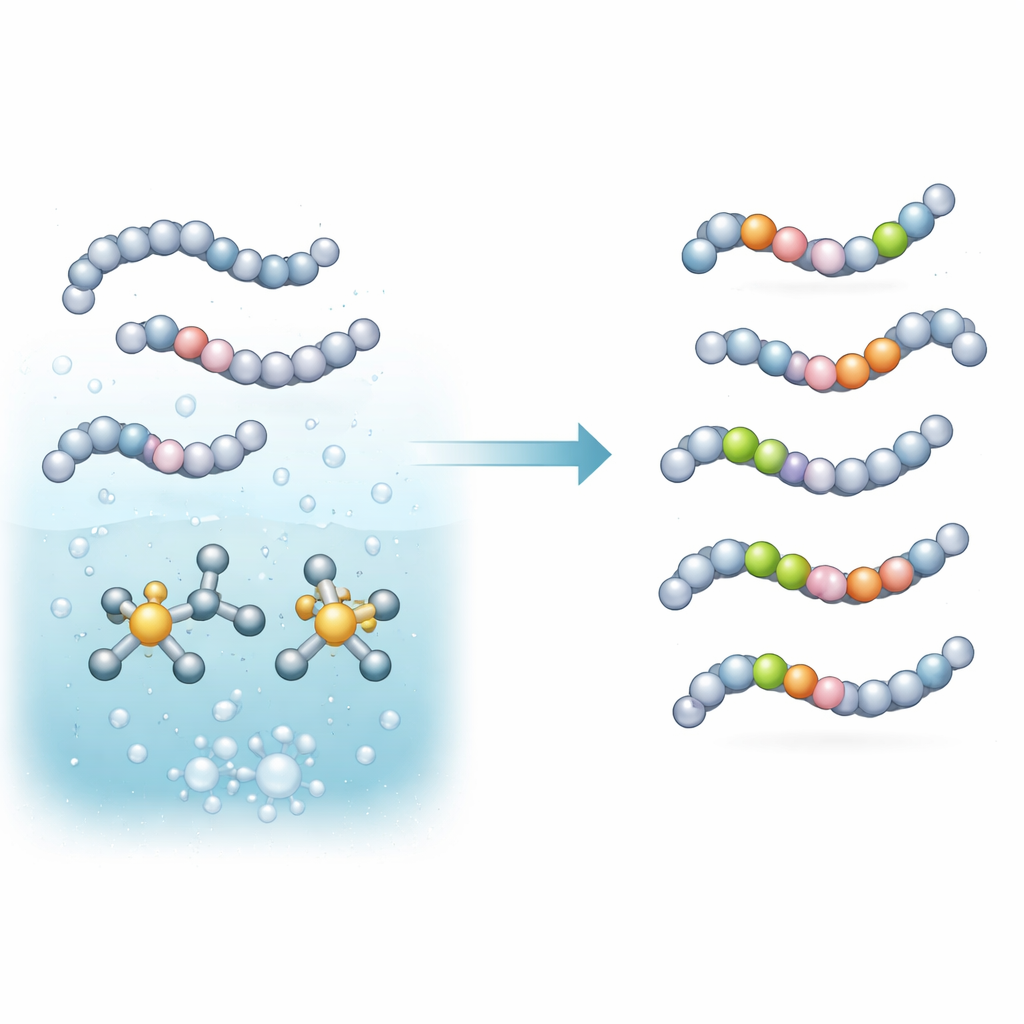
Välja precis rätt platser på peptiderna
Inte varje väteatom i en peptid är lika användbar som märkning. Vissa förloras lätt vid metabolism, vilket skulle utplåna den radioaktiva taggen. Författarna undersökte noggrant var deras katalys föredrar att verka. De upptäckte att skyddade fria aminosyror såsom lysin och arginin är särskilt väl lämpade. I lysin märker metoden selektivt en kolatom i sidokedjan (den så kallade gamma-positionen), en plats som anses ”icke-aktiverad” och mer sannolikt stabil i kroppen. Arginin uppvisar liknande beteende vid närliggande positioner i sin sidokedja. Genom att testa en serie närbesläktade molekyler, inklusive korta kedjor med två aminogrupper, fann teamet att två kväveplatser placerade på rätt sätt hjälper metallen att klämma fast molekylen och nå den målade kol–vätebindningen.
Ta en titt under katalysatorns huva
För att förstå varför denna selektivitet uppstår kombinerade forskarna experiment med detaljerade beräkningar med densitetsfunktionalteori. Dessa beräkningar kartlägger energilandskapet när iridiumkomplexet bildas från ett dimeriskt utgångsmaterial, binder vatten, sedan aminosyran och slutligen insertar i en specifik kol–vätebindning. Modellerna visar att brytningen av den ursprungliga iridiumdimeren är energimässigt möjlig i vatten för en typ av prekursor men inte för en nära besläktad, vilket förklarar varför endast vissa startkomplex är effektiva. De visar också att substratet självt hjälper till att stabilisera den aktiva metallcentra och förhindra att det klumpar ihop sig till inaktiva partiklar. Den mest gynnsamma vägen involverar att aminosyran binder via två kväveatomer och bildar ett ”pincettliknande” grepp som placerar en enskild kol–vätebindning för utbyte med deuterium eller tritium.
Från enkla byggstenar till verkliga peptidläkemedel
Med mekanismen klar utvidgade teamet metoden från enskilda aminosyror till korta peptider med upp till sju rester och därefter till mer komplexa terapeutiska sekvenser med så många som 13 aminosyror. I samtliga fall skedde märkningen i sidokedjorna av lysin eller arginin i peptidens ände, och peptiderna förblev i stort sett intakta under reaktionsförhållandena. För tritium optimerade de reaktionen vid låga gastryck för att säkert uppnå höga specifika aktiviteter, vilket innebär att en stor andel molekyler bär åtminstone en tritiumatom. Dessa tritiummärkta peptider producerades i en enda behållare och är redo att användas som spårämnen i in vitro- och potentiellt in vivo-studier. 
Vad detta innebär för framtidens läkemedel
Detta arbete visar att det är möjligt att selektivt fästa deuterium eller tritium på realistiska peptidläkemedel i ett enkelt, vattenbaserat steg samtidigt som man riktar in sig på metabolt robusta positioner på nyckelaminosyror. För läkemedelsutvecklare innebär det lättare tillgång till precist märkta spårversioner av peptidterapier, vilka är avgörande för att mäta absorption, distribution och metabolism. Utöver spårproduktion kan de mekanistiska insikterna i hur iridiumkatalysatorn interagerar med aminosyror inspirera nya sätt att finjustera var och hur komplexa biomolekyler modifieras, vilket öppnar dörrar för mer exakt kemisk kontroll över framtida biologiska läkemedel.
Citering: Martinelli, E., Weck, R., Güssregen, S. et al. Radiolabeling of oligopeptides by selective hydrogen isotope exchange with deuterium and tritium in aqueous buffers. Nat Commun 17, 2317 (2026). https://doi.org/10.1038/s41467-026-69850-x
Nyckelord: radiomärkta peptider, väteisotoputbyte, deuterium- och tritiummärkning, peptidterapeutika, iridiumkatalys