Clear Sky Science · sv
Cholecystokinin från betaceller driver utvecklingen av pankreasadenokarcinom kopplat till fetma
När extra vikt talar med bukspottkörteln
Det är väl etablerat att fetma ökar risken för pankreascancer, en av de dödligaste cancerformerna, men den biologiska ”konversation” som kopplar kroppsfett till tumörer har varit oklar. Denna studie avslöjar en oväntad budbärare: ett matsmältningshormon kallat cholecystokinin, eller CCK, som produceras inne i de insulinproducerande cellerna i bukspottkörteln. Genom att följa hur dessa celler förändras vid metabolisk stress visar författarna hur ett hormon som ska hjälpa kroppen att hantera belastning i stället kan driva cancer, och de föreslår nya sätt att avbryta sjukdomen innan den tar fäste.
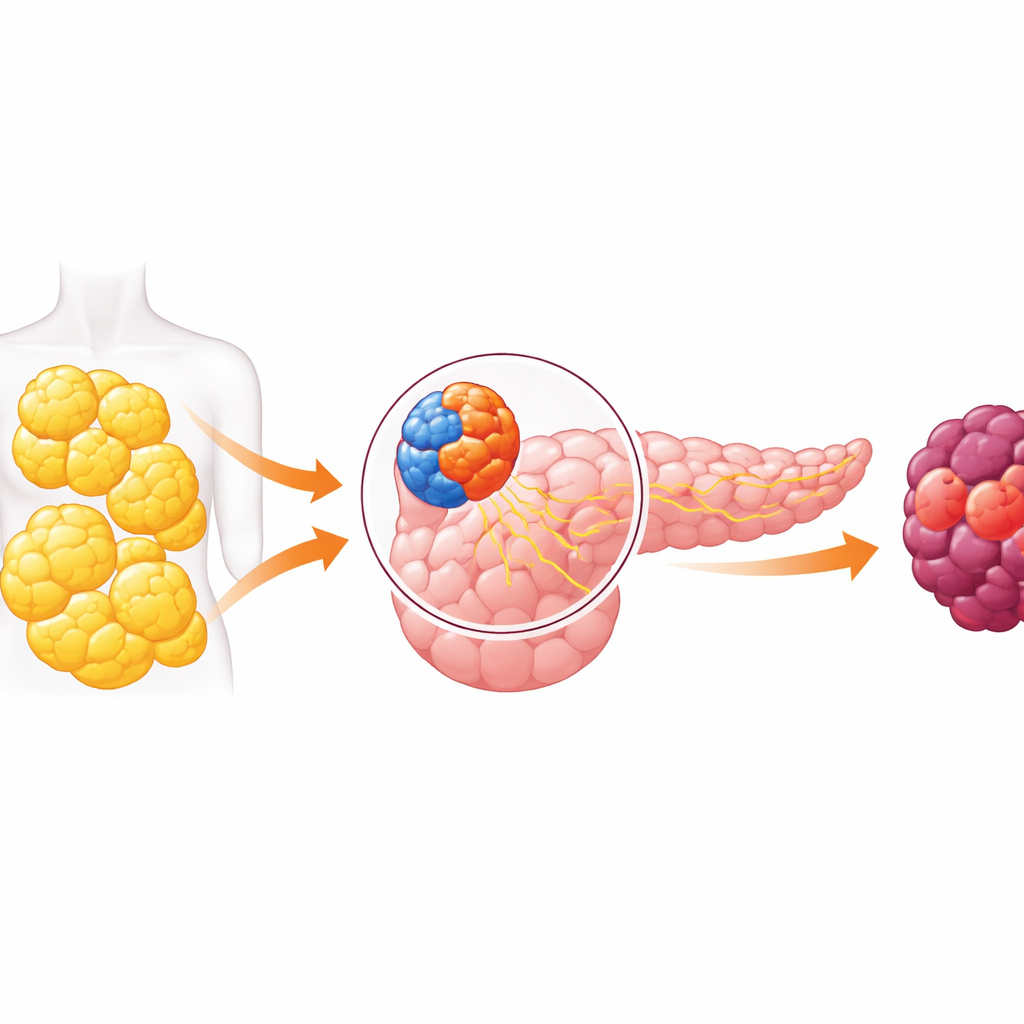
Ett tvåsidigt organ och en farlig dialog
Bukspottkörteln har två huvuduppgifter. Den ena sidan, den endokrina delen, innehåller små öar av celler som frigör hormoner som insulin för att kontrollera blodsockret. Den andra, den exokrina delen, tillverkar matsmältningsvätskor och inkluderar de celler som oftast ger upphov till pankreascancer. Under lång tid antog forskare att dessa avdelningar i stort sett fungerade isolerat. Nyare arbete har kullkastat den idén och visat att signaler från hormonproducerande celler kan påverka intilliggande matsmältningsceller. Denna artikel fördjupar sig i det samspelet och finner att det vid fetma kan driva den exokrina delen av pankreas mot cancer.
Stress i hormonproducerande celler tänder en ny signal
Vid fetma utsätts de insulinproducerande betacellerna för ett konstant tryck att möta kroppens ökade behov av insulin. Med hjälp av enkelcells-RNA-sekvensering och avancerade beräkningsverktyg följde forskarna enskilda betaceller när möss gick från magra till överviktiga och vidare till svåragradigt feta. De fann att en undergrupp av omogna betaceller expanderade och gradvis förlorade sin specialiserade insulinidentitet. När dessa celler blev stressade ökade markörer för proteinviktningsstress och cellskada medan insulinproduktionen sjönk. Samtidigt började dessa celler producera höga nivåer av CCK, ett hormon som vanligtvis förknippas med tarmarna och som kan stimulera matsmältningsceller att växa och förändras.
Från hjälpsamt hormon till cancerbränsle
För att undersöka om den nyproducerade CCK bara var en biprodukt av stress eller en aktiv sjukdomsdrivare konstruerade teamet möss vars betaceller producerade extra CCK, även utan fetma. Dessa djur utvecklade pankreasprekancer och invasiva tumörer i liknande utsträckning som feta möss, trots normal kroppsvikt och blodsocker. I kontrast, när CCK specifikt togs bort från pankreas hos feta möss minskade tumörbördan kraftigt, även om djuren fortfarande var tunga och hade höga insulinnivåer. I flera olika musmodeller följde CCK-nivåerna i pankreas tätt med tumörmängden, medan insulinnivåerna tenderade att röra sig i motsatt riktning. Det pekade mot CCK — inte insulin — som det dominerande hormonet som kopplar fetma till pankreascancer i dessa system.
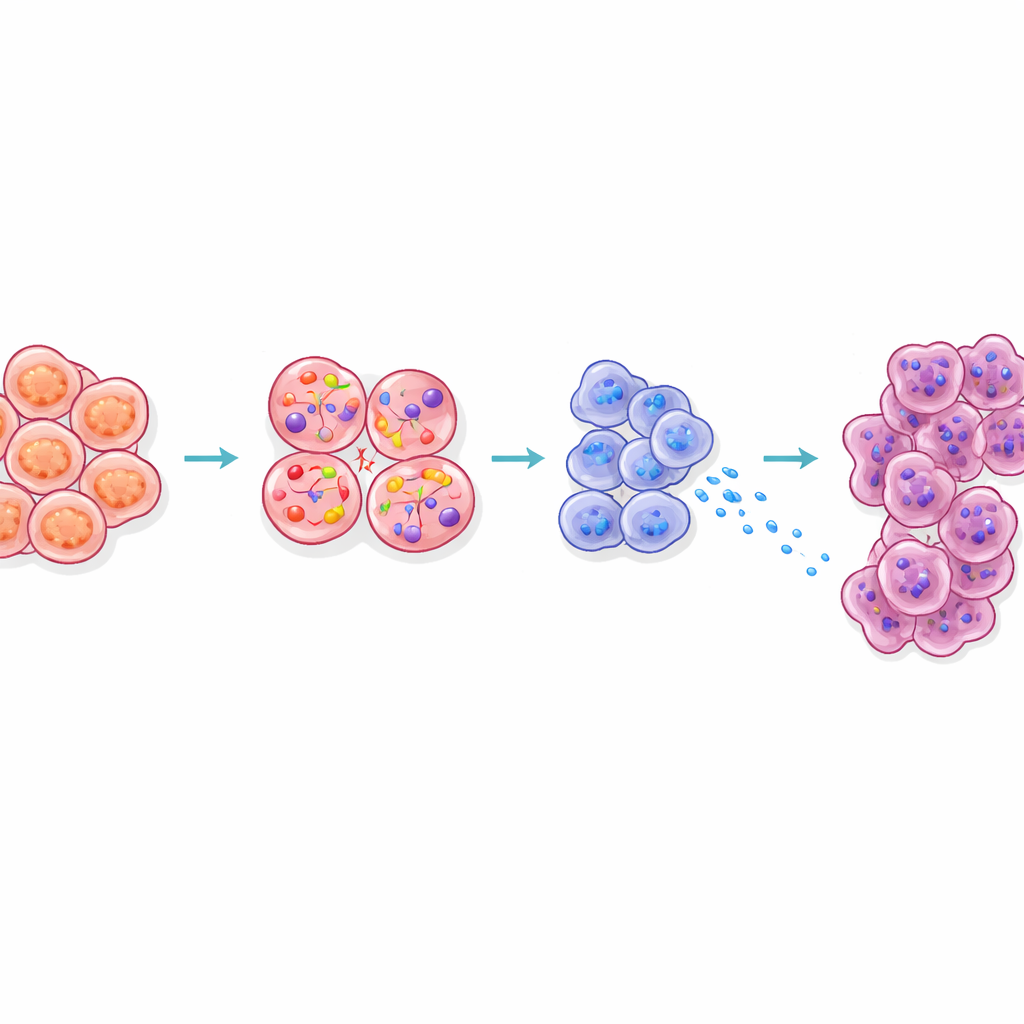
Hur signalen når och förbereder intilliggande celler
Studien undersökte också hur CCK från betaceller omformar den omgivande vävnaden. Acinära celler, som normalt utsöndrar matsmältningsenzymer, ligger tätt intill öarna i pankreas. Hos feta möss visade acinära celler nära öarna en stressprofil, producerade fler matsmältningsenzymer och proteiner kallade Reg, och gick över i tillstånd som är kända för att lättare omvandlas till cancer. Blockering av CCK-signalering hos feta möss minskade dessa Reg-signaler. Tredimensionell avbildning visade dessutom att tidiga prekancerösa lesioner tenderade att uppstå ovanligt nära öarna hos feta djur. Tillsammans tyder dessa resultat på att CCK som diffunderar från stressade betaceller skapar en ”het zon” runt öarna där matsmältningsceller är förberedda att bli tumörer.
Delade mönster med mänsklig diabetes och en nyckelbrytpunkt
Genom att jämföra musdata med mänsklig pankreasvävnad från personer med och utan typ 2-diabetes fann författarna slående paralleller: betaceller från diabetiska donatorer kartlade till samma stressade, mindre mogna tillstånd som sågs hos feta möss. De använde sedan en regulatorisk analys för att fråga vad som slår på CCK i betaceller och identifierade en stressresponsiv väg centrerad på proteinet cJun. När de blockerade den uppströms JNK–cJun-vägen hos feta möss eller i betaliknande celler i odling, sjönk CCK-nivåerna, och cJun kunde ses binda nära en regulatorisk region av CCK-genen. Detta tyder på att kronisk stress aktiverar JNK–cJun, vilket i sin tur växlar betaceller till ett CCK-producerande läge.
Vad detta betyder för personer i riskzonen
För en lekman är huvudbudskapet att insulinproducerande celler i pankreas under belastning av fetma och diabetes inte bara sveks — de anpassar sig på ett sätt som ofrivilligt uppmuntrar intilliggande celler att bilda cancer. De gör detta genom att slå på CCK, ett hormon som fungerar som en tillväxt- och stressignal för närliggande matsmältningsceller och därigenom skapar en bördig mark för tumörer. Eftersom CCK från pankreas inte är nödvändigt för att upprätthålla blodsockerkontrollen skulle riktade insatser mot denna specifika hormonkälla eller dess stressaktiverade brytpunkt i princip kunna minska risken för pankreascancer hos personer med fetma eller typ 2-diabetes utan att rubba den övergripande hormonbalansen. Arbetet omformulerar pankreascancer som en sjukdom av felaktig kommunikation mellan organets två sidor och lyfter fram nya möjligheter för tidig förebyggande åtgärd.
Citering: Garcia, C.C., Venkat, A., McQuaid, D.C. et al. Beta cell-derived cholecystokinin drives obesity-associated pancreatic adenocarcinoma development. Nat Commun 17, 3292 (2026). https://doi.org/10.1038/s41467-026-69821-2
Nyckelord: pankreascancer, fetma, betaceller, cholecystokinin, typ 2-diabetes