Clear Sky Science · sv
Sammansatt SMG5–SMG6 PIN-domänbildning är avgörande för NMD
Hur celler skyddar sig mot felaktiga budskap
Våra celler läser ständigt genetiska budskap (mRNA) för att tillverka proteiner. Men dessa budskap kan ibland innehålla tidiga stoppkoder som skulle ge upphov till förkortade, potentiellt skadliga proteiner. Processen som förstör sådana felaktiga budskap kallas nonsense‑medierad mRNA‑nedbrytning (NMD). Den här artikeln visar hur två nyckelproteiner, SMG5 och SMG6, fysiskt samarbetar för att klyva defekta budskap och förklarar ett länge olöst mysterium i hur cellulär kvalitetskontroll fungerar.
Att hitta det dolda samarbetet
I många år har forskare vetat att SMG6 kan klyva RNA direkt, medan SMG5 betraktats som ”katalytiskt dött” och främst en hjälpare eller stomme. Ändå visade experiment i celler något gåtfullt: SMG6 kunde inte fungera korrekt utan SMG5, och NMD kollapsade om någon av dem saknades. Författarna använde toppmodern strukturprediktion (AlphaFold), biokemiska analyser med renade proteiner och genetiska tester i humana cellinjer för att lösa denna motsats. Deras modeller förutsade att svansregionerna hos SMG5 och SMG6, kallade PIN‑domäner, lägger sig intill varandra för att bilda en gemensam struktur. Denna sammansatta enhet — kallad en ”cPIN” — föreslogs vara den verkliga klyvmaskinen i NMD. 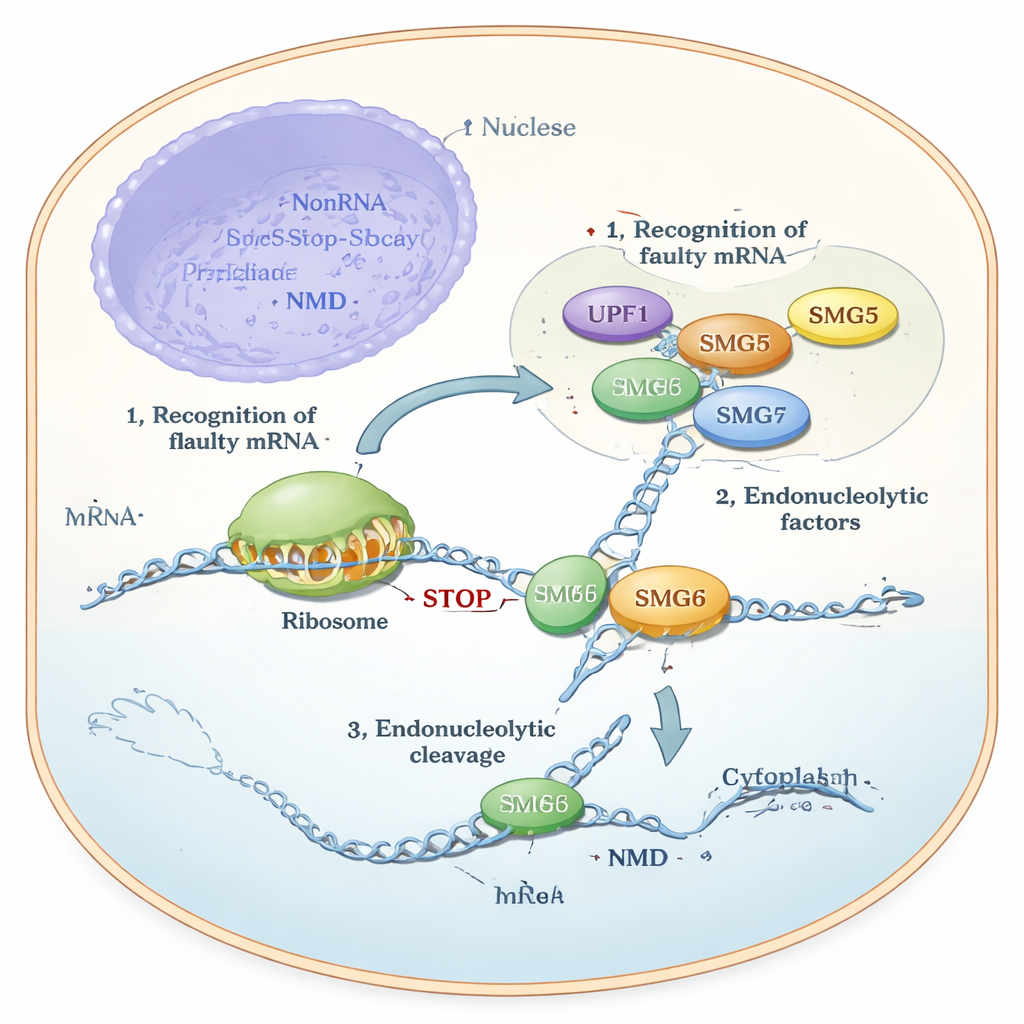
Återskapa de molekylära saxarna i provröret
För att testa förutsägelsen producerade teamet fragment av humana SMG5 och SMG6 i bakterier och renade dem. Var för sig visade SMG6 endast svag förmåga att klyva ett designat RNA‑substrat, och SMG5 ensam visade praktiskt taget ingen aktivitet. Men när de två fragmenten blandades ökade klyvningsaktiviteten markant, även under förhållanden där förorenande enzymer sannolikt inte spelade någon roll. Samma effekt sågs på både linjära och cirkulära RNA‑baserade testmolekyler, vilket indikerar att den förbättrade klyvningen verkligen kom från SMG5–SMG6‑paret. Kemisk tvärbindning och masspektrometri visade dessutom att de två proteinerna kommer i nära kontakt, vilket stöder idén om ett direkt, om än övergående, samarbete.
Fullända det skärande bladet
Strukturmodellerna föreslog exakt hur SMG5 stärker SMG6. SMG6 bidrar med fyra sura aminosyror som håller metalljoner i själva klyvningsstället, vilket är typiskt för denna enzymfamilj. Överraskande placerade modellerna en ytterligare sur rest från SMG5 precis intill dessa, vilket i praktiken förlängde den katalytiska fickan. Andra positivt laddade rester på SMG5 förutsades greppa RNA‑ryggraden och hjälpa till att positionera den för klyvning. När forskarna muterade dessa kritiska rester i SMG5 eller SMG6 förlorade den sammansatta komplexet mycket av sin klyvningsförmåga in vitro. Samma mutationer kunde inte heller återställa NMD i konstruerade humana celler där det normala proteinet hade uttömts, vilket knöt den strukturella modellen tätt till verklig cellulär funktion. 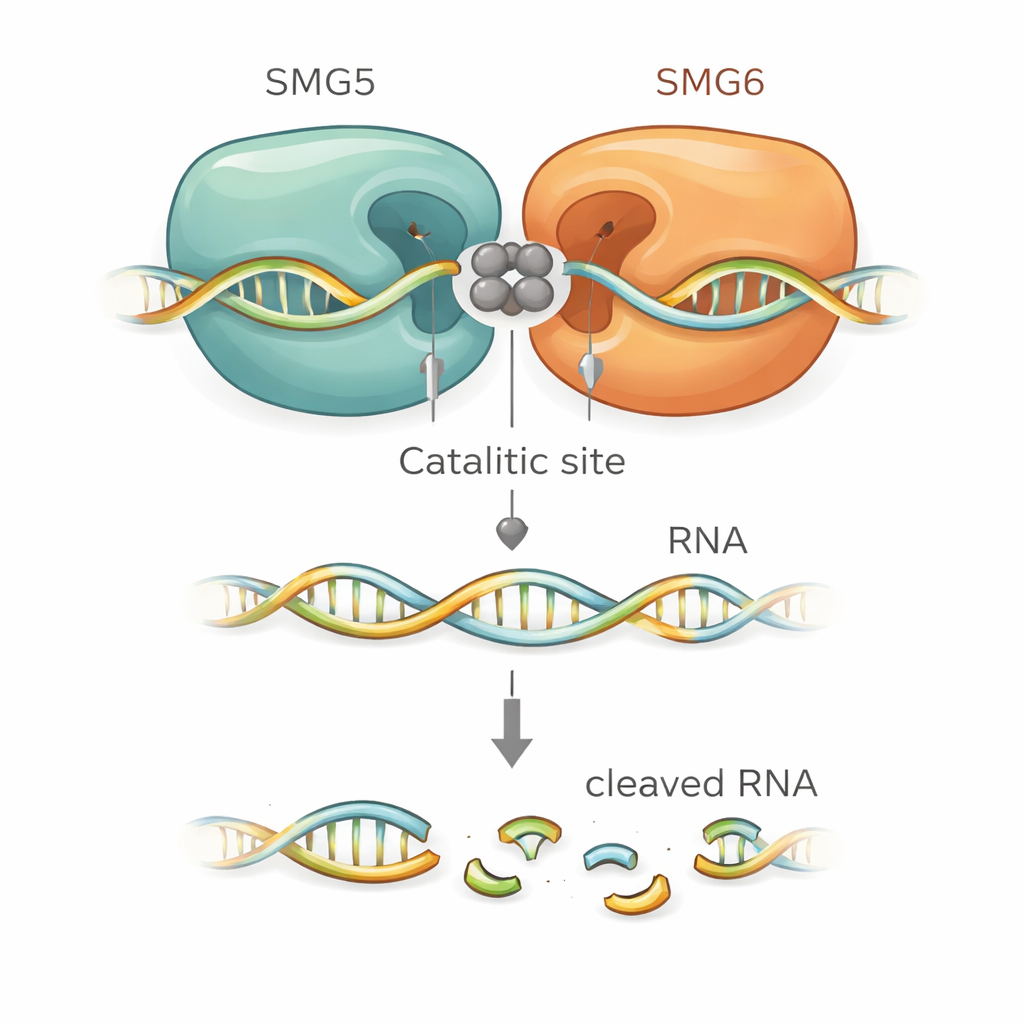
Bevisa att båda parter är väsentliga i celler
Då fullständigt borttagande av SMG5 eller SMG6 dödar celler använde teamet ett ”degron”‑system som låter dem märka varje protein så att det snabbt kan förstöras med ett litet molekylärt medel. Genom att kombinera denna snabba nedbrytning med RNA‑interferens uppnådde de nästan total borttagning av SMG5, SMG6 eller en central regulator kallad UPF1. Genom att sekvensera RNA i hela genomet kunde de sedan se vad som händer med NMD när varje faktor försvinner. Uttömning av SMG5 eller UPF1 gav nästan identiska förändringar i cellulära RNA, med felaktiga, NMD‑känsliga transkript som ackumulerades kraftigt. Borttagning av SMG6 gav en mycket liknande, om än något mildare, effekt. Dessa data visar att SMG5 och SMG6 inte är valfria parallella grenar i vägen; de verkar tillsammans med UPF1 som kärnkomponenter i en huvudväg för nedbrytning.
Varför detta är viktigt för cellhälsa
Förenklat visar studien att SMG5 och SMG6 klickar ihop för att bilda ett enda, kraftfullt molekylärt saxpar som skär sönder defekta genetiska budskap. SMG6 utgör största delen av bladet, men SMG5 bidrar med en saknad egg och hjälper till att hålla RNA på plats, vilket förvandlar en svag klyvare till en effektiv sådan. Denna sammansatta ”cPIN” förklarar varför celler absolut behöver båda proteinerna för att hålla sina RNA‑budskap rena. Genom att klargöra hur NMD:s viktiga klyvsteg aktiveras först när felaktiga budskap känns igen, ger arbetet en tydligare bild av hur celler förhindrar ansamling av toxiska, förkortade proteiner och finjusterar genuttrycket.
Citering: Kurscheidt, K., Theunissen, S., Pasquali, N. et al. Composite SMG5-SMG6 PIN domain formation is essential for NMD. Nat Commun 17, 1934 (2026). https://doi.org/10.1038/s41467-026-69819-w
Nyckelord: nonsense‑medierad mRNA‑nedbrytning, RNA‑kvalitetskontroll, SMG5 SMG6, mRNA‑övervakning, reglering av genuttryck