Clear Sky Science · sv
Icke‑hydrolyserbara acetyllysinanaloger för att studera proteinacetylering in vitro och i celler
Varför små kemiska märken på proteiner spelar roll
Inne i varje cell förses proteiner ständigt med små kemiska märken som fungerar som av‑/på‑knappar eller dimrar för deras aktivitet. En av de viktigaste av dessa märkningar kallas acetylering, vilket kan ändra hur ett protein beter sig utan att förändra dess genetiska kod. Att förstå exakt vad acetylering gör på en specifik plats på ett specifikt protein har visat sig vara förvånansvärt svårt, eftersom celler kan ta bort dessa märken lika snabbt som de sätter dit dem. I den här studien presenteras en smart kemisk "vikarie" för acetylering som inte kan tas bort, vilket ger forskare ett sätt att frysa dessa avstängningsmekanismer på plats och se vad som händer.
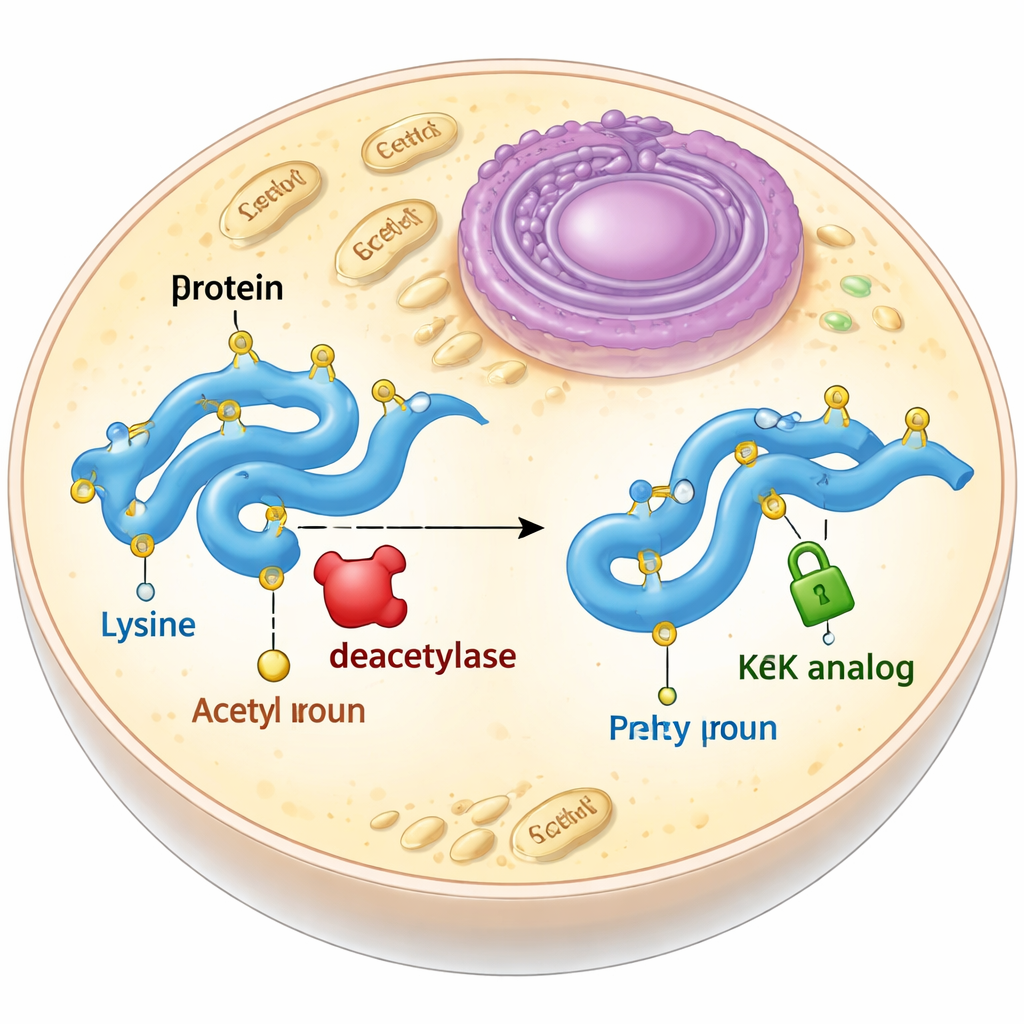
En stabil vikarie för ett flyktigt märke
Acetylering sker vanligtvis på en byggsten i proteiner kallad lycin. När en lycin acetyleras förlorar den sin positiva laddning och dess sidokedja blir något längre. Biologer försöker ofta efterlikna detta genom att mutera lycin till en annan aminosyra, glutamin, som är oladdad men kortare, eller genom att tillsätta riktig acetyllysin med hjälp av en utvidgad genetisk kod. Båda tillvägagångssätten har nackdelar: glutamin återger inte fullt ut de formförändringar som acetylering orsakar, och riktig acetyllysin avlägsnas snabbt av enzymer som kallas deacetyleraser inne i celler. Författarna gav sig därför i kast med att designa och testa acetyllysin‑liknande molekyler som behåller rätt storlek och form men inte kan tas bort.
Test av nya kemiska mimetika på ett modellprotein
Teamet koncentrerade sig först på ubiquitin, ett litet, välstuderat protein som själv pryds med många olika märkningar. Med avancerad genetisk ingenjörskonst placerade de olika lycinvarianter på en position i ubiquitin: naturlig acetyllysin, två icke‑avtagbara analoger kallade TFAcK och ketolycin (KeK), samt vanliga substitut som glutamin, alanin och arginin. De undersökte sedan hur dessa förändringar påverkade ubiquitins form och funktion. Högupplösta NMR‑mätningar visade att acetyllysin, TFAcK och KeK alla gav nästan identiska strukturella förändringar, särskilt runt en central helix, medan glutamin och andra enkla mutationer inte gjorde det. Funktionella tester med enzymet HDM2 visade att ubiquitin som bar acetyllysin, TFAcK eller KeK uppträdde likartat och annorlunda jämfört med glutaminvarianten, vilket understryker att sidokedjans längd och volym — inte bara dess laddning — är avgörande.
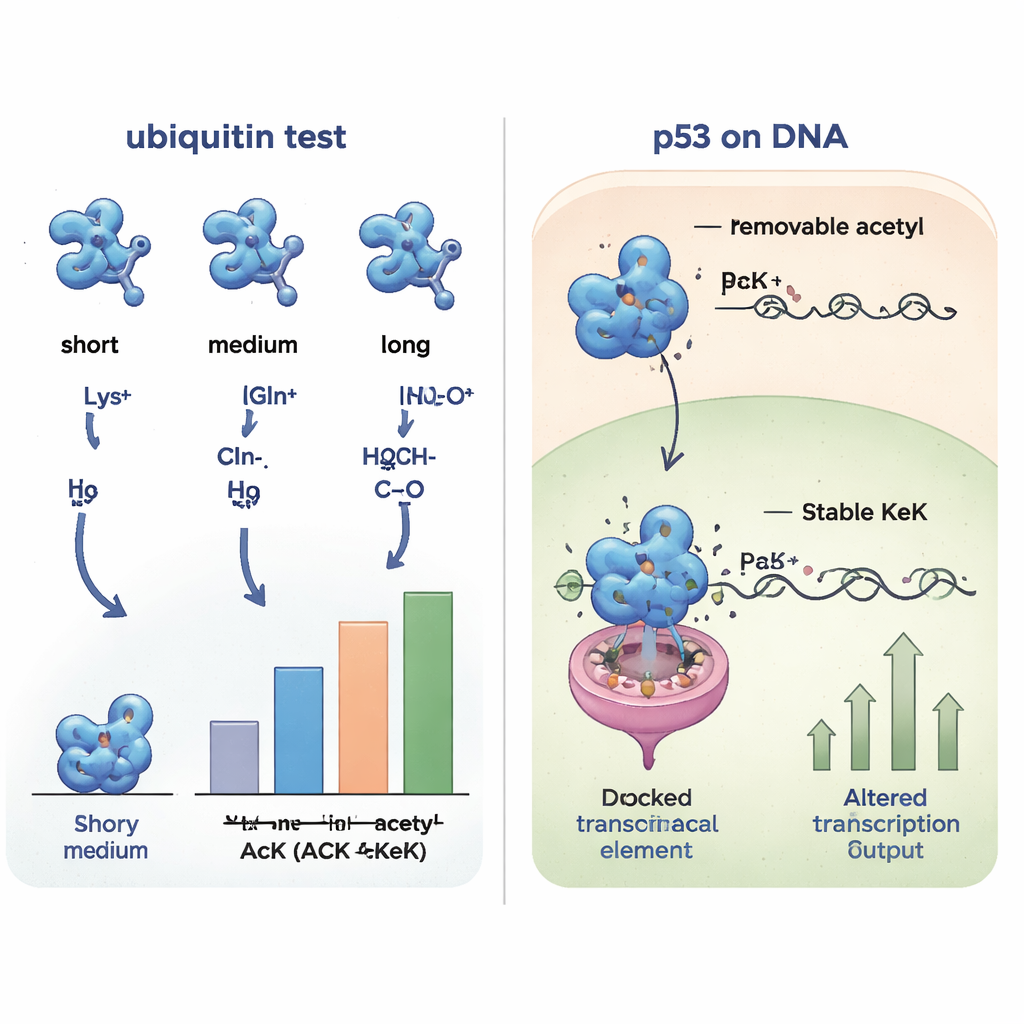
Undersöka proteinpartnerskap över hela cellen
Då små strukturella förändringar kan påverka vilka partners ett protein interagerar med jämförde forskarna nästa hur de olika ubiquitinversionerna band till andra proteiner från humana cellextrakt. Genom att fiska upp bindande partner och identifiera dem med masspektrometri fann de att ubiquitin som innehöll acetyllysin, TFAcK eller KeK delade mycket lika interaktionsmönster, medan former som innehöll glutamin eller alanin bildade en egen kluster och såg annorlunda ut. Positivt laddade varianter (lysin eller arginin) bildade ännu en grupp. Denna systematiska jämförelse visade att de icke‑avtagbara analogerna TFAcK och särskilt KeK efterliknar både strukturen och bindningsbeteendet hos riktig acetylering mycket bättre än den traditionella glutaminsubstitutionen.
Låsa fast acetylering på tumörsuppressorn p53
För att se om dessa verktyg fungerar inne i levande celler vände sig författarna till p53, en central tumörsuppressor ofta kallad "genomets väktare." Specifika lysiner i p53:s DNA‑bindande region kan acetyleras och därigenom ändra vilka gener den aktiverar, exempelvis de som stoppar cellcykeln eller utlöser celldöd. Teamet konstruerade humana celler så att p53 skulle införliva acetyllysin, TFAcK eller KeK vid två viktiga lysinpositioner (120 och 164) endast när motsvarande icke‑standardaminosyra tillsattes. Alla tre kunde byggas in i p53, men detaljerade mätningar visade att i celler togs acetyl‑ och TFAcK‑grupperna till stor del bort av deacetyleraser, medan KeK förblev intakt. När de testade p53:s förmåga att aktivera en reportergen och den naturliga p21‑genen var varianter som bar KeK på dessa platser mycket mindre aktiva, i linje med vad som förväntas när acetylering på dessa positioner är låst, medan acetyllysin och TFAcK uppträdde mer likt normalt p53 eftersom de hade blivit deacetylerade.
Vad detta betyder för att studera cellbeslut
Sammantaget visar studien att KeK är en trogen och icke‑avtagbar vikarie för acetyllysin: den reproducerar nära nog de strukturella förändringarna, bindningspreferenserna och de funktionella konsekvenserna av acetylering, men kan inte raderas av cellulära enzymer. För icke‑specialister innebär detta att forskare nu har ett sätt att "frysa" en normalt reversibel kemisk brytare på en enda plats i ett protein och sedan observera hur det påverkar processer som genreglering och cellödesbeslut. Det bör göra det mycket lättare att skilja acetyleringens specifika roller från andra överlappande modifieringar, och kan i slutändan klargöra hur felreglerad proteinacetylering bidrar till sjukdomar som cancer.
Citering: Kienle, S.M., Sigg, M., Schneider, T. et al. Non-hydrolyzable acetyllysine analogs to study protein acetylation in vitro and in cells. Nat Commun 17, 1985 (2026). https://doi.org/10.1038/s41467-026-69782-6
Nyckelord: proteinacetylering, posttranslationell modifiering, ubiquitin, p53, utvidgning av den genetiska koden