Clear Sky Science · sv
Dynamisk transkriptomisk omvandling i transplanterade humana neurala progenitorceller avslöjar mekanismer för bevarande av synen i en råttmodell för retinitis pigmentosa
Varför det är viktigt att skydda försvagande syn
Retinitis pigmentosa är en grupp ärftliga sjukdomar som gradvis berövar människor synen, ofta med nattblindhet som tidigt symptom och sedan försämring mot laglig blindhet. Eftersom hundratals olika genmutationer kan ge upphov till tillståndet är det svårt att behandla varje variant med individuell genterapi. Denna studie undersöker en mer universell strategi: att transplantera humana neurala progenitorceller — omogna nervceller odlade i laboratoriet — in i ögat för att skydda de kvarvarande ljussensoriska cellerna. Att förstå exakt hur dessa transplanterade celler beter sig och hjälper till att bevara synen kan forma framtida behandlingar inte bara för retinitis pigmentosa utan även för andra blindande sjukdomar.
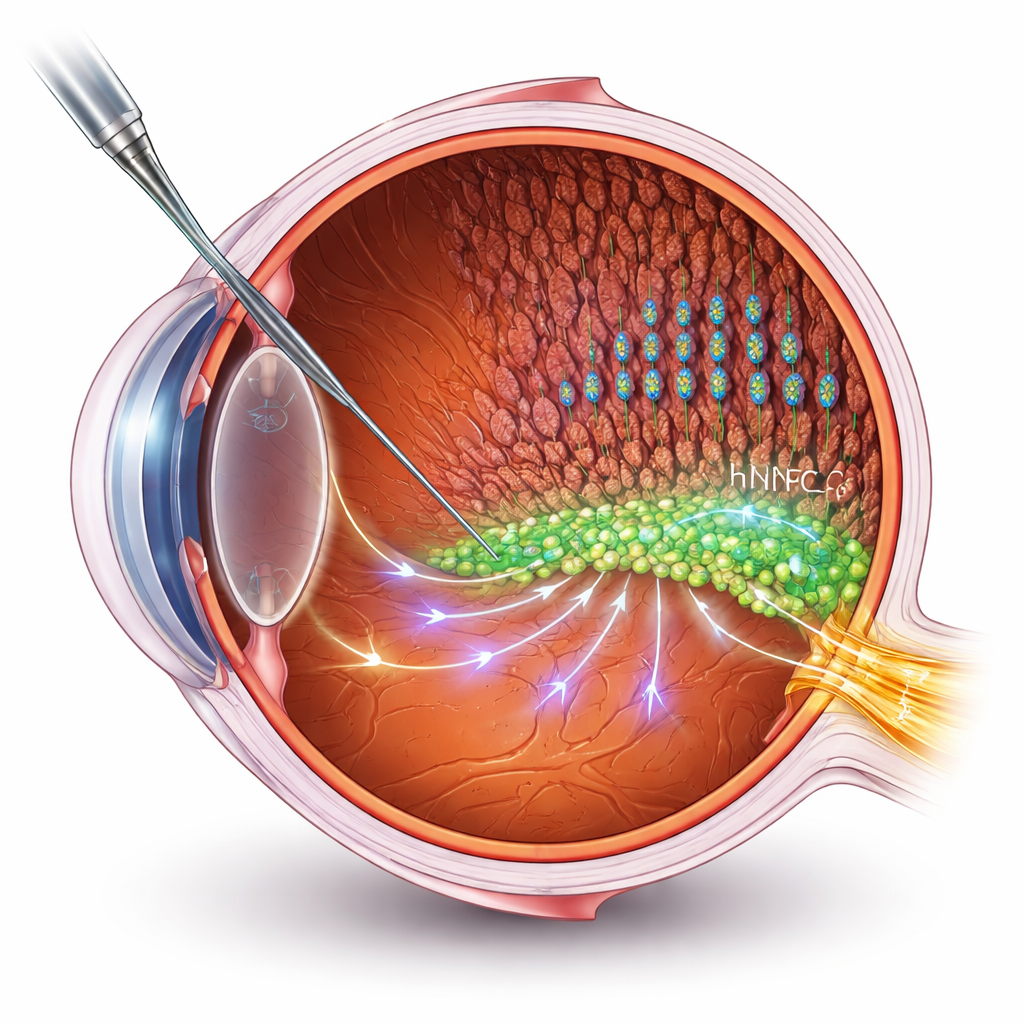
Hjälpa celler istället för att ersätta dem
Många stamcellsterapier syftar till att ersätta döda eller skadade celler. Men vid avancerade näthinnesjukdomar är det en stor teknisk utmaning att bygga nya förbindelser till hjärnan. Här tar forskarna en annan väg: de använder humana neurala progenitorceller (hNPCs) som ”hjälpare” som stödjer patientens egna näthinnoceller. De transplanterade hNPCs till subretinala rummet i en välkänd råttmodell för retinitis pigmentosa och mätte sedan synfunktion med elektriska inspelningar och beteendetester. De behandlade råttorna behöll bättre visuell funktion och mer intakta lager av fotoreceptorer — stavar och tappar som fångar ljus — än obehandlade djur, även om degenerationen fortfarande fortskred långsamt.
Hur transplanterade celler förändras inne i det sjukliga ögat
För att se vad som händer på molekylär nivå använde teamet single-cell RNA-sekvensering, en teknik som kartlägger vilka gener som är aktiva i tusentals enskilda celler. De följde de transplanterade hNPCs vid två tidpunkter, ungefär tidiga och senare stadier efter transplantation. Istället för att bli nya fotoreceptorer mognade majoriteten av de transplanterade cellerna till astrocytliknande stödjeceller, med en mindre andel som visade markörer för oligodendrocyter eller omogna neuroner. Med tiden stabiliserades dessa celler och antog egenskaper som tyder på att de är anpassade för att överleva i en stressfylld, degenererande miljö och för att interagera nära med närliggande retinala celler.
Skyddande signaler, metabolism och städning
hNPCs producerade en rik blandning av skyddande proteiner kända som trofiska faktorer. Bland dem fanns MANF och MYDGF, som kopplas till cellsöverlevnad, minskad oxidativ stress och dämpad inflammation, samt andra faktorer som midkine och pleiotrophin som stödjer tillväxt och rörelse hos nervceller. Dessa molekyler verkade agera både på transplantatet självt och på den omgivande näthinnan. I de behandlade råttorna visade stavar och tappar genuttrycksmönster som låg närmare friska kontroller, med förbättrat stöd för visuell signalering och cellunderhåll. De transplanterade cellerna förstärkte också vägar som är involverade i att rensa cellulärt skräp och att anpassa metabolismen, vilket tyder på att de hjälper fotoreceptorer att hantera energikrav och toxiska biprodukter som byggs upp under sjukdomen.
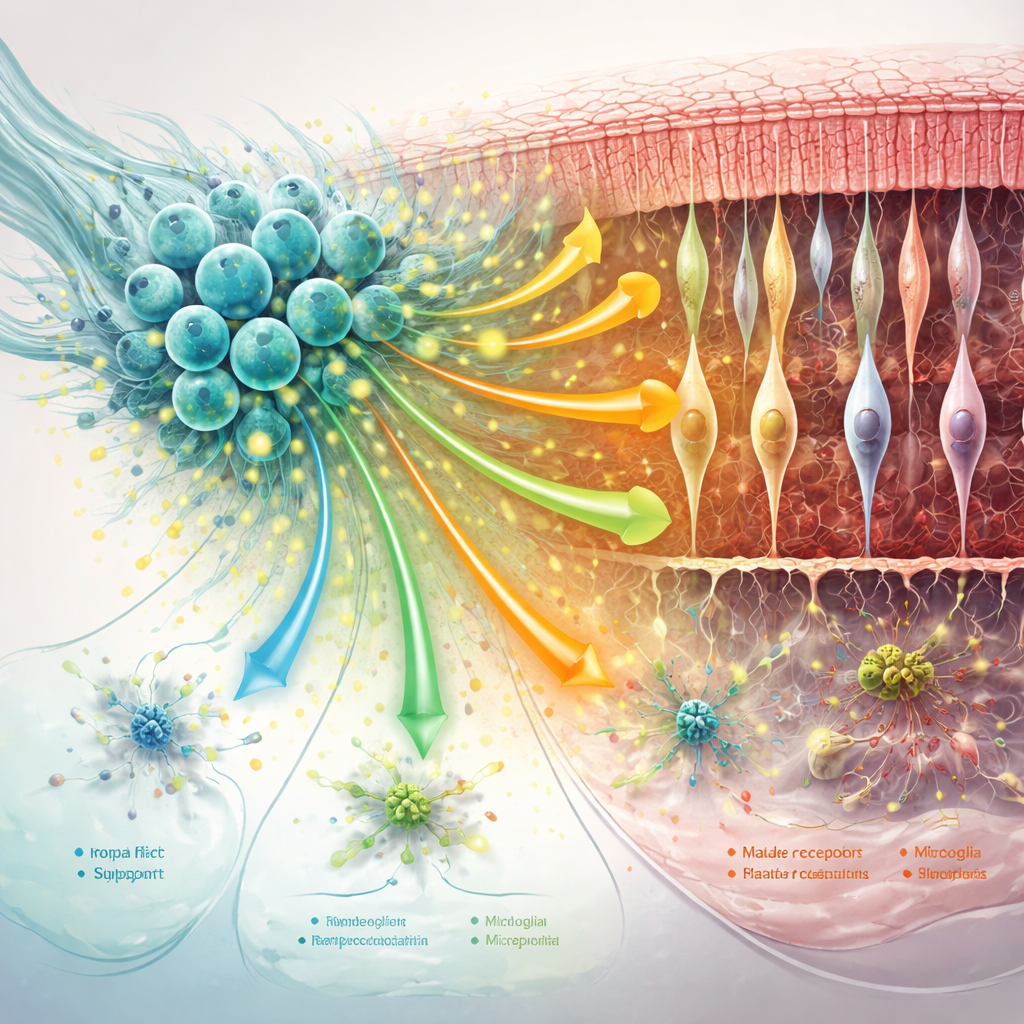
Stillande stödjeceller och omformning av retinala grannskapet
Näthinnans stödjande nätverk — Müller-celler, mikroglia och den omgivande proteinmatrisen — spelar en stor roll för att antingen förvärra eller bromsa degenerationen. Studien fann att behandling med hNPCs dämpade viktiga markörer för skadliga ”reaktiva” förändringar i Müller-celler och försköt mikroglia bort från överdrivet inflammatoriska tillstånd, särskilt vid tidigare tidpunkter. Samtidigt stärkta kommunikationssignaler som hjälper till att stabilisera synapser, hålla celler samman och bibehålla stödkonstruktionen runt fotoreceptorerna. När sjukdomen fortskred avtog några av dessa fördelar: den övergripande cell-till-cell-kommunikationen försvagades, vissa skyddande vägar — inklusive MANF-relaterad signalering — minskade, och stödjeceller antog mer stress- och immuninriktade profiler.
Vad detta innebär för framtida ögonbehandlingar
För en icke-specialist är huvudbudskapet att transplanterade humana neurala progenitorceller kan fungera som lokala ”förstainsatser” i en degenererande näthinna. De bygger inte upp näthinnan från grunden, men de frigör skyddande molekyler, justerar metabolismen, lugnar skadlig inflammation och hjälper till att bevara den lokala strukturen — allt detta bromsar synförlusten. Denna skyddande effekt avtar dock med tiden i takt med att miljön blir mer ogästvänlig och dialogen mellan transplantat och värdceller försvagas. Författarna föreslår att förstärkning av nyckelfaktorer såsom MANF och förbättring av värdretinans hälsa — möjligtvis genom genetisk modifiering av transplantatet eller kombinationsbehandlingar — kan vara nödvändigt för att omvandla en tillfällig lindring till ett långvarigt bevarande av synen.
Citering: Shahin, S., Bell, S., Lu, B. et al. Dynamic transcriptomic remodeling in grafted human neural progenitor cells uncovers mechanisms for vision preservation in a rat model of retinitis pigmentosa. Nat Commun 17, 2164 (2026). https://doi.org/10.1038/s41467-026-69776-4
Nyckelord: retinitis pigmentosa, stamcellsterapi, retinal degeneration, neuroprotection, single-cell RNA sequencing