Clear Sky Science · sv
TCL1A medierar defekter i DNA-metylering vid recidiverande hydatidiform mola med patogena varianter i NLRP7
Varför detta är viktigt för kvinnors hälsa
Vissa graviditeter går fel mycket tidigt och utvecklas till en massa onormalt moderkaksvävnad istället för ett växande foster. Denna tillstånd, kallat hydatidiform mola, kan återkomma hos vissa kvinnor och ibland utvecklas till cancer. Denna studie undersöker en huvudorsak bakom dessa sällsynta men allvarliga graviditeter och avslöjar hur en enda felaktig skyddsmekanism i ägget kan rubba de kemiska ”etiketterna” som styr normal utveckling.
En graviditetsstörning som har sin grund i ägget
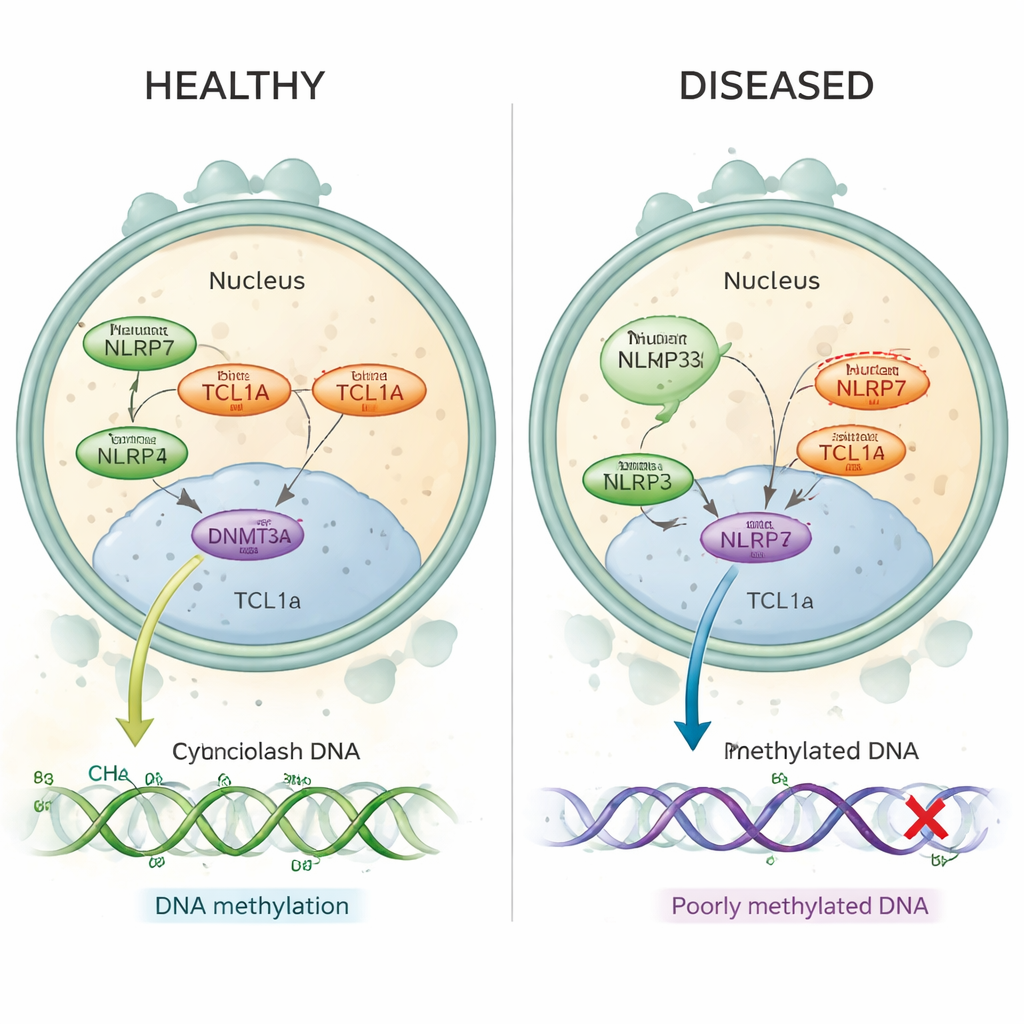
Recidiverande hydatidiform mola är en störning där kvinnor upplever upprepade molära graviditeter, ofta utan några normala graviditeter däremellan. Många sådana fall beror nu kända på skadliga förändringar i en gen som heter NLRP7, vilken är aktiv i ägget före och strax efter befruktningen. Hos dessa kvinnor saknar viktiga DNA‑regioner som borde bära moderns ”imprints” normalt metyleringsmönster — små kemiska markörer som hjälper till att slå på eller av gener vid rätt tidpunkt. Fram till nu förstod forskarna inte hur ett protein som finns i äggets cytoplasma, som NLRP7, skulle kunna kontrollera metylering som sker på DNA paketerat inne i cellkärnan.
Att hitta en saknad partner
För att lösa detta pussel undersökte forskarna kasserade mänskliga ägg och mycket tidiga embryon från fertilitetskliniker. De fångade upp NLRP7 och kända partners från dessa celler och identifierade andra proteiner som följer med. Ett stack ut: TCL1A, redan känt i blodcancer som ett protein som kan förflytta sig in i kärnan och störa DNA‑metylerande enzymer kallade DNMT3A och DNMT3B. TCL1A är ovanligt rikligt i mänskliga ägg, vilket tyder på att det spelar en viktig roll där. Detaljerade interaktionstester visade att TCL1A binder tätt och specifikt till NLRP7, men inte till närbesläktade proteiner, och att detta komplex är kopplat till en större äggspecifik struktur kallad det subkortikala maternala komplexet.
Att se det molekylära omfamningen
Teamet använde sedan kryo‑elektronmikroskopi för att visualisera den tredimensionella strukturen av NLRP7–TCL1A‑komplexet. De fann att två NLRP7‑molekyler parar ihop sig och var och en greppar ett TCL1A‑dimer längs en krökt yta av upprepade motiver. Denna uppställning förklarar varför många sjukdomsframkallande förändringar i NLRP7 klustrar längs den ytan: förändringar i nyckelkontaktpunkter försvagar eller förstör omfamningen med TCL1A. När forskarna återskapade mer än 50 kända patientvarianter i celler, destabiliserade de flesta av de versioner som är kopplade till recidiverande molära graviditeter antingen NLRP7 eller minskade dess förmåga att binda TCL1A kraftigt.
Hur felplacerade proteiner rubbar DNA‑markörer
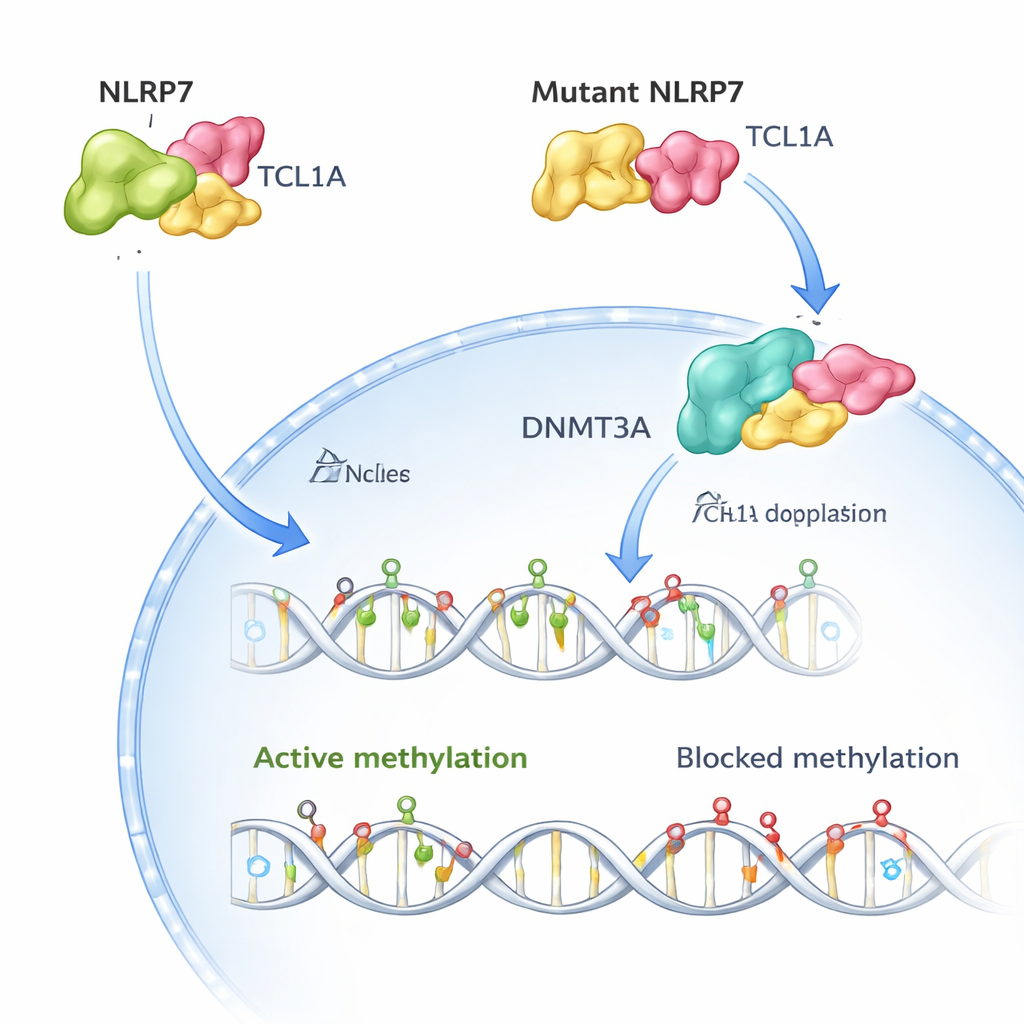
I friska mänskliga ägg finns både NLRP7 och TCL1A huvudsakligen i cytoplasman, med endast en liten mängd TCL1A som når kärnan. Författarna visar att NLRP7 effektivt fungerar som en grindvakt: när det kan hålla TCL1A stannar TCL1A utanför kärnan. När NLRP7 är muterat och inte längre kan binda väl, läcker TCL1A in i kärnan. Där fäster det vid DNMT3A, det huvudsakliga enzymet som sätter nya metyleringsmarkörer i ägg, och dämpar dess aktivitet. I stamcellsmodeller som normalt får metylering under mognad orsakade överproduktion av TCL1A en dramatisk förlust av metylering över genomet, medan samtidig uttryck av NLRP7 delvis räddade denna defekt. Tillsammans stöder dessa fynd en enkel bild: normalt håller NLRP7 en metylerings"broms" (TCL1A) låst i cytoplasman så att DNMT3A kan märka DNA korrekt; felaktigt NLRP7 låter den bromsen glida in i kärnan och blockera processen.
Från mekanism till diagnos
Utöver att förklara hur recidiverande molära graviditeter uppstår, föreslår studien ett praktiskt sätt att bedöma om en nyligen upptäckt NLRP7‑förändring hos en patient verkligen är skadlig. Författarna jämför tre tillvägagångssätt — laboratorietester av NLRP7–TCL1A‑bindning, datorbaserade prediktioner och standardverktyg för genetisk poängsättning — och visar att förlust av TCL1A‑bindning överensstämmer väl med varianter som orsakar sjukdom. De upptäcker också en tidigare oigenkänd skadlig variant, L766R, i familjer med recidiverande molor, vilket bekräftar att den både försvagar proteinet och omdirigerar TCL1A in i kärnan.
Vad detta betyder i enkla ord
Denne studie avslöjar en molekylär kedjereaktion bakom en sällsynt men förödande graviditetsstörning. I grund och botten bär ägg från drabbade kvinnor ett trasigt "livvakt"‑protein, NLRP7, som misslyckas med att hålla sin partner TCL1A utanför kärnan. När den väl kommer in stör TCL1A enzymet som skriver viktiga kemiska markörer på DNA. Utan dessa markörer växer den tidiga moderkakan onormalt och ett foster kan inte bildas. Genom att spåra denna väg steg för steg klargör studien varför vissa genetiska förändringar hos mödrar upprepade gånger kan sabotera graviditeter och pekar mot mer precist genetiskt rådgivning och diagnostik för kvinnor med recidiverande hydatidiforma molor.
Citering: Gao, Z., Liu, Q., Li, L. et al. TCL1A mediates DNA methylation defects in recurrent hydatidiform mole with NLRP7 pathogenic variants. Nat Commun 17, 2160 (2026). https://doi.org/10.1038/s41467-026-69744-y
Nyckelord: DNA-metylering, recidiverande hydatidiform mola, NLRP7, TCL1A, genomisk imprinting