Clear Sky Science · sv
GCN5 driver MASLD‑progression via LXRα/SREBP1c‑signalväg–medierad de novo‑lipogenes
Varför den här leverhistorien är viktig
Metabol dysfunktionsassocierad steatotisk leversjukdom (MASLD), tidigare kallad icke‑alkoholrelaterad fettleversjukdom, drabbar nu ungefär en av fyra människor globalt. Den utvecklas ofta tyst, men kan förvärras till ärrbildning, levercancer och allvarliga metabola komplikationer. Denna studie avslöjar en molekylär "volymknapp" som driver skadlig fettansamling i levern och visar hur en nedreglering kan skydda levern och potentiellt göra befintliga hjärt‑läkemedelsstrategier säkrare.
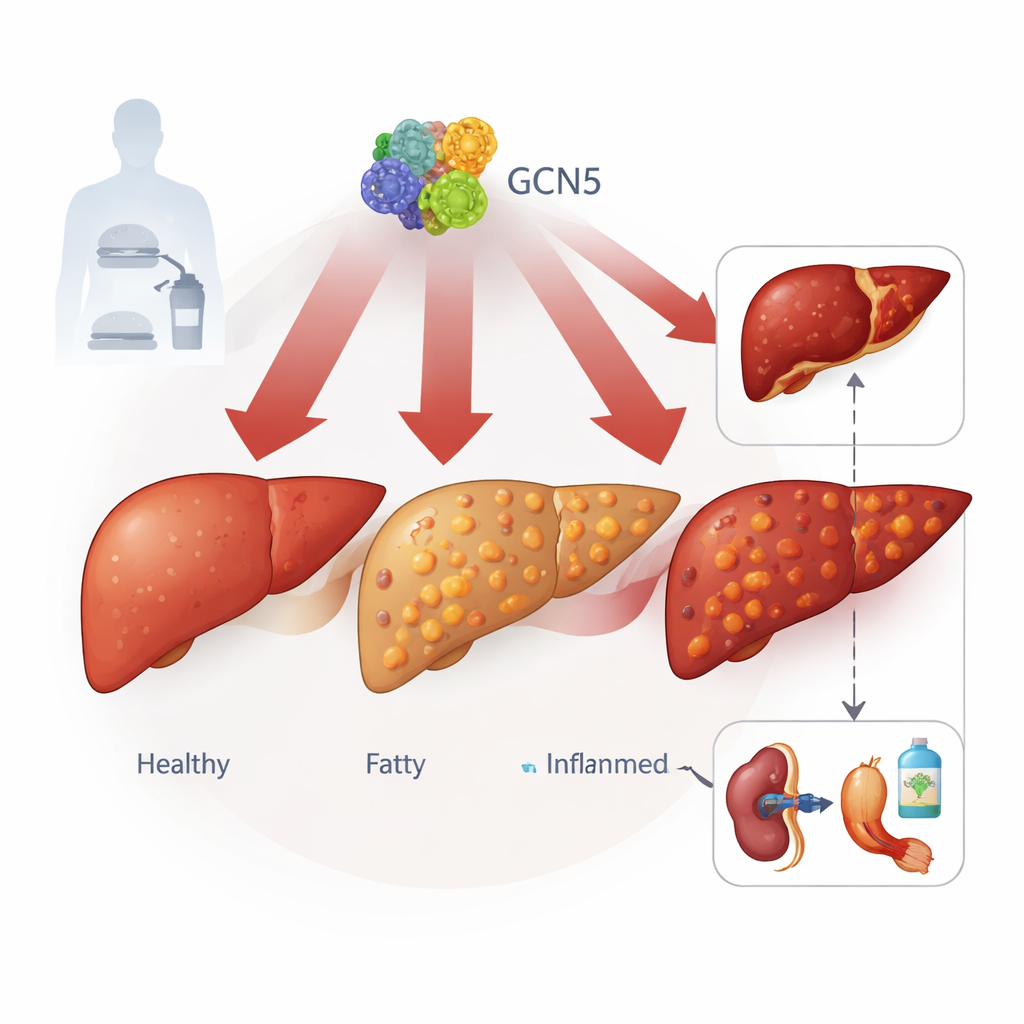
En dold strömbrytare inne i levercellerna
Författarna fokuserar på ett protein kallat GCN5, mest känt som en regulator av hur tätt DNA paketeras. Genom att studera levervävnad från mer än 100 personer, från friska till svår MASLD, och från flera musemodeller för kostinducerad fettleversjukdom, fann de att GCN5‑nivåerna i leverceller ökar stadigt i takt med sjukdomens förvärring. Ett närbesläktat protein, PCAF, visade inte samma mönster, vilket tyder på att GCN5 har en särskild roll. Höga GCN5‑nivåer korrelerade med mer leverfett, högre blodfetter och tydligare tecken på leverskada, vilket kopplar denna molekylära brytare till verklig sjukdomsgravitet.
Att skruva upp eller ner GCN5 i djur
För att testa orsak och verkan ökade teamet genetiskt eller tog bort GCN5 specifikt i musleverceller. När GCN5 ökades utvecklade möss på en fettrik diet tyngre, fetare lever, högre blodfetter och mer levercellsskada, trots att de inte åt mer eller gick upp i kroppsvikt. Leverceller odlade i skålar uppvisade liknande beteende: extra GCN5 ledde till större och fler fettkärnor. Däremot var möss som saknade GCN5 enbart i leverceller starkt skyddade. I flera dietmodeller som efterliknar mänsklig MASLD och dess mer inflammatoriska form samlade dessa djur på sig mindre leverfett, visade lägre blodlipider och leverenzymnivåer och utvecklade mindre inflammation och ärrbildning.
Hur GCN5 pressar levern att tillverka fett
Genom att gräva i metabolismen mätte forskarna många fettsyror och deras byggstenar i levern. Förlust av GCN5 minskade främst de fetter som levern tillverkar från grunden, en process känd som de novo‑lipogenes, medan kostrelaterade fleromättade fetter i huvudsak förblev oförändrade. Genuttrycks‑ och isotopspårningsförsök visade att GCN5 verkar upstream om en huvudregulator för fettbildning kallad SREBP1c. När GCN5 var aktiv slogs gener som bygger och modifierar fettsyror på, och leverns interna fett‑tillverkningshastighet ökade. Att ta bort eller blockera GCN5 nedreglerade detta program och minskade flödet av kol från socker till nyproducerat leverfett.
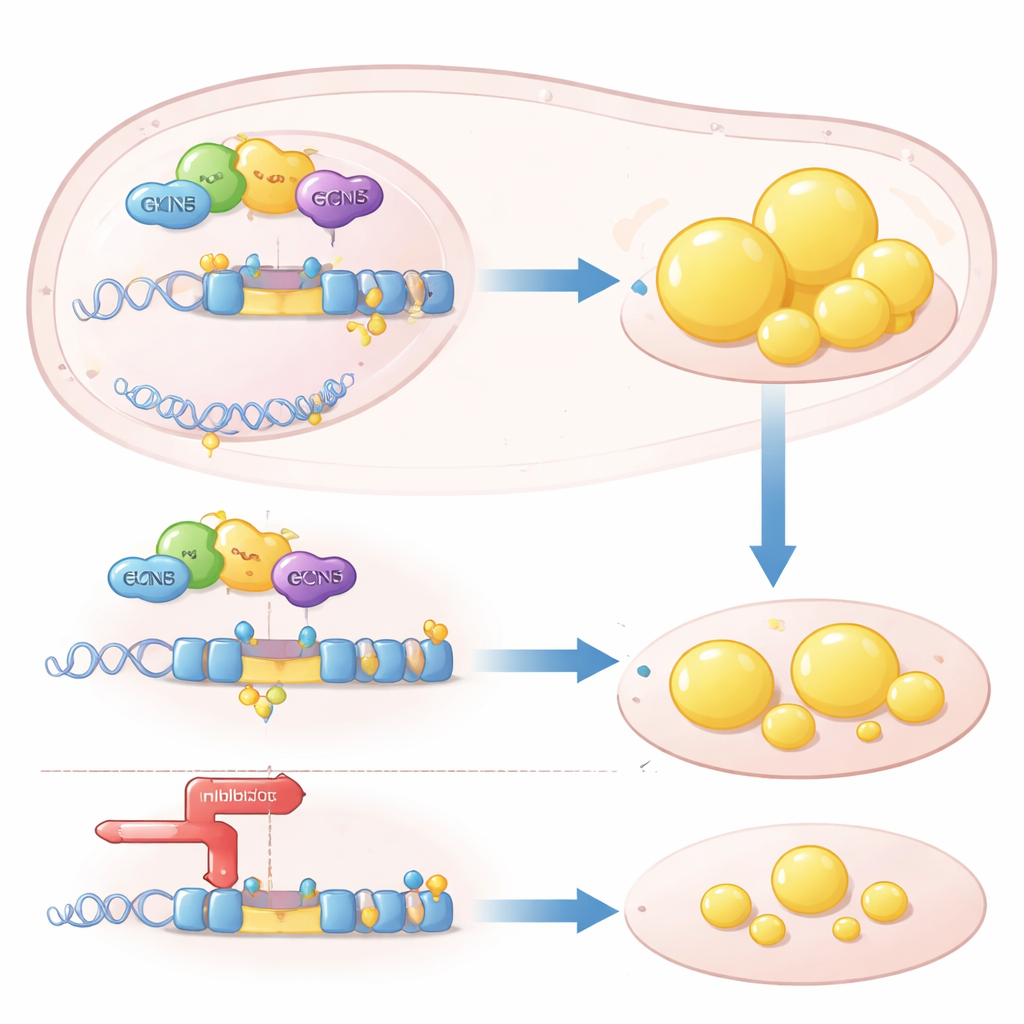
En epigenetisk hävstång på en viktig fettgen
Mechanistiskt agerar GCN5 som en "epigenetisk" hävstång: det kemiskt modifierar histonproteiner på DNA för att göra vissa gener lättare att läsa. Författarna visade att GCN5 rekryteras till kontrollregionen för SREBP1c‑genen tillsammans med en nukleär receptor kallad LXRα, som känner av kolesterolrelaterade molekyler. Väl där lägger GCN5 till acetylmärken på histon H3, luckrar upp lokalt kromatin och ökar SREBP1c‑transkriptionen. Denna effekt var mycket selektiv: GCN5 förstärkte LXRα:s förmåga att slå på SREBP1c men inte en annan LXR‑målgene, ABCA1, som hjälper till att rensa kolesterol från vävnader. Utan GCN5 kunde LXRα inte längre effektivt engagera SREBP1c‑promotorn, och det nedströms fett‑syntesprogrammet stannade av.
Läkemedelskandidat och en lovande kombination
Teamet testade sedan CPTH2, en småmolekylär hämmare av GCN5 som koncentreras i levern. I musemodeller redan satta på feta dieter minskade CPTH2 leverstorlek, fettinnehåll och skademarkörer utan uppenbar toxicitet eller förändringar i matintag. I odlade mänskliga och musleverceller sänkte CPTH2 fettkärnor och triglycerider endast när GCN5 fanns närvarande, vilket bekräftar att dess verkan är specifik. Viktigt är att CPTH2 både i celler och i möss behandlade med LXR‑aktiverande föreningar (utformade för att förbättra kolesterolborttagning och bekämpa ateroskleros) selektivt blockerade den oönskade ökningen av SREBP1c‑driven fettproduktion samtidigt som gener som främjar omvänd kolesteroltransport bevarades. När CPTH2 kombinerades med en LXR‑agonist i högt fett‑matade möss sänktes skadliga blodlipider och leverkolesterol ytterligare och extra fettansamling i levern förhindrades.
Vad detta betyder för patienter
Studien placerar GCN5 som en central drivare av leverfettansamling vid MASLD genom att koppla kost‑ och hormonella signaler till SREBP1c‑fettproduktionsbrytaren. Eftersom GCN5 synes vara dispensabel för den fördelaktiga kolesterolrensande grenen av LXR‑signalering, kan läkemedel som hämmar GCN5 — såsom CPTH2 eller mer avancerade efterföljare — dämpa leverfett och inflammation samtidigt som hjärt‑skyddande terapier får verka. För personer i riskzonen för både fettleversjukdom och hjärt‑kärlsjukdom kan riktade insatser mot denna epigenetiska brytare en dag erbjuda ett sätt att skydda levern utan att offra fördelarna med förbättrad kolesterolhantering.
Citering: Xiao, HT., Song, P., Jin, J. et al. GCN5 drives MASLD progression through LXRα/SREBP1c signaling pathway–mediated de novo lipogenesis. Nat Commun 17, 2821 (2026). https://doi.org/10.1038/s41467-026-69736-y
Nyckelord: fettleversjukdom, epigenetik, lipidmetabolism, levermetabolism, nukleära receptorer