Clear Sky Science · sv
N-Myc MB0–MBI-regionen interagerar specifikt och dynamiskt med N-loben hos Aurora-kinas A
Varför detta är viktigt för cancerbehandling
Många aggressiva barndomscancer är beroende av ett protein kallat N-Myc för att hålla tumörcellerna växande. N-Myc är själv svår att blockera med läkemedel eftersom det beter sig mer som en lös, böjlig tråd än som ett styvt lås som en nyckel kan passa i. Denna studie visar, med en tidigare otillgänglig detaljnivå, hur N-Myc greppar ett annat protein, enzymet Aurora-kinas A (AurA), för att öka dess aktivitet och hjälpa cancerceller att överleva. Genom att kartlägga detta partnerskap avslöjar forskarna en realistisk väg att bryta upp det med små molekyler.
En flexibel stökmakare hittar en stabil partner
N-Myc tillhör MYC-familjen av huvudregulatorer som styr celltillväxt, metabolism och delning. När dessa regulatorer överproduceras blir de kraftfulla cancerdrivare, särskilt i tumörer i nervsystemet som högrisk-neuroblastom hos barn. Till skillnad från många enzymer eller receptorer veckar sig inte N-Myc till en fast tredimensionell form på egen hand; det är ett ”intrinsiskt oordnat” protein som ständigt rör sig och omformas. Denna flexibilitet gör det anpassningsbart men också ökänd för att vara svårt att rikta läkemedel mot. AurA, däremot, är ett välstrukturerat enzym som hjälper till att organisera celldelningen. Tidigare arbete visade att AurA hjälper till att stabilisera N-Myc i tumörceller och att de två proteinerna interagerar fysiskt, men exakt vilka kontaktpunkter som är viktiga och hur de fungerar har varit oklart.
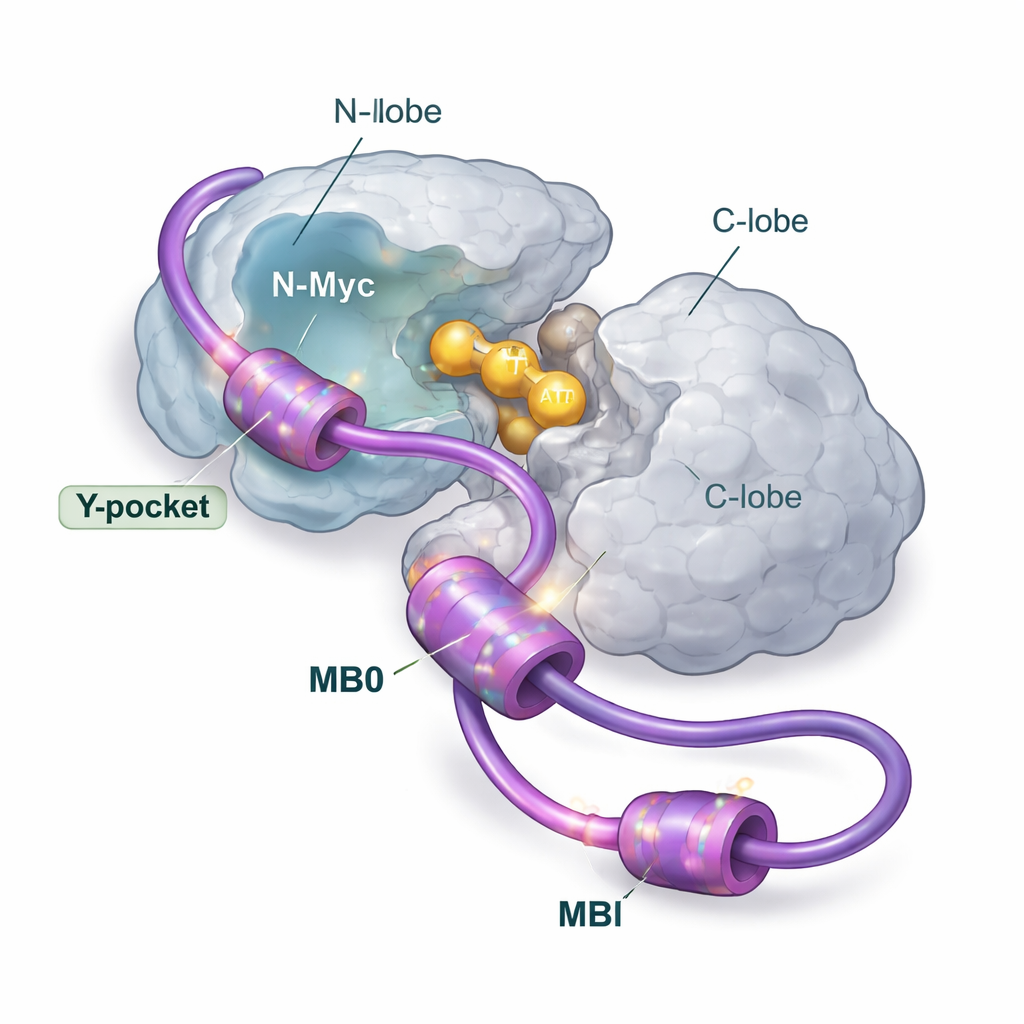
Flera grepppunkter, en huvudsaklig landningsplats
Med ett brett verktygspaket av strukturella och biofysiska metoder — inklusive kärnmagnetisk resonans, röntgenspridning, masspektrometri, kalorimetri och datormodellering — dissekerar författarna hur N-Myc och AurA förenas i lösning. De fokuserade på N-Mycs främre del, som innehåller två bevarade regioner kallade MB0 och MBI. Dessa korta segment är rika på aromatiska byggstenar (såsom fenylalanin, tyrosin och tryptofan) som har en tendens att fästa i fettiga fickor på partnerproteiner. Teamet visar att N-Myc binder AurA huvudsakligen som ett 1:1-par, där MB0 och MBI fungerar som de primära kontaktzonerna. Ett annat N-Myc-utdrag som fått uppmärksamhet i tidigare kristallstrukturer visar sig spela bara en mindre roll när hela MB0–MBI-regionen är närvarande.
En dynamisk handskakning som slår på enzymet
I stället för att låsa sig i en enda fast pose förblir N-Myc till stora delar oordnat när det är bundet till AurA. Data pekar mot ett ”grumligt” komplex: flera N-Myc-segment turas om att kontakta olika ytor på AurA:s N-lob, särskilt en fåra känd som Y-fickan och en närliggande slinga som förbinder signaler till det aktiva sätet. Trots denna löshet är effekten tydlig — bindning av MB0 och MBI stabiliserar AurA:s N-lob och ökar dess kinasaktivitet, vilket innebär att det blir mer effektivt på att överföra fosfatgrupper till sina mål. När forskarna systematiskt ersatte viktiga aromatiska rester i MB0 och MBI med alanin blev N-Myc–AurA-komplexet svagare, enzymet stabiliserades mindre och dess aktivitet sjönk. Detta visar att specifika aromatiska ”ankare” i den i övrigt sladdriga N-Myc-kedjan är avgörande för att öka AurA:s aktivitet.
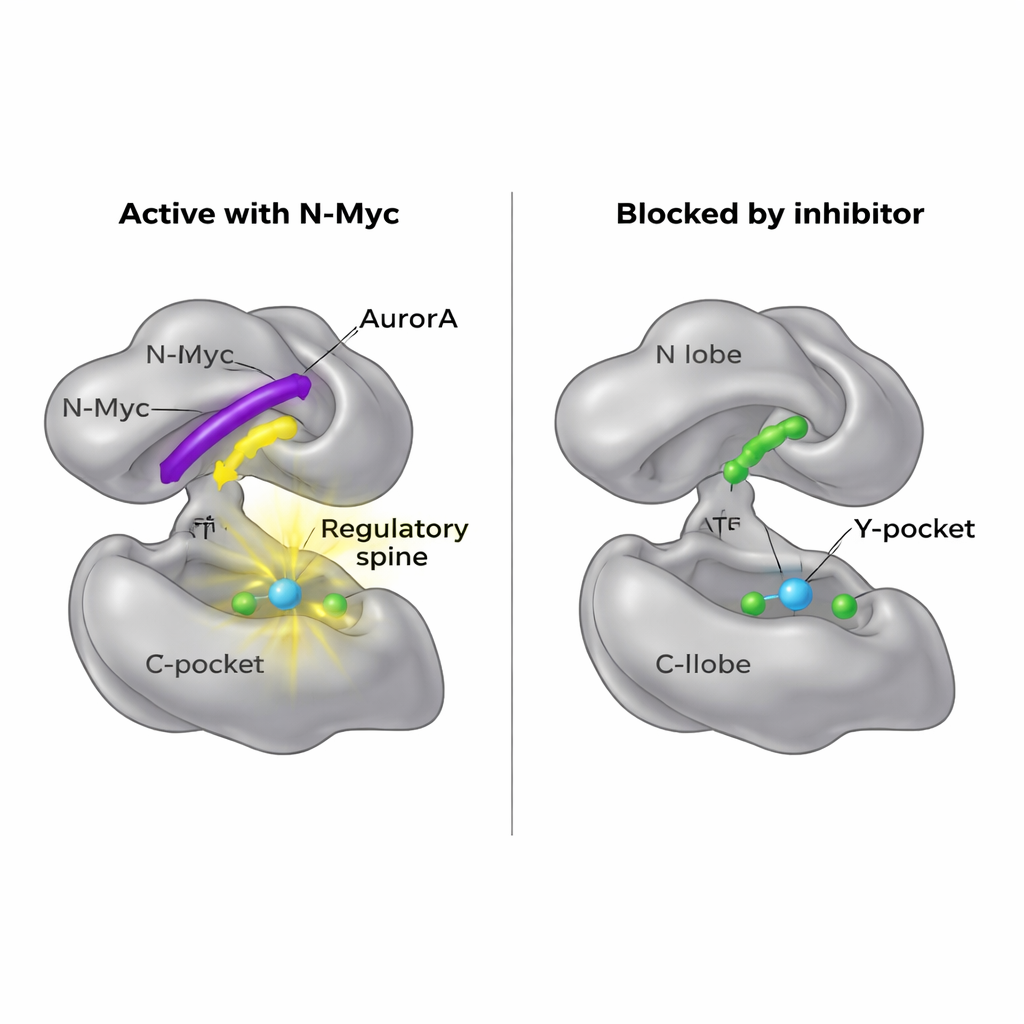
En ny öppning för läkemedel
Eftersom N-Myc i sig är svårt att angripa med läkemedel frågade sig forskarna om de i stället kunde blockera dess dockningsplats på AurA. Deras strukturkartor visade att MB0 och MBI upptar samma allmänna region av N-loben som en annan partnerprotein, TPX2, använder för att aktivera AurA. En liten molekyl kallad AurkinA är redan känd för att kila in i Y-fickan och undantränga TPX2. I bindningsexperiment konkurrerade AurkinA effektivt med N-Myc om AurA:s N-lob och förhindrade att både N-Myc1–69 och N-Myc1–100-fragmenten fäste. Detta resultat visar att N-lobens yta, och särskilt Y-fickan, är en druggbar hetfläck som kontrollerar inte bara klassiska regulatorer som TPX2 utan även oordnade onkoproteiner som N-Myc.
Vad detta innebär för framtida terapi
Detta arbete omformulerar N-Myc–AurA-partnerskapet som en dynamisk, flerkontaktig omfamning centrerad på AurA:s N-lob, snarare än en enda stel bindningsyta. För icke-specialister är huvudbudskapet att även ett formfattigt cancerprotein som N-Myc kan angripas indirekt genom att rikta in sig på en stabil dockningsfläck på dess partnerenzym. Genom att visa att befintliga N-lob-bindande föreningar kan tränga undan N-Myc från AurA öppnar studien en tydlig väg mot läkemedel som selektivt stör denna interaktion. Sådana ämnen skulle kunna försvaga ett kritiskt stöd för N-Myc i högriskbarntumörer och, med vidare utveckling, erbjuda en ny behandlingsväg för cancerformer som länge betraktats som ”obehandlingsbara”.
Citering: Hultman, J., Morad, V., Tanner, E. et al. The N-Myc MB0-MBI region interacts specifically and dynamically with the N-lobe of Aurora kinase A. Nat Commun 17, 2016 (2026). https://doi.org/10.1038/s41467-026-69725-1
Nyckelord: N-Myc, Aurora-kinas A, intrinsiskt oordnade proteiner, neuroblastom, hämmare av protein–protein-interaktioner