Clear Sky Science · sv
En rumsligt upplöst atlas över mänsklig glioblastom visar distinkta cellulära och molekylära mönster i anatomiska nischer
Varför den här kartan över hjärncancer är viktig
Glioblastom är en av de mest dödliga hjärncancerformerna, delvis därför att varje tumör är ett lapptäcke av olika celltyper och mikro-miljöer. Vanliga avbildningar och laboratorietester ser oftast tumören som en enhetlig massa. Denna studie bygger en högupplöst ”atlas” som visar var varje huvudcellstyp befinner sig i mänskliga glioblastom, hur dessa celler klustras i distinkta grannskap, och hur vissa av dessa nischer kan bidra till tumöråterväxt och förkorta patienters överlevnad.
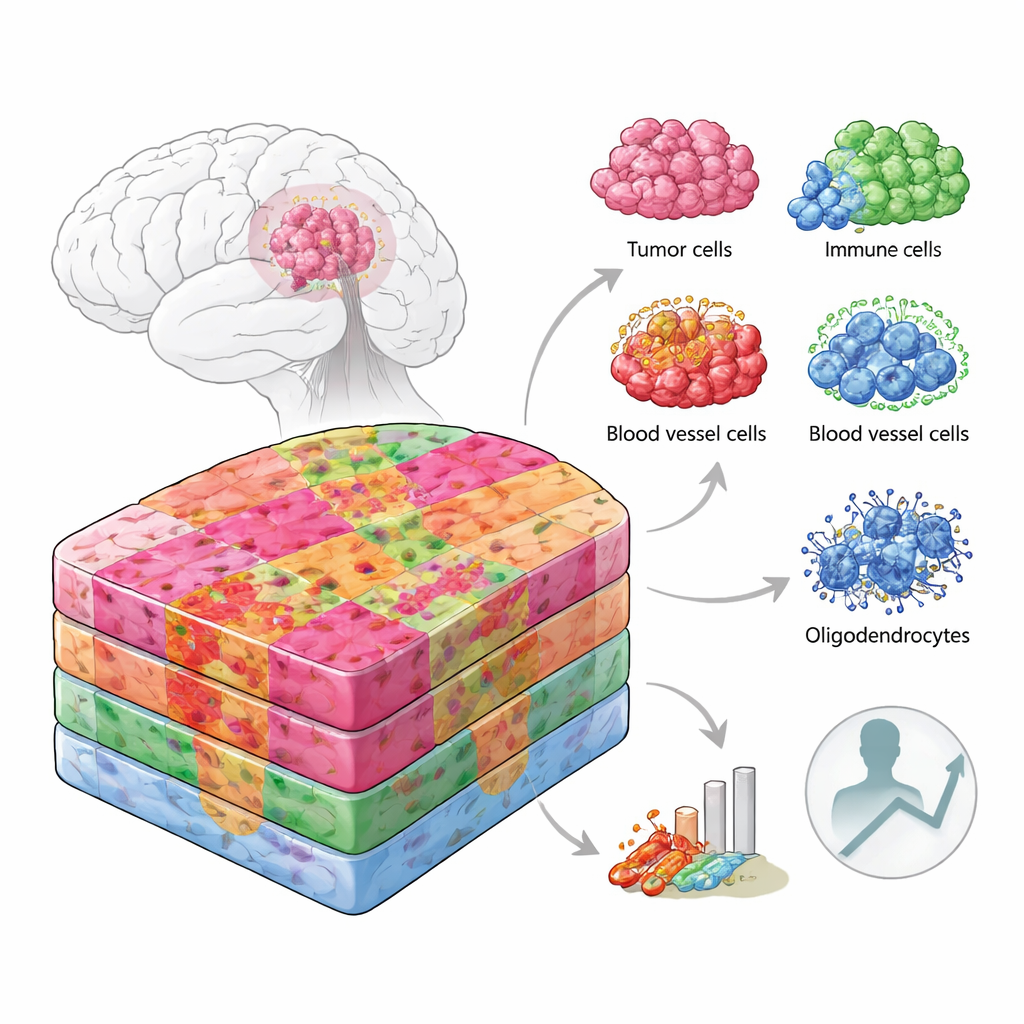
Att betrakta tumörer som stadsdelar
I stället för att betrakta ett tumörsnitt som homogent närmade sig forskarna det som en stadskarta, där varje distrikt har sin egen struktur och sina invånare. De kombinerade flera banbrytande tekniker som avläser genaktivitet från tusentals små platser över tumörvävnaden och matchade detta med enkellscellsdata och proteinmätningar. Viktigt är att de gjorde detta inte bara på färskt-fryst material från operationssalen utan även på rutinmässigt arkiverad, vaxinbäddad sjukhusvävnad — det som de flesta patologilabbet faktiskt förvarar. Totalt analyserade de mer än 100 000 rumsligt streckkodade regioner och över 220 000 individuella celler från patienter i olika åldrar och med olika genetisk bakgrund, och täckte både den täta tumörkärnan och dess mer diffusa kanter.
Gömda grannskap inne i glioblastom
Genom att överlagra genaktivitet på högförstorade mikroskopbilder delade teamet varje tumör i anatomiska ”nischer”, såsom den främre kanten där cancerceller infiltrerar normal hjärna, de trånga centrala zonerna, områden rika på blodkärl och regioner kring död eller syrefattig vävnad. Varje nisch visade sig inhysa sin egen blandning av celltyper. Tumörkanten i grå substans var rik på neuroner och typiska stödjeceller, medan kanten i vit substans innehöll många oligodendrocyter — de celler som normalt isolerar nervfibrer. Vissa vaskulära nischer var fullpackade med specialiserade blodkärls- och stödjeceller, medan andra dominerades av immunceller och ärrliknande vävnad. Hypoxiska zoner nära död vävnad hyste mest aggressiva, mesenkym-liknande tumörceller och makrofager, med betydligt mindre cellulär mångfald.
En överraskande roll för stödjeceller
Ett av de mest iögonfallande fynden rörde oligodendrocyter, vanligtvis betraktade som tysta ”isolatorer” i hjärnan. Atlasen avslöjade fyra distinkta oligodendrocyt-tillstånd, inklusive en tidigare underskattad typ som nästan uteslutande förekom i glioblastomens kärnor. Dessa celler hade förlorat många av sina myelinrelaterade gener och slog istället på gener kopplade till inflammation och stress, vilket liknade sjukdomsassocierade oligodendrocyter som setts vid multipel skleros och andra hjärnsjukdomar. Rumsligt klustrade denna immunkaraktäriserade oligodendrocytpopulation i en ”immun–glial nisch” tillsammans med aktiverade mikroglia, makrofager, onormala blodkärlsceller och mesenkym-liknande tumörceller — men betydligt inte i de mest syrefattiga regionerna.
Knyta mikroskopiska mönster till patientutfall
Författarna undersökte därefter om de genprogram som definierar dessa oligodendrocyt-tillstånd dyker upp i stora samlingar av tumörprover kopplade till patientjournaler. I två oberoende gliomkohorter var en signatur för konventionella, myelinproducerande oligodendrocyter kopplad till bättre överlevnad, även efter att man tagit hänsyn till ålder och viktiga genetiska riskmarkörer. I kontrast korrelerade signaturen för immunkompetenta oligodendrocyter med sämre överlevnad och var mer framträdande i aggressiva, behandlingsresistenta tumörer — särskilt de som återkom efter terapi och saknade en vanlig metyleringsförändring relaterad till DNA-reparation. Detta tyder på att hur oligodendrocyter omprogrammeras inne i tumören, och var de ligger i förhållande till tumör- och immunceller, kan påverka hur sjukdomen svarar på behandling och hur sannolikt det är att den återkommer.
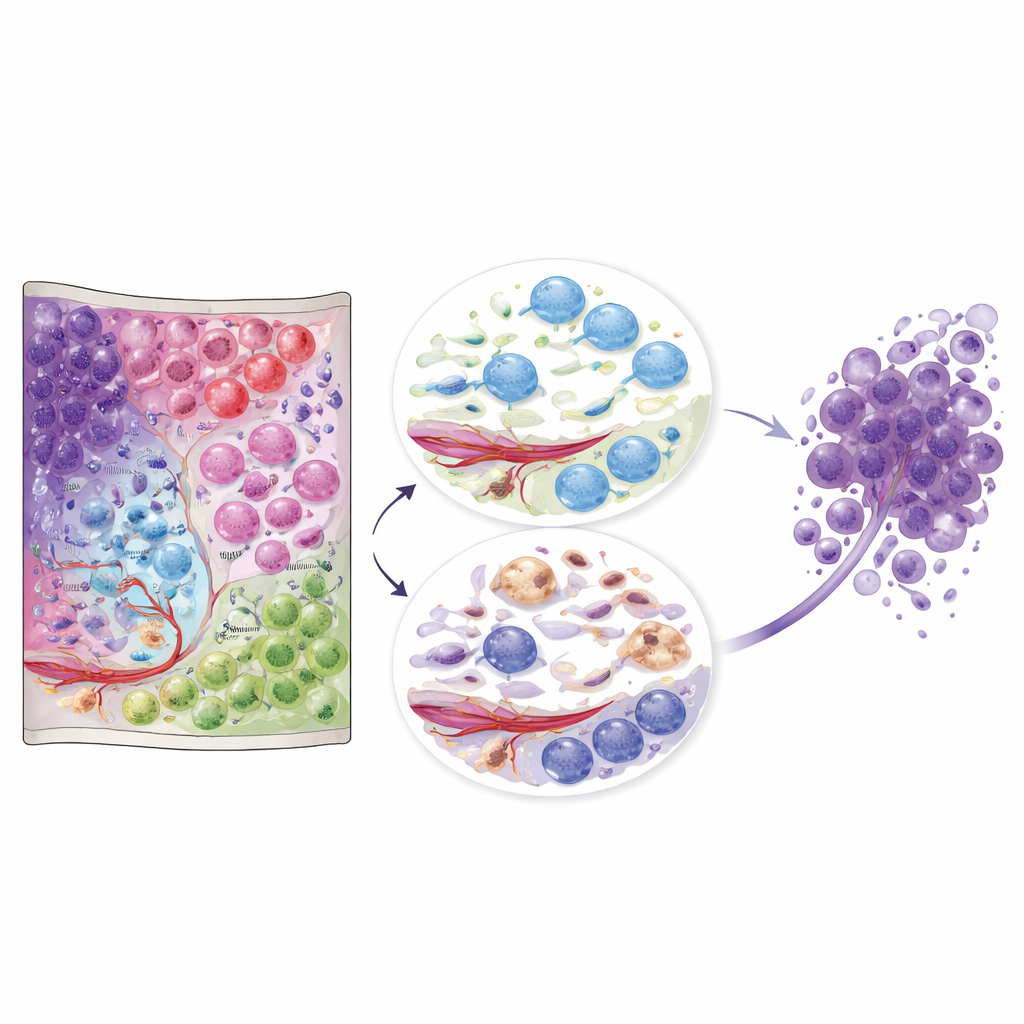
Vad denna atlas betyder för framtida vård
Tillsammans omvandlar dessa data glioblastom från en suddig massa till ett detaljerat landskap av interagerande cellgemenskaper. För icke-specialister är huvudbudskapet att läge och grannar spelar roll: samma breda celltyper beter sig mycket olika beroende på vilken nisch de intar. Den offentligt tillgängliga atlasen erbjuder en referens som andra forskare och kliniker kan använda för att placera sina egna prover i detta rumsliga sammanhang. På lång sikt kan terapier utformas inte bara för att döda tumörceller, utan för att störa skadliga nischer — såsom immunscar-regioner eller fickor med immunkompetenta oligodendrocyter — som tycks främja tumöröverlevnad och återfall.
Citering: Sonpatki, P., Park, H.J., Xing, Y.L. et al. A spatially resolved human glioblastoma atlas reveals distinct cellular and molecular patterns of anatomical niches. Nat Commun 17, 2951 (2026). https://doi.org/10.1038/s41467-026-69716-2
Nyckelord: glioblastom, rumslig transkriptomik, tumörmikromiljö, oligodendrocyter, hjärncanceratlas