Clear Sky Science · sv
FLEXTAG: ett litet och självförnyande system för proteinetikettering för blekningsresistent flerkedjig superupplösningsavbildning
Att se det osynliga inne i celler
Mycket av modern biologi bygger på att fotografera de molekyler som håller våra celler vid liv. Men även de bästa ljusmikroskopen kämpar med ett enkelt problem: de lysande markörerna som används för att framhäva proteiner bleknar snabbt, och det är svårt att märka många olika mål samtidigt utan att rubba cellernas funktion. I den här artikeln presenteras FLEXTAG, en ny familj av små, förnybara taggar som lyser mycket längre, stöder flera färger och fungerar med de mest kraftfulla mikroskopen forskare använder för att se cellernas inre arkitektur.
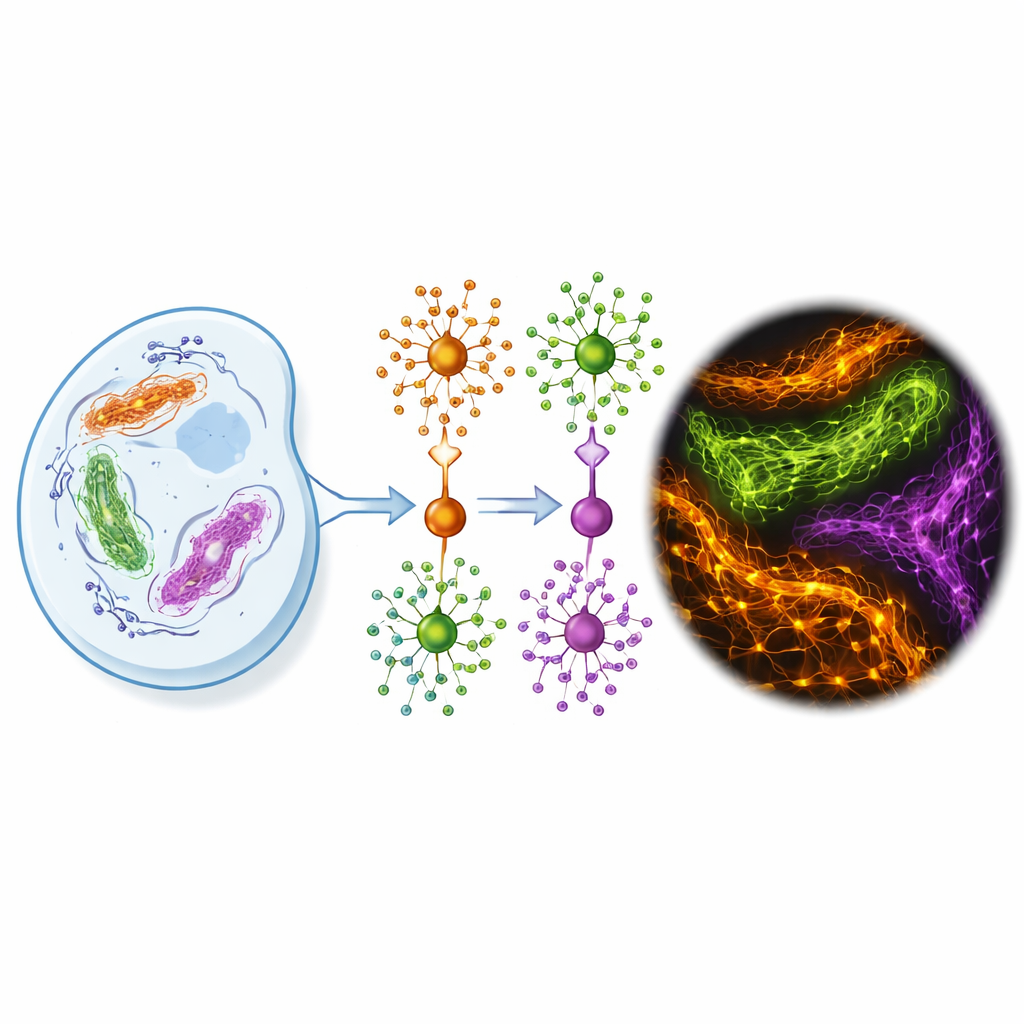
Varför skarpare cellbilder är så svåra
Konventionella fluorescensmikroskop kan avslöja strukturer på omkring en fjärdedels mikrometer, vilket fortfarande är mycket större än de flesta enskilda proteiner. Superupplösningsmetoder pressar fram mer detalj, ner till några miljondelar av en millimeter, men bara om de fluorescerande etiketterna beter sig perfekt. Dagens populära proteinmarkörer är antingen klumpiga antikroppar, svaga fluorescerande proteiner eller kemiska taggar vars färgämnen snabbt förstörs under det intensiva ljus som krävs för dessa tekniker. Fixering av celler med kemikalier för detaljerad avbildning kan också låsa proteiner i positioner som hindrar färgerna från att nå sina mål, och lösa färgämnen kan fastna ospecifikt och mörklägga bilden med bakgrundsglow.
En ny typ av påfyllbar protein-tagg
Författarna utvecklade FLEXTAG (förkortning för Fluorescent Labeling for Exchangeable, X-resilient Tagging in Advanced Generic Nanoscopy) för att angripa dessa begränsningar direkt. FLEXTAG är inte en enda tagg utan en samordnad trio—FLEXTAG1, FLEXTAG2 och FLEXTAG3—var och en ett litet ingenjörsprotein (12–18 kilodalton, ungefär hälften så stora som klassiska taggar som GFP och betydligt mindre än HaloTag). Varje FLEXTAG binder en matchande småmolekylär ligand som bär ett starkt organiskt färgämne. Avgörande är att denna bindning är reversibel: färg–ligand-molekyler kommer kontinuerligt och går. När en fluorofor skadas av ljus tar en ny från omgivande lösning dess plats, så signalen i praktiken ‘‘självförnyas’’ istället för att stadigt blekna.
Att bygga tre kompakta och tillförlitliga taggar
För att skapa FLEXTAG1–3 återanvände teamet tre välkända proteinskelett från cellbiologi och läkemedelsdesign och använde därefter strukturell modellering och bildbaserade tester för att omforma deras beteende. FLEXTAG1 härstammar från ett bromodomänprotein som känner igen en modifierad småmolekyl; författarna införde mutationer för att bryta upp dess tendens att para sig och bilda klumpar, samtidigt som stark bindning till liganden bevarades. FLEXTAG2 kommer från bakteriellt dihydrofolatreduktas. Genom att lägga till en strategisk disulfidbrygga och finjustera flexibla länkar stabiliserade de proteinet och ökade dramatiskt hur många taggar som bar färg vid varje givet ögonblick, samtidigt som bindningen förblev reversibel. FLEXTAG3 är baserat på ett mänskligt FKBP-protein som används i kemisk biologi; här balanserade teamet bindningsstyrka och hastighet så att färger lossnar tillräckligt snabbt för att kunna ersättas, men ändå binder tillräckligt starkt för att ge klara bilder och undvika överdriven aggregering.
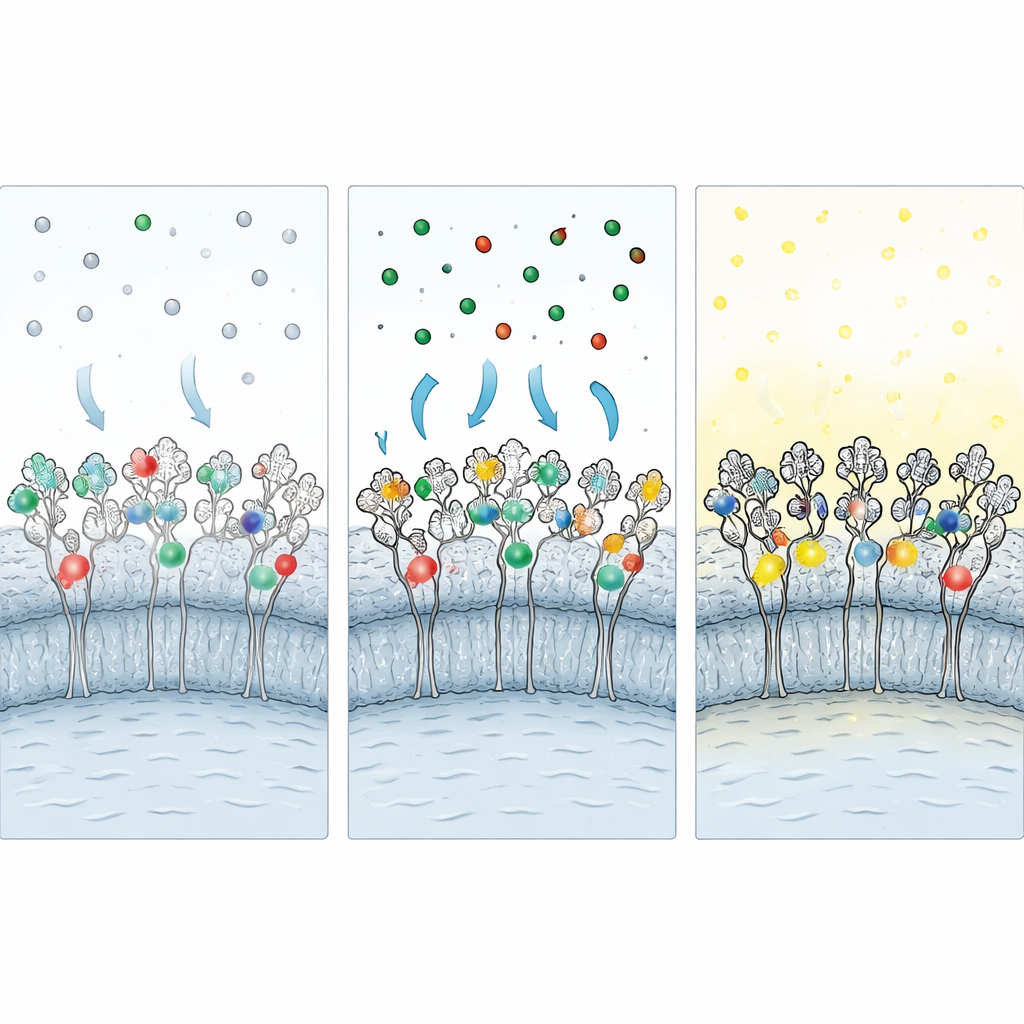
Skydda taggar under fixering och minska bakgrundsglow
Eftersom många viktiga experiment kräver avbildning av fixerade celler utvecklade forskarna en ‘‘skyddande fixerings’’-strategi. Innan aldehydfixativ tillsattes översvämmade de levande cellerna med omärkta versioner av varje ligand och blockerade taggens bindningsficka. Under fixeringen skyddar dessa skyddande ligander känsliga aminosyror från kemisk tvärbindning. Efter fixering tvättas de skyddande liganderna bort och ersätts med fluorescerande sådana, vilket återställer tillgången till taggen. Ytterligare steg—kemisk reduktion för att neutralisera kvarvarande reaktiva grupper och en blockerande cocktail innehållande albumin, detergent och ett kaotropt salt—minskar vidare klibbigt, ospecifikt samband av fria färgämnen. Tillsammans bevarar dessa åtgärder omkring 60–70 % av märkningen som ses i levande celler samtidigt som signal-till-brus-förhållandet förbättras markant.
Skarpare, längre filmer över många metoder
Med FLEXTAG-ramverket på plats testade författarna det över de stora familjerna av superupplösningsmikroskopi. I mönstrade belysningsmetoder som SIM och STED möjliggjorde FLEXTAGs flerkedjig avbildning av mitokondrier, mikrotubuli, endoplasmatiskt retikulum och aktin med mycket mindre blekning än standard kovalenta taggar; över dussintals avbildningscykler sjönk signalen från konventionella taggar till hälften eller mer, medan FLEXTAG-signaler förblev nästan konstanta. I enskolekylmetoder som PAINT och STORM gav den snabba on–off-utbytet av FLEXTAG-ligander rika, stabila strömmar av lokalisationer som kunde omvandlas till tredimensionella, flerkedjiga kartor av subcellulära strukturer, även i levande celler över många minuter. FLEXTAG2 visade särskilt gynnsam kinetik för PAINT, medan FLEXTAG3 utmärkte sig i långtids STORM-filmer. Eftersom taggarna är ortogonala mot varandra och kompatibla med ett brett spektrum av färgämnen kan forskare märka flera proteiner samtidigt och sedan välja den avbildningsmetod som bäst passar deras fråga utan att ändra de underliggande konstrukten.
Vad detta betyder för att titta inne i celler
FLEXTAG erbjuder en slags universell, påfyllbar förbindelse mellan proteiner och starka färgämnen. Dess lilla storlek minskar risken att taggen förvränger var ett protein hamnar eller hur det fungerar, och dess självförnyande färger hjälper till att kringgå det länge existerande problemet med fotobilning i kraftfulla mikroskop. Genom att kombinera dessa taggar med skyddande fixering och kemi som dämpar bakgrund kan forskare få renare, längre varande och mer färgrika vyer av hur proteiner är organiserade och rör sig inne i celler. I praktiska termer innebär det bättre kartor över cellulär arkitektur, mer tillförlitlig spårning av molekylära interaktioner över tid och en mångsidig verktygslåda som bör gynna både grundläggande cellbiologi och transnationella studier som förlitar sig på att se sjukdomsrelaterade förändringar i nanoskala.
Citering: Zhang, H., Yao, Y., Wang, X. et al. FLEXTAG: a small and self-renewable protein labeling system for anti-fading multi-color super-resolution imaging. Nat Commun 17, 2156 (2026). https://doi.org/10.1038/s41467-026-69658-9
Nyckelord: superupplösningsmikroskopi, fluorescerande proteinmärkning, levande-cell-avbildning, motstånd mot fotobilning, cellulär arkitektur