Clear Sky Science · sv
Signaturer för exoninkludering gör det möjligt att noggrant uppskatta aktiviteten hos splitsningsfaktorer
Att läsa cellens dolda redigeringsmärken
Varje cell i vår kropp redigerar ständigt sina RNA-meddelanden innan de omvandlas till proteiner. Denna redigering, kallad splitsning, hjälper till att avgöra om en cell förblir frisk eller blir cancerös. Studien bakom denna artikel visar att genom att noggrant undersöka vilka RNA-delar som bevaras eller hoppas över — så kallade exoninkluderingssignaturer — kan forskare med hög noggrannhet sluta sig till aktiviteten hos de molekylära ”redigerarna” som styr splitsning, även i komplexa sjukdomar som cancer.
Hur celler klipper och klistrar sina meddelanden
Gener läses inte i ett enda obrutet streck. Istället tar cellerna bort icke-kodande segment och syr ihop kodande delar, kända som exoner, för att bygga de slutliga RNA-meddelandena. Specialiserade proteiner kallade splitsningsfaktorer styr denna klipp-och-klistra-process och bestämmer vilka exoner som inkluderas. Deras beteende påverkas av många regleringslager: hur mycket av deras eget RNA och protein som produceras, hur de kemiskt modifieras, var de befinner sig i cellen och hur de interagerar med andra proteiner. Eftersom så många reglage kan ändra splitsningsfaktorers beteende, räcker det ofta inte att mäta en enda datatyp — till exempel genuttryck — för att avslöja vad dessa faktorer faktiskt gör.
Att omvandla exonmönster till aktivitetsavläsningar
Inspirerade av tidigare arbete med transkriptionsfaktorer föreslår författarna en annan strategi: istället för att försöka mäta splitsningsfaktorer direkt, läsa av deras aktivitet utifrån deras effekter. När en splitsningsfaktor förändras skiftar inkluderingen av dess målexoner i igenkännliga mönster. Teamet sammanställde hundratals experiment där enskilda splitsningsfaktorer slagits ner, slagits ut eller överuttryckts, och använde dessa data för att bygga ”empiriska nätverk” som länkar varje faktor till de exoner den tydligt påverkar. De anpassade sedan ett beräkningsramverk kallat VIPER för att läsa en ny exoninkluderingssignatur och poängsätta hur aktiv varje splitsningsfaktor måste vara för att förklara det observerade mönstret.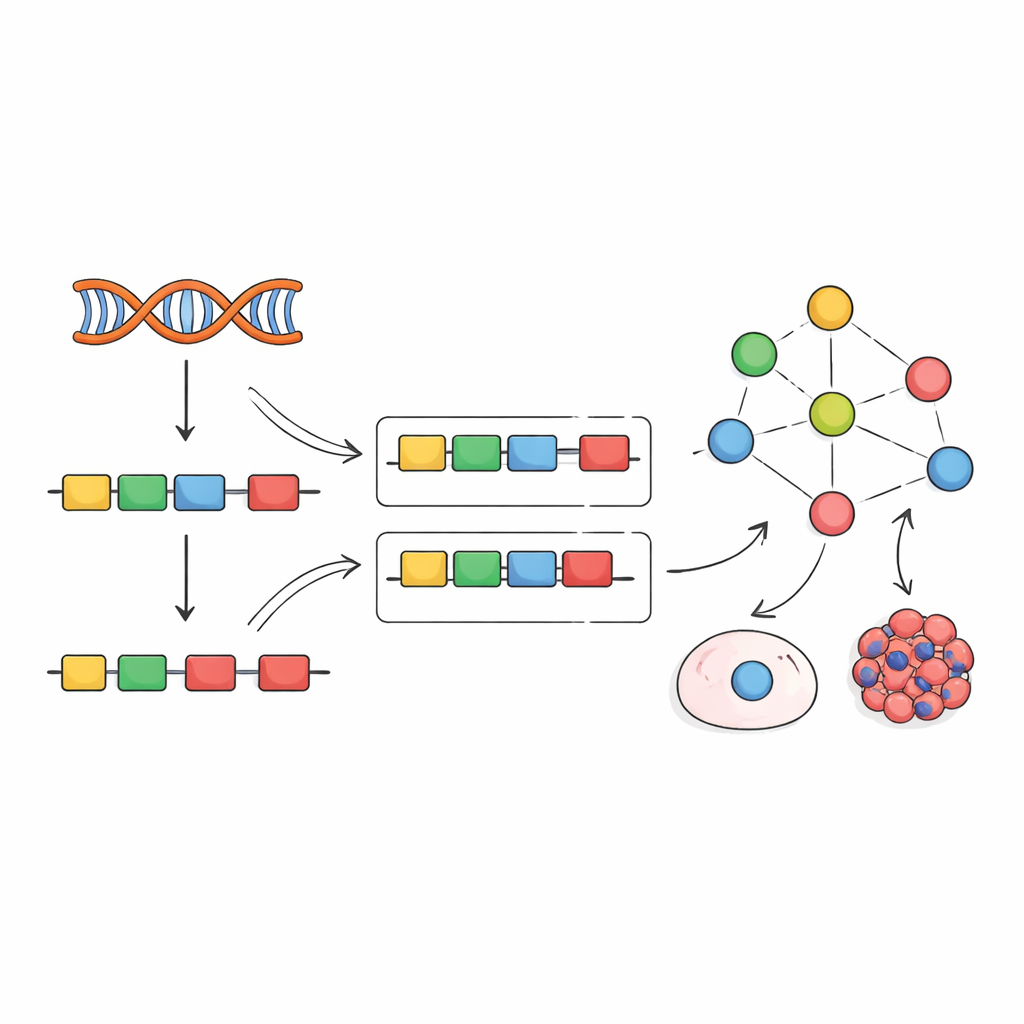
Test av metoden i verkliga störningar
För att se om detta tillvägagångssätt fungerar benchmarkade forskarna flera sätt att bygga nätverk och beräkna aktivitetspoäng. Empiriska nätverk som härstammar direkt från perturbationsexperiment, kombinerade med VIPER:s berikningsanalys, presterade tydligt bättre än alternativ baserade enbart på statistisk inferens. Metoden identifierade korrekt den experimentellt perturberade splitsningsfaktorn i de flesta tester, även över olika celltyper och studier. Den fångade också mer subtila regleringsmekanismer. Till exempel utlöser ett cancerläkemedel kallat Indisulam nedbrytning av splitsningsfaktorn RBM39:s protein medan dess RNA-nivåer stiger i vad som verkar vara ett kompensationsförsök. Traditionell uttrycksanalys skulle vilseledande antyda att RBM39 är mer aktivt, men den exonbaserade aktivitetspoängen avslöjade korrekt en kraftig funktionsförlust, i linje med läkemedlets kända verkan.
Att avslöja dolda splitsningsprogram i cancer
Utrustade med detta verktyg vände sig författarna till The Cancer Genome Atlas och analyserade data på exon-nivå från flera tumörtyper och matchande friska vävnader. De upptäckte två breda och återkommande splitsningsprogram. Ett program består av splitsningsfaktorer som tenderar att vara mer aktiva i tumörer och är förknippat med sämre patientöverlevnad — ett onkogentliknande program. Det andra kännetecknas av faktorer som systematiskt är mindre aktiva i tumörer och kopplas till bättre utfall, liknande tumörsuppressorer. Dessa program påverkar gener involverade i grundläggande cancerkarakteristika såsom snabb cellproliferation och tumörers förmåga att dölja sig för immunsystemet. Till exempel verkar vissa exoner reglerade av det tumör-suppressorliknande programmet påverka hur väl patienter svarar på immunkontrollpunktsterapier, vilket pekar på nya markörer eller interventionspunkter.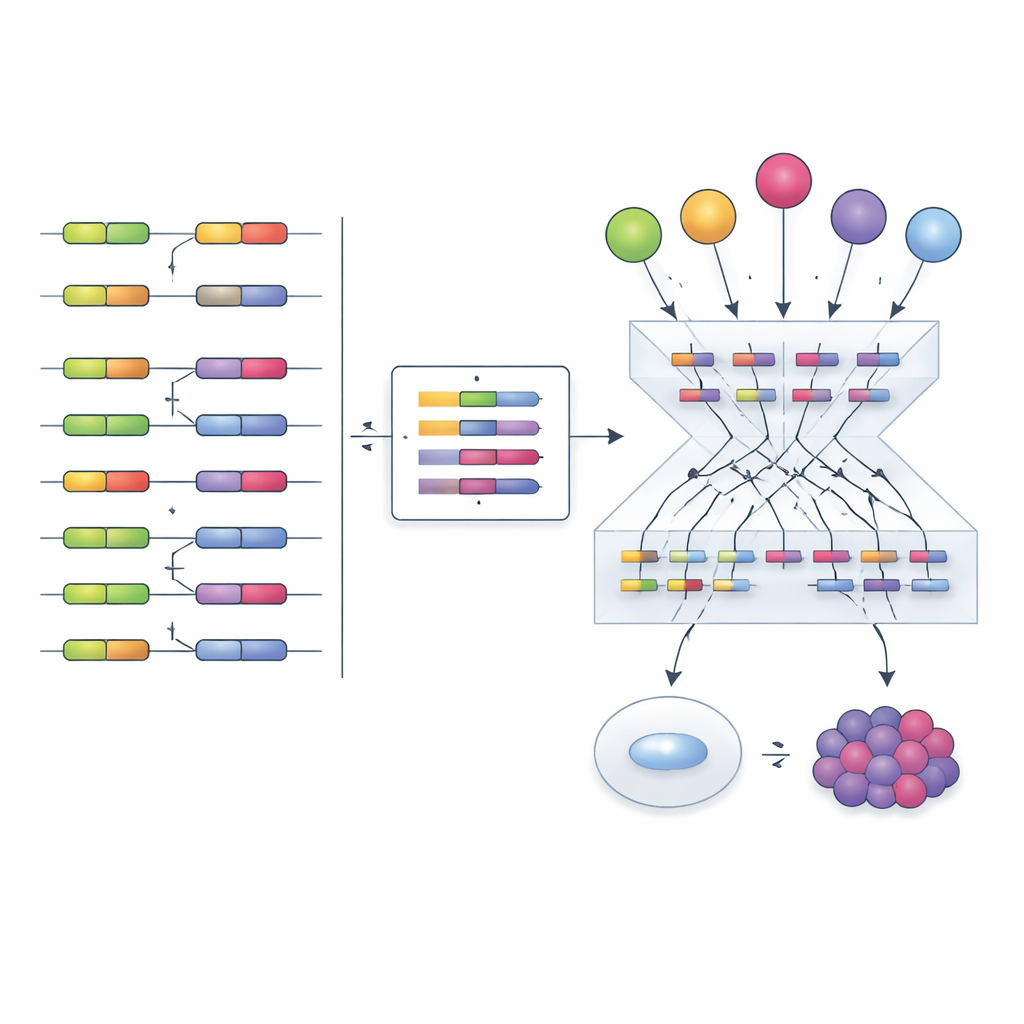
Att följa splitsningsförändringar på vägen mot cancer
Teamet undersökte också en steg-för-steg-modell av mänskliga celler som går från normala till odödliga, tumörbildande och slutligen metastaserande tillstånd. De fann att det onkogentliknande splitsningsprogrammet blir mer aktivt när celler förvärvar cancerdrivande mutationer, medan det tumör-suppressorliknande programmet mattas ut. Genom att integrera flera datalager — RNA-nivåer, proteinmängd, kemiska modifieringar och splitsningsförändringar inom splitsningsfaktorerna själva — identifierade de en fokuserad uppsättning kandidat-molekylära händelser som kan driva dessa programskiften, vilket ger en prioriterad lista för framtida experimentella tester.
Varför detta är viktigt för patienter och framtida forskning
I korthet visar studien att splitsningsfaktorers komplexa beteende kan destilleras till en enda, tolkbar aktivitetspoäng härledd från hur exoner inkluderas eller hoppas över. Detta gör det möjligt att studera splitsningsreglering i stora patientkohorter och i olika experiment med endast standard RNA-sekvenseringsdata, utan att kräva dyr multi-omisk profilering. För en allmän läsare är huvudbudskapet att mönster i hur gener klipps och klistras innehåller rik information om cellens dolda kontrollsystem, och att avkoda dessa mönster kan avslöja nya cancerdrivare, förbättra prognoser och vägleda jakten på mer precisa behandlingar.
Citering: Anglada-Girotto, M., Segura-Morales, C., Moakley, D.F. et al. Exon inclusion signatures enable accurate estimation of splicing factor activity. Nat Commun 17, 1994 (2026). https://doi.org/10.1038/s41467-026-69642-3
Nyckelord: RNA-splitsning, splitsningsfaktorer, cancergenomik, transkriptomik, slutsats om proteinaktivitet