Clear Sky Science · sv
LOAd703‑inducerad genmodifiering av tumörmikromiljön i kombination med atezolizumab vid metastaserande malignt melanom: en fas I/II‑studie
Varför denna nya melanomstudie är viktig
För personer med avancerat hudmelanom som inte längre svarar på dagens kraftfulla immunterapier är behandlingsalternativen begränsade och ofta tuffa. Denna studie prövar en annan idé: att använda ett genmodifierat virus som injiceras direkt i tumörer, tillsammans med ett befintligt immunstärkande läkemedel, för att väcka kroppens försvar och återfå kontroll över cancern. De tidiga resultaten tyder på att denna metod kan ges säkert och kan hjälpa en betydande andel patienter vars sjukdom tidigare varit motståndskraftig mot standardvård.
En envis hudcancer som överlistar behandling
Melanom är en av de vanligaste allvarliga hudcancerformerna i västliga länder, och förekomsten har ökat kraftigt under de senaste årtiondena. Moderna immuncheckpointläkemedel — som tar bort bromsen på T‑celler — har förändrat prognosen och höjt femårsöverlevnaden vid avancerat melanom till omkring hälften av patienterna. Ändå slutar många tumörer så småningom att svara. Ofta omges dessa resistenta cancerformer av en ”kall” miljö av celler och molekyler som håller immunceller borta eller släcker deras funktion. Att hitta sätt att omprogrammera denna tumörmikromiljö så att T‑celler återigen kan känna igen och angripa tumören är en viktig forskningsprioritet.
Ett virus designat för att omstyra tumörens grannskap
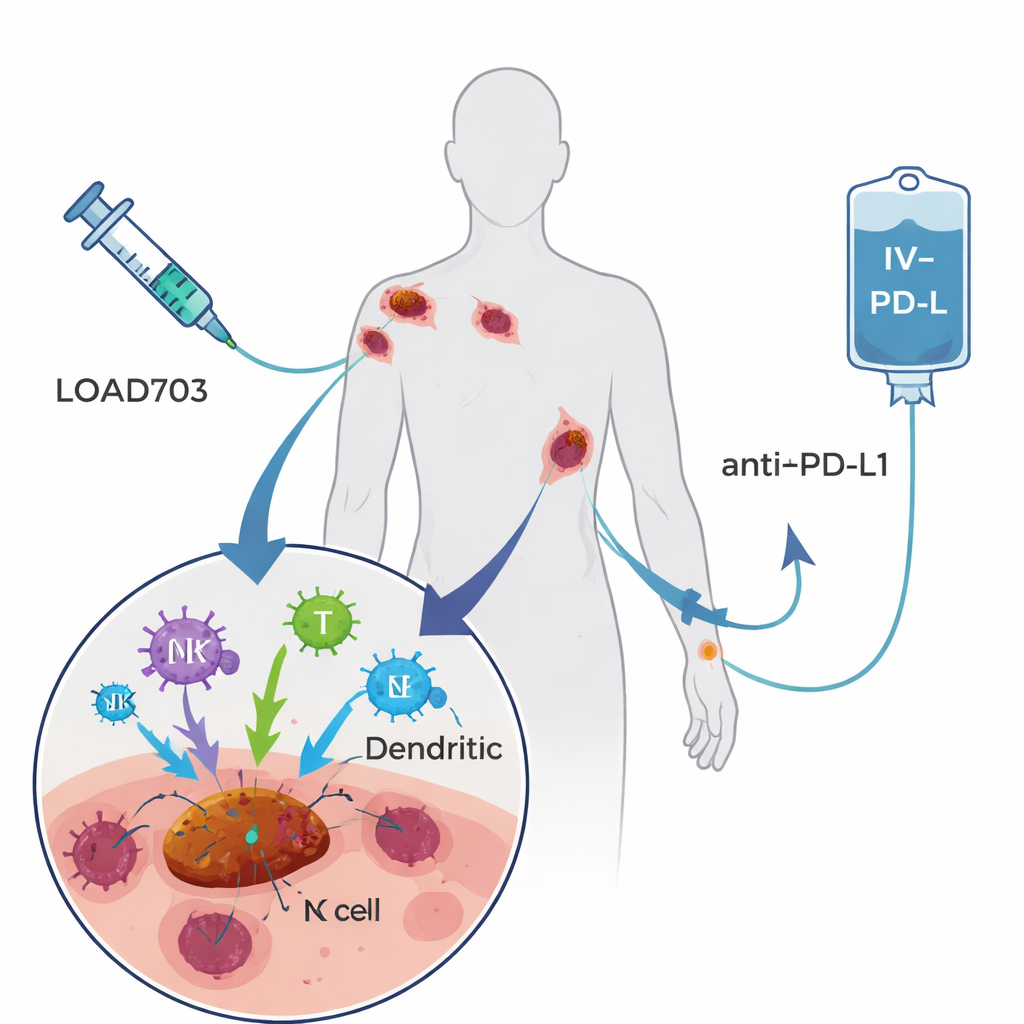
Behandlingen som testades här, kallad LOAd703, är ett modifierat adenovirus — en typ av vanligt förkylningsvirus — konstruerat för att utföra två uppgifter. För det första föredrar det att replikera i och förstöra tumörceller, en strategi känd som onkolytisk viroterapi. För det andra bär det genetiska instruktioner för två kraftfulla immunstimulerande signaler uttryckta på infekterade celler. Dessa signaler, CD40L och 4‑1BBL, hjälper professionella immunchaufförer (dendritiska celler) att mogna och presentera tumörfragment, samtidigt som de stärker och utvidgar cancerbekämpande T‑celler och natural killer‑celler. Patienterna i studien fick LOAd703 injicerat direkt i en eller flera tumörer var tredje vecka, tillsammans med atezolizumab, ett etablerat antikroppsbaserat läkemedel som ges intravenöst och blockerar PD‑L1‑bromsen på T‑celler. Förhoppningen var att viruset skulle förvandla tumörer till kroppsegna vaccinfabriker, medan antikroppen höll de återaktiverade T‑cellerna aktiva.
Vem som behandlades och hur det gick
Fas I/II‑studien rekryterade 24 personer med stadium IV‑melanom som tydligt progredierat trots minst en tidigare PD‑1‑hämmare; många hade fått flera behandlingslinjer med immunterapi och målinriktade läkemedel. Två virusdosnivåer testades. Kombinationsbehandlingen tolererades överlag väl. De vanligaste biverkningarna kopplade till viruset — feber, frossa, illamående och influensaliknande symtom — var i huvudsak milda och övergående. Endast två patienter fick mer allvarliga men reversibla reaktioner vid den högre dosen, och ingen behövde avbryta behandlingen på grund av virusrelaterade problem. När forskarna bedömde tumörsvaren hade fyra patienter (17 %) mätbar tumörminskning, och mer än hälften hade åtminstone stabil sjukdom under en tid. Två år efter studieintagningen var nästan hälften av deltagarna fortfarande vid liv, inklusive några vars skanningar visade långvarig kontroll eller komplett försvinnande av påvisbar sjukdom efter avslutad terapi.
Tecken på att immunsystemet återaktiverades
För att se vad som hände inne i tumörerna och i blodomloppet analyserade teamet vävnadsbiopsier och blodprover tagna före behandling och omkring nio veckor efter påbörjad behandling. I de injicerade tumörerna observerades ökad aktivitet i gener kopplade till typ 1‑immunsvar, inklusive markörer för aktiverade T‑celler och natural killer‑celler, samt molekyler som hjälper dessa celler att ta sig in i tumörer från närliggande blodkärl. Signaler associerade med antigenpresentation — processen där tumörfragment visas för T‑celler — ökade också, vilket tyder på att viral terapi omvandlade tumörmikromiljön från undertryckande till mer immunvänlig. I blodet steg flera immunrelaterade proteiner, inklusive PD‑L1 självt, efter terapin, i linje med en bred aktivering av immunsystemets vägar. Patienter som överlevde längre tenderade att visa genmönster knutna till robust T‑cellsfunktion och antiviralt skydd, medan de med kortare överlevnad uppvisade mönster associerade med suppressiva celltyper och signaler för vävnadsombyggnad.
Vad detta kan innebära för framtida vård
Detta var en liten, enkel arms‑studie utan jämförelsegrupp, så dess överlevnads‑ och responssiffror måste tolkas försiktigt. Ändå antyder kombinationen av god tolerabilitet, immunaktivering i tumörer och uppmuntrande sjukdomskontroll hos tungt förbehandlade patienter att genmodifierade onkolytiska virus som LOAd703 skulle kunna hjälpa till att återkänsliggöra melanom för checkpoint‑blockad — eller till och med hålla tumörer i schack på egen hand. Resultaten stödjer större, kontrollerade prövningar, eventuellt i kombination med ytterligare immuntargeterade läkemedel, för att klargöra vilka patienter som gynnas mest och hur denna strategi bäst kan integreras i melanombehandlingen.
Citering: Hamid, O., Ekström-Rydén, V., Mehmi, I. et al. LOAd703-induced tumor microenvironment gene engineering in combination with atezolizumab in metastatic malignant melanoma: a phase I/II trial. Nat Commun 17, 1760 (2026). https://doi.org/10.1038/s41467-026-69629-0
Nyckelord: melanom, immunterapi, onkolytiskt virus, tumörmikromiljö, resistens mot checkpoint‑hämmare