Clear Sky Science · sv
Läkemedel i bur möjliggör fotokatalytisk samtidig frisättning av kväveoxid och lokalbedövningsmedel för antibakteriell analgesi
Bekämpa bakterier och smärta samtidigt
Bakterieinfektioner hotar inte bara vår hälsa; de gör också ont — ofta väldigt mycket. Standardbehandlingar riktar sig vanligtvis mot bakterierna men lämnar patienterna beroende av separata smärtstillande medel, som kan sluta verka snabbt eller ge biverkningar. Denna studie presenterar ett ljusstyrt läkemedel som syftar till att döda bakterier och lindra smärta i ett samordnat steg, vilket ger en glimt av smartare och mer bekväm infektionsvård.
En två-i-ett-läkemedelsidé
Forskarna byggde sin strategi kring tetrakain, ett välkänt lokalbedövningsmedel som används för att bedöva hud och nerver. De kopplade kemiskt ihop kväveoxid, en liten gasmolekyl känd för sina starka antibakteriella och antiinflammatoriska effekter, med tetrakain. Detta skapade en ”prodrug” kallad TTC-NO som i stort sett är inaktiv tills den aktiveras. TTC-NO packades sedan, tillsammans med ett ljuskänsligt hjälpämne, i små polymerkapslar kallade miceller som kan färdas i vattenmiljöer såsom blod eller vätska i vävnad. 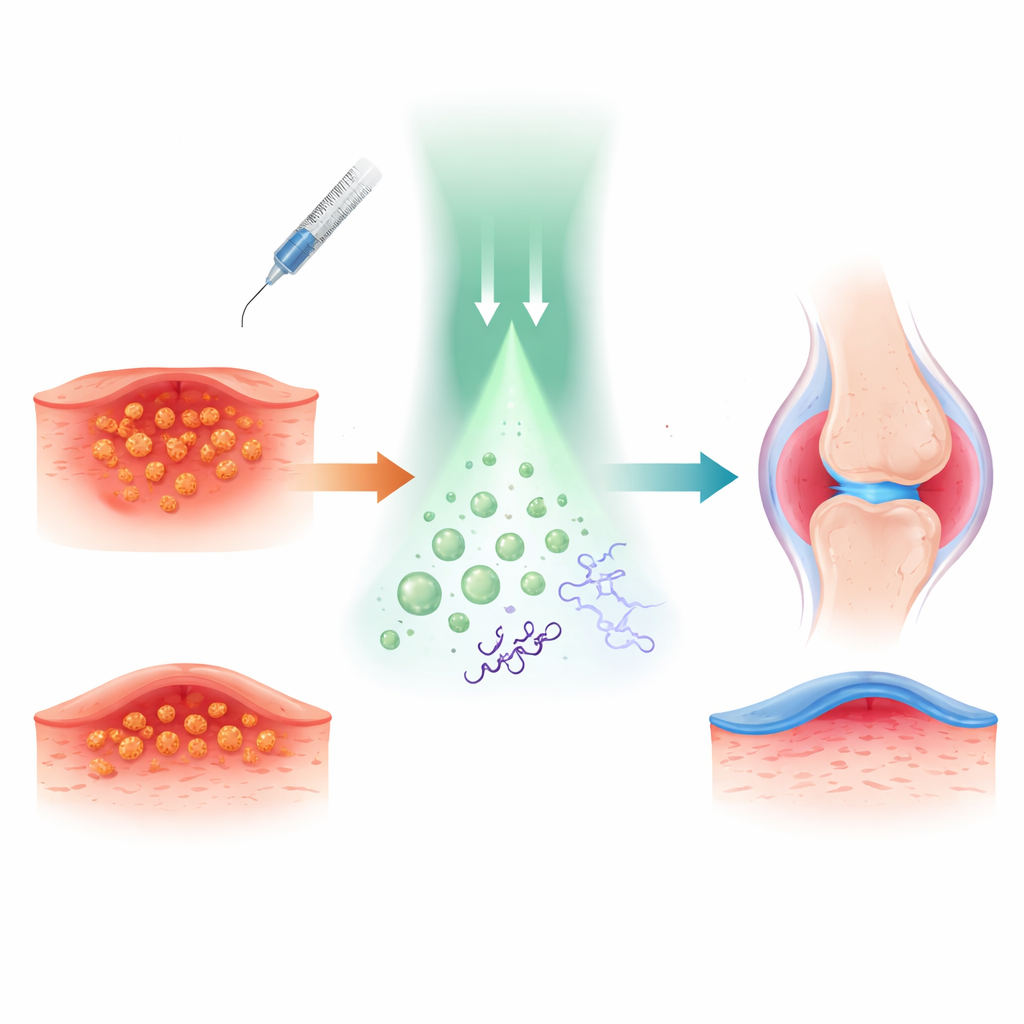
Aktivera läkemedlet med milt ljus
För att förstå hur denna ljusbrytare fungerar studerade teamet kemin i lösning. De visade att en fotokatalysator baserad på iridium kan överföra en elektron till TTC-NO när den belyses med grönt ljus. Detta försvagar en specifik bindning, vilket gör att kväveoxiden släpper och tetrakain återställs till sin aktiva form. Mätningar med spektroskopi och kromatografi bekräftade att TTC-NO nästan helt omvandlas till tetrakain och kväveoxid under dessa förhållanden, samtidigt som den förblir i stort sett oförändrad i mörker. När de två komponenterna kapslades in i miceller förblev partiklarna stabila, omkring 80 nanometer i diameter, och frigjorde endast sitt innehåll vid bestrålning, vilket visar att konceptet ”läkemedel i bur” kan styras utifrån med ljus.
Hjälper infekterade sår att läka snabbare
Teamet gick sedan vidare till möss med hudsår som avsiktligt infekterats med meticillinresistent Staphylococcus aureus (MRSA), en problematisk sjukhusbakterie. Vissa sår fick standardbehandlingar som antibiotika eller tillväxtfaktor, medan andra behandlades med TTC-NO-miceller, med eller utan ljus. När ljuset slogs på minskade TTC-NO-systemet kraftigt bakterieantalet, dämpade inflammation, stimulerade ny blodkärlsbildning och ökade kollageninlagring — alla viktiga för korrekt läkning. Sår behandlade på detta sätt stängdes snabbare och mer fullständigt än de som fick enbart tetrakain eller miceller som hölls i mörker, och prestandan var jämförbar med ett förstahandsantibiotikum. Viktigt är att säkerhetskontroller inte visade några större skador på organ eller blodkemi.
Lindra smärta och tysta nervsignaler
Eftersom infektion och vävnadsskada kraftigt aktiverar smärtbanor mätte forskarna noggrant smärtrelaterat beteende i samma sårmodell. Traditionell tetrakain ökade kortvarigt den kraft som krävdes för att utlösa ett smärtsvar men avtog inom några timmar. TTC-NO-miceller aktiverade med ljus gav däremot lindring i upp till 12 timmar. Mikroskopiska studier av nervknippen nära ryggmärgen och aktivitetsinspelningar i hjärnans sensoriska cortex visade att den kombinerade behandlingen dämpade urladdningen hos smärtkännande neuroner långt efter att ren tetrakain förlorat sin effekt. Ytterligare experiment antydde att den förlängda effekten berodde på minskad bakteriemängd och inflammation från kväveoxiden, inte enbart från nervbedövning.
Skydda smärtsamma infekterade leder
Forskarna testade också systemet i möss med septisk artrit, en svår MRSA-infektion inne i knäleden som ger svullnad, bentapp och intensiv smärta. Ljusaktiverade TTC-NO-miceller minskade ledens bredd, skar ner bakterieantalet och skyddade benstrukturen som visats med högupplösta skanningar. Nivåerna av skadliga inflammatoriska molekyler i blodet sjönk, medan skyddande signalmolekyler ökade. Beteendemässigt kunde behandlade möss tolerera starkare mekaniskt tryck på den drabbade tassen och rörde sig friare i en öppen arena, vilket återigen visade längrevarig lindring än enbart tetrakain. Nerv- och hjärnmätningar speglade dessa beteendemässiga förbättringar, vilket indikerar en bred dämpning av smärtbanor utan uppenbar lokal eller systemisk toxicitet. 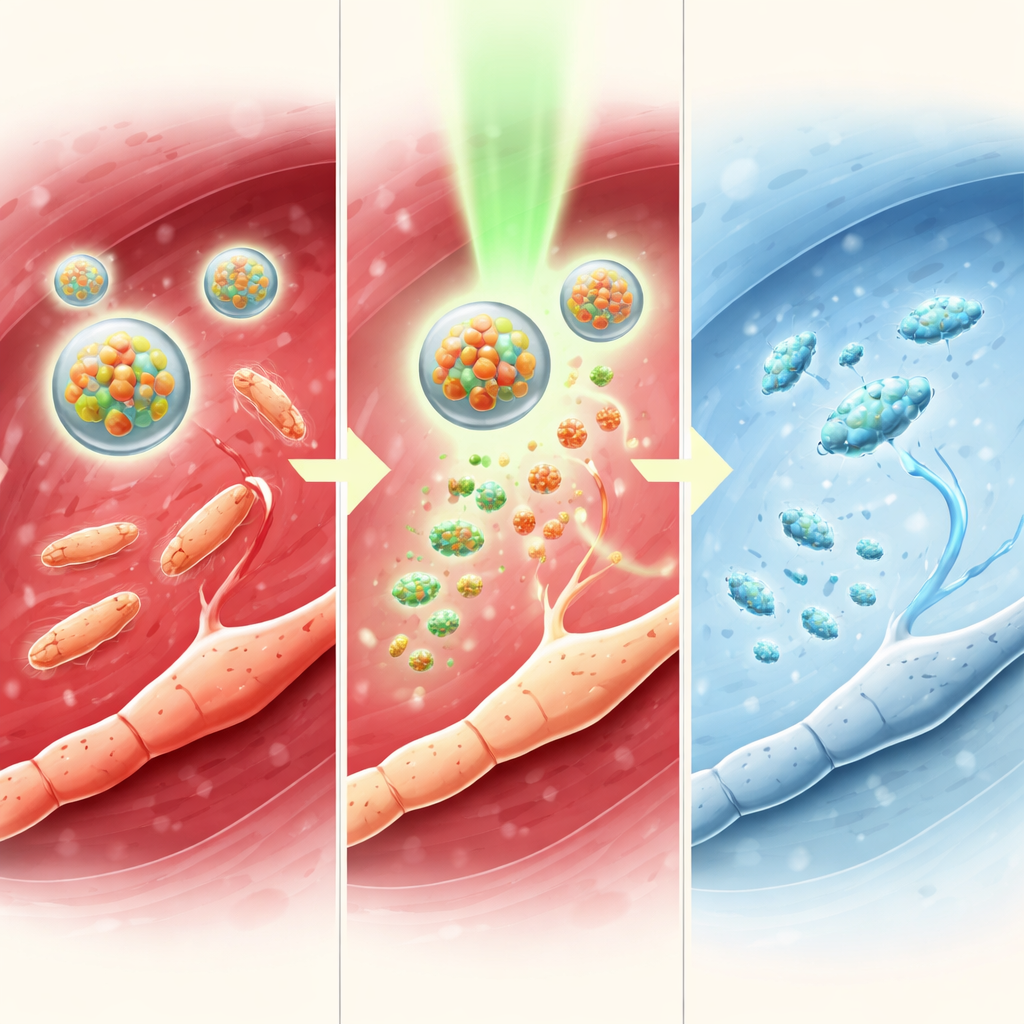
Vad detta kan innebära för patienter
Sammantaget visar arbetet ett enda ljusaktiverat nanosystem som både kan rensa envisa bakterieinfektioner och avsevärt minska den associerade smärtan. Genom att kemiskt ”bura in” ett lokalbedövningsmedel i en kväveoxid-frigörande struktur och paketera det i miceller uppnår författarna lokal, styrd frisättning av två verksamma ämnen på begäran med milt synligt ljus. I djurmodeller för hudsår och ledinfektioner påskyndar denna design läkning och förlänger smärtlindring bortom vad ett konventionellt lokalbedövningsmedel kan erbjuda. Mycket testande återstår innan mänsklig användning, men studien belyser hur smarta, omkopplingsbara läkemedel en dag kan göra infektionsbehandling både mer effektiv och bekvämare.
Citering: Zhang, J., Gan, G., Cao, C. et al. Drug-caged drugs enable photocatalytic dual decaging of nitric oxide and anesthetics for antibacterial analgesia. Nat Commun 17, 2843 (2026). https://doi.org/10.1038/s41467-026-69624-5
Nyckelord: kväveoxidterapi, ljusaktiverade läkemedel, antibakteriell analgesi, nanomedicin, MRSA-infektioner