Clear Sky Science · sv
Treg-γδ T-cellaxen avgör sexuell dimorfism i hepatocarcinogenes
Varför vissa levercancerformer drabbar män hårdare
Läkare har länge vetat att levercancer drabbar män ungefär dubbelt så ofta som kvinnor, men förklaringarna sträcker sig bortom enkla skillnader i könshormoner. Denna studie går på djupet i de immunceller som finns inne i levertumörer och avslöjar en dold dialog mellan två typer av T‑celler som hjälper till att förklara varför manliga leverar är mer sårbara — och hur den kunskapen kan peka mot nya, mer skräddarsydda behandlingar.
Immunets dragkamp inne i levertumörer
Levercancer, särskilt hepatocellulärt karcinom, växer i ett komplext grannskap av immunceller, blodkärl och ärrvävnad. Författarna jämförde tumörer från män och kvinnor, både hos patienter och i musmodeller, och fann en slående obalans: manliga tumörer var fulla av fler regulatoriska T‑celler, eller Tregs, en celltyp som normalt hjälper till att dämpa överdrivna immunsvar. Samtidigt skilde sig inte det totala antalet andra vanliga T‑celler mycket mellan könen. Eftersom höga nivåer av Tregs kopplades till sämre överlevnad, misstänkte teamet att dessa celler inte bara är åskådare utan aktiva medhjälpare som hjälper tumörer att undkomma immunsystemet. 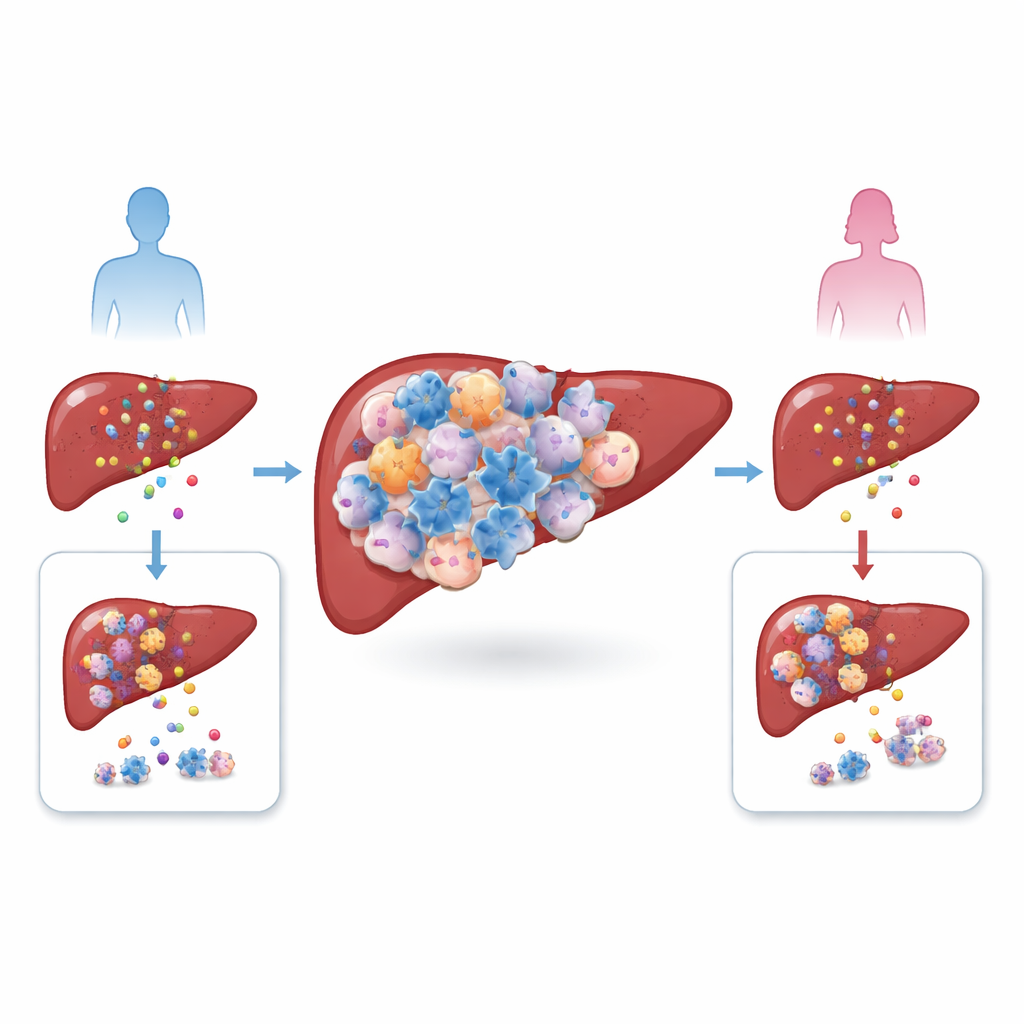
Hur manliga hormoner lockar in suppressorceller
För att förstå varför manliga tumörer attraherar fler Tregs fokuserade forskarna på kemiska signaler som produceras av cancercellerna. De fann att manliga levertumörer producerade högre mängder av en molekyl som kallas Ccl2, medan Tregs bar mer av dess matchande receptor, Ccr2. Det här paret fungerar som en hemhämtningssignal som drar Tregs in i tumören. När Ccl2‑signalen eller Ccr2‑receptorn avlägsnades i möss krympte tumörerna och betydligt färre Tregs tog sig in i levern, särskilt hos hanar. Teamet visade sedan att testosteron, det huvudsakliga manliga könshormonet, driver denna process: det aktiverar en kedja av proteiner i levercancerceller som slår på Ccl2‑genen och förstärker den kemiska kallelsen som lockar Tregs. Kastrerade hanmöss, som producerar mindre testosteron, hade lägre Ccl2 i sina tumörer och färre infiltrerande Tregs.
Vaktceller som skulle kunna bekämpa cancer — men hålls tillbaka
En annan typ av T‑cell, känd som gammadelta‑T‑celler, kan fungera som snabba ”vakter” som känner igen och dödar tumörceller utan det vanliga antigenvisningsmaskineriet. I frisk lever är dessa celler relativt få, men i levercancer kan de vara kraftfulla tumörbekämpare. Studien visade att kvinnliga tumörer innehöll fler av dessa gammadelta‑celler och att de var mer aktiva och bättre beväpnade med toxiska molekyler. Att ta bort manliga könshormoner i möss ökade antalet och vigören hos gammadelta‑celler i tumörer, medan de klassiska mördarcellerna, CD8‑T‑celler, i stort sett förblev oförändrade. I odlingsskålar skadade gammadelta‑celler lätt levercancerceller, men denna effekt försvagades när Tregs tillsattes, vilket tyder på att Tregs specifikt bromsar denna lovande antitumörpopulation.
Hypoxi, sändningar i paket och tysta försvarare
När forskarna gick djupare undrade de hur Tregs lyckas dämpa gammadelta‑T‑celler. Inne i tumörer är syre ofta knapp, ett tillstånd som kallas hypoxi. Under dessa låga syreförhållanden började Tregs i manliga tumörer producera stora mängder av ett protein som kallas S100a4. Istället för att fungera direkt som en fri molekyl packades S100a4 i små membranbundna partiklar kända som extracellulära vesiklar. Dessa vesiklar knoppade av från Tregs och togs upp av närliggande gammadelta‑T‑celler. Väl inne i cellerna omprogrammerade S100a4 deras genetiska kontrollsystem: det minskade öppenheten i DNA‑regioner som reglerar nyckelsignalering och mördarmolekyler och sänkte deras aktivitet. Gammadelta‑cellerna blev mindre kapabla att reagera via sina T‑cellsreceptorer och mindre benägna att frisätta toxiska proteiner och cytokiner, vilket effektivt slöade ned deras antikancerförmåga. 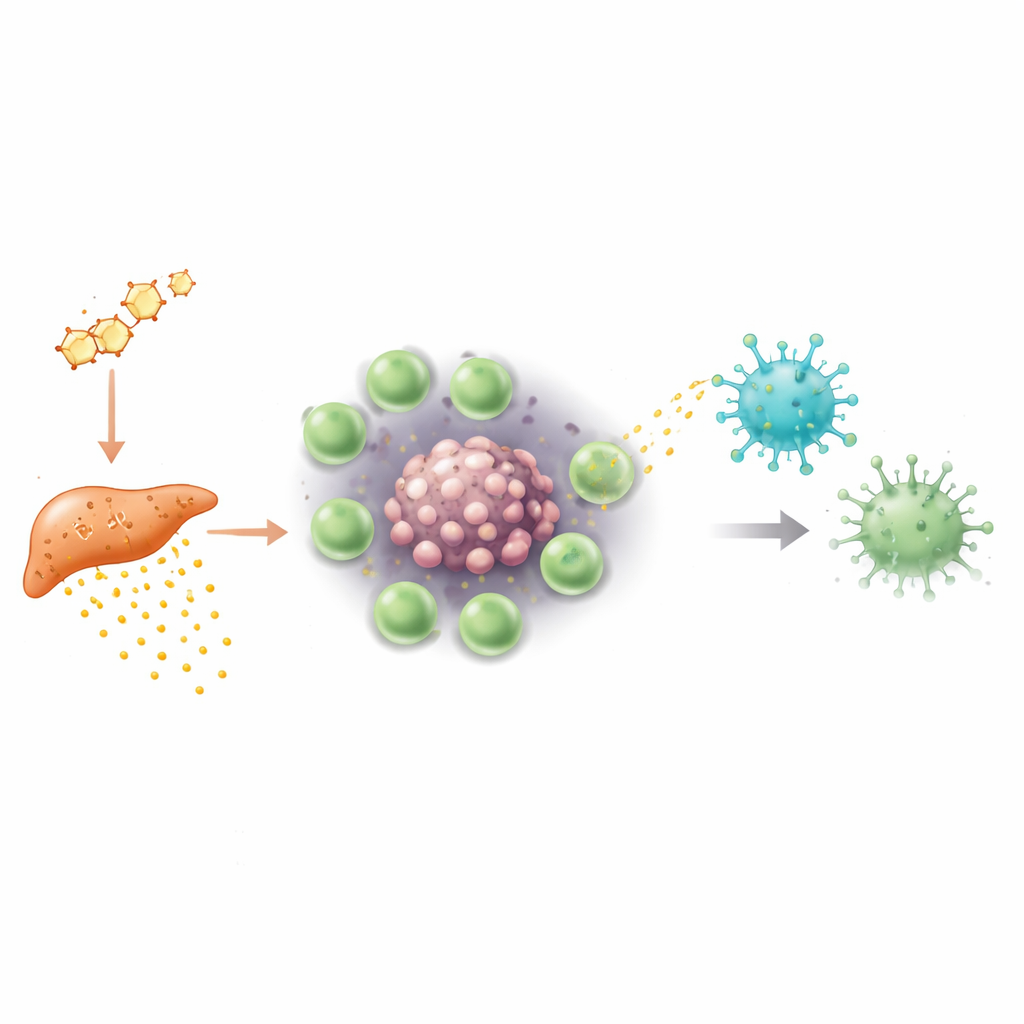
Bryta den skadliga kretsen
Slutligen testade teamet vad som händer om denna Treg–S100a4–gammadelta‑axel avbryts. I möss som är konstruerade så att Tregs inte kan producera S100a4 krympte manliga levertumörer, den totala S100a4‑nivån i tumörerna föll, och gammadelta‑T‑celler blev både fler och mer aktiva. Noterbart var att antalet Tregs i tumören inte minskade — bara deras hämmande effekt på gammadelta‑celler lyftes. Denna förändring suddade nästan ut den vanliga skillnaden i tumörsvårighetsgrad mellan han‑ och honmöss, vilket understryker hur central denna bana är för könsbaserade skillnader i levercancer.
Vad detta betyder för framtida behandlingar
Enkelt uttryckt visar studien att manliga hormoner får levercancerceller att skicka ut starkare ”välkomstsignaler” för immunsuppressiva Tregs. När dessa väl är inne i tumören — och under syrebristens stress — skickar Tregs ut S100a4‑fyllda vesiklar som tyst avväpnar närliggande gammadelta‑T‑celler, vilka annars skulle kunna hålla cancern i schack. Genom att rikta in sig antingen på Ccl2‑signalen som lockar Tregs eller på S100a4‑budskapen som tystar gammadelta‑celler, skulle framtida terapier kunna återställa kroppens egna försvar, särskilt hos män. Arbetet antyder att levercancerbehandlingar kan vinna på att vara könsspecifika och på att utnyttja, snarare än förbise, gammadelta‑T‑cellernas unika styrkor.
Citering: Liang, Q., Zhang, Q., Zhang, W. et al. Treg-γδ T cell axis determines sexual dimorphism in hepatocarcinogenesis. Nat Commun 17, 2640 (2026). https://doi.org/10.1038/s41467-026-69603-w
Nyckelord: hepatocellulärt karcinom, regulatoriska T‑celler, gammadelta‑T‑celler, könsskillnader, tumörimmunologi