Clear Sky Science · sv
Pyrimidinergetisk kalciumsignalering kopplar tubulär metabolism till fibros i njursjukdom
Varför ärrbildning i njuren spelar roll
Kronisk njursjukdom drabbar tyst hundratals miljoner människor världen över och slutar ofta med att njurarna blir ärriga och stela. När denna ärrbildning, kallad fibros, väl etablerats är förlorad njurfunktion svår att återfå. Ändå saknas fortfarande läkemedel som specifikt stoppar fibros. Denna studie ställer en enkel men avgörande fråga: hur övergår kortvarig skada på njurens filtrerande tubuli gradvis till bestående ärrvävnad, och skulle avbrott i den kedjan kunna bromsa eller förhindra njursvikt?
Upptagna njurtubuli och deras dolda kemi
Njurens proximala tubuli är mikroskopiska arbetsbin som återtar största delen av vatten och näringsämnen som filtrerats från blodet. För att driva detta arbete är deras kemi ovanligt aktiv. Genom att analysera enkelcells-geneuttrycksdata från musnjurar fann forskarna att dessa tubuliceller är särskilt rika på gener som hanterar pyrimidiner, en familj småmolekyler som normalt hjälper till att bygga och reparera DNA och RNA. I skadade tubuli var ett enzym i en ”salvage”-väg, cytidin-deaminas, kraftigt uppreglerat, vilket tyder på att skadade celler omorganiserar pyrimidinanvändningen för att fylla på vissa energirika byggstenar, inklusive en förening kallad UDP.
Signaler som läcker ut från skadade celler
När teamet skadade mänskliga tubuliliknande celler i kultur med toxiner som efterliknar cytostatika eller folsyraöverdos, släppte cellerna ut UDP i omgivande vätska. I faktiska musnjurar utsatta för skada visade färgning av vävnadsnitt både höga nivåer av det pyrimidinhanterande enzymet i tubuli och tecken på att närliggande stödjeceller, så kallade fibroblaster, aktiverades och förändrade form. Fibroblaster sitter normalt tysta mellan tubuli, men när de aktiveras förökar de sig och hjälper till att lägga ner kollagen och andra fibrer som förtjockar och styvar upp njurvävnaden. Dessa observationer föreslog en enkel idé: skadade tubuli kan ”läcka” kemiska nödsignaler som närliggande fibroblaster kan uppfatta.
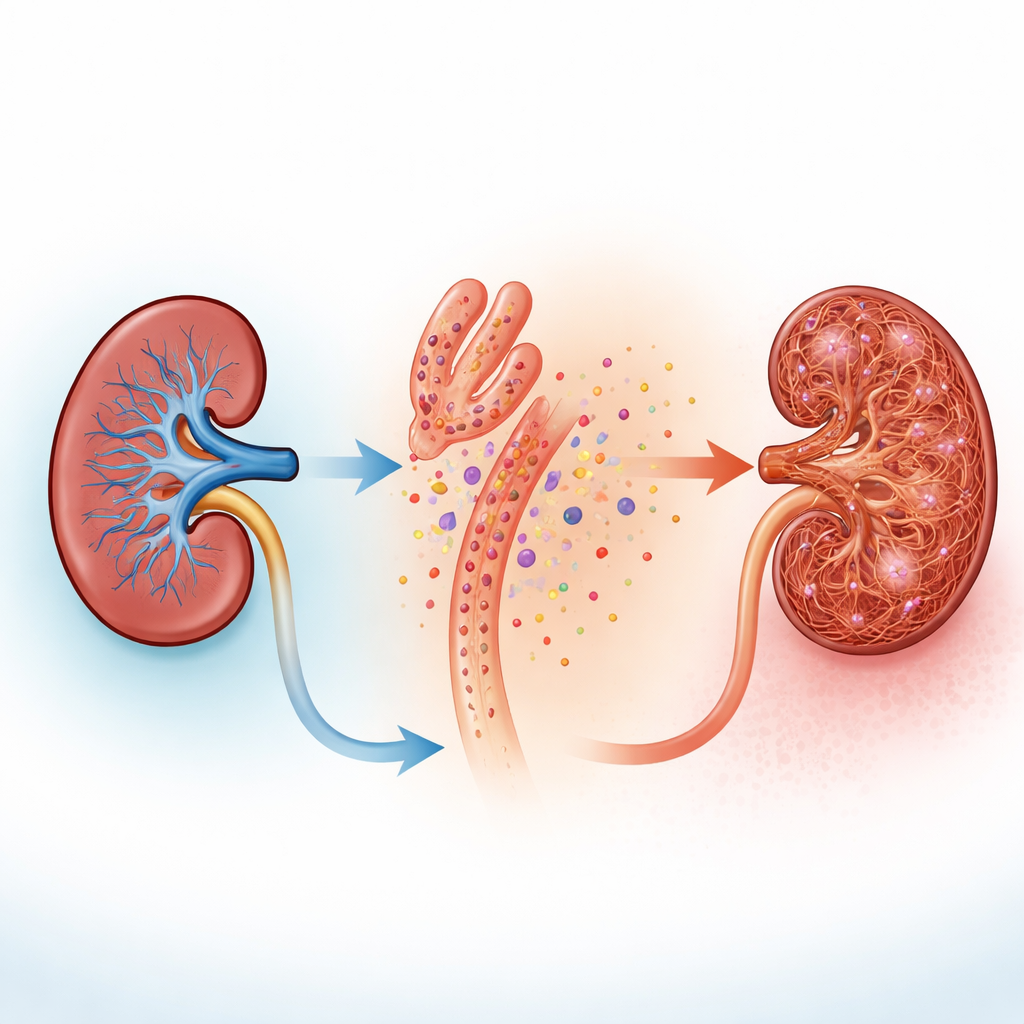
Hur fibroblaster lyssnar med kalciumblixtar
De misstänkta ”öronen” på fibroblaster är P2Y6-receptorer, ytproteiner som svarar på UDP. Genom att gräva i flera enkelcellsdataset såg författarna att P2Y6 fanns på stromaceller och ökade ytterligare i musmodeller för kronisk njursjukdom. Mätningar över hela njurar bekräftade kraftiga ökningar av P2Y6-nivåer i två olika ärrbildningsmodeller. I färska njursnitt och i odlade njurfibroblaster som varit konstruerade för att lysa när kalcium i cellen stiger, gav tillförsel av UDP eller ett P2Y6-aktiverande läkemedel snabba kalciumtoppar. Dessa blixtar startade i de långa, tunna utskotten som omger tubuli och svepte sedan in i cellkroppen, och de försvann när P2Y6 blockerades eller kalcium kemiskt bundits upp. I levande möss visade högupplöst intravitalkomikroskopi att fibroblaster runt tubuli uppvisar frekvent, oregelbunden kalciumaktivitet som ökar dramatiskt när tubuli skadas, samtidigt som tubulicellerna själva tystnar.
Från kortvariga signaler till bestående ärr
Kalciumutbrott inne i en cell är inte bara fyrverkeri; de kan omprogrammera beteendet. När fibroblaster i kultur badades i ett P2Y6-aktiverande ämne förökade de sig snabbare, rörde sig mer och slog på gener kopplade till ett mer aggressivt, ”myofibroblastiskt” tillstånd. Dessa gener kodar proteiner såsom fibronectin, vimentin och kollagen som direkt bidrar till ärrbildning. Blockering av P2Y6 eller att förhindra kalciumökningar raderade dessa förändringar, och nedreglering av receptorens gen dämpade svaret. I möss visade två distinkta former av njurskada—uretärobstruktion och folsyra-nefropati—samma mönster: skadade njurar hade fler prolifererande fibroblaster, fler myofibroblastmarkörer, mer kollagen och större områden med fibros.
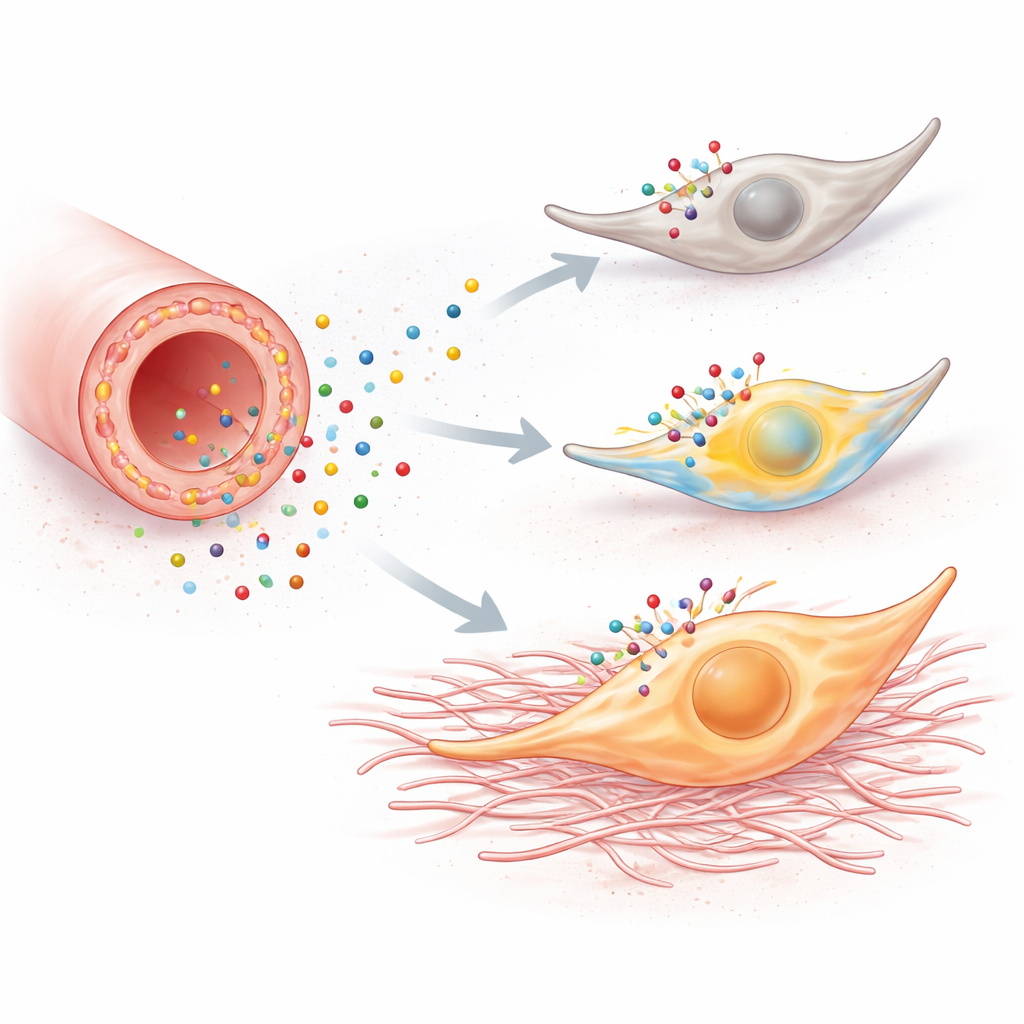
Dämpa skadlig signalering
För att pröva om denna väg inte bara är närvarande utan faktiskt skadlig, tog forskarna antingen bort P2Y6 genetiskt eller blockerade den med ett läkemedel. Möss utan receptorn utvecklade mindre njurfibros efter uretärobstruktion eller folsyreskada: deras fibroblaster förökade sig mindre, de lade ner mindre fibrös matrix och rekryterade färre inflammatoriska celler. Blodprover visade att dessa knockout-djur också bevarade bättre njurfiltreringsfunktion. Behandling av normala möss med en P2Y6-blockerande förening gav jämförbart skydd, inklusive dämpad kalciumaktivitet i fibroblaster och minskad ärrbildning, även om förbättringar i blodmarkörer var mer variabla.
Vad detta betyder för framtida behandlingar
Sammantaget avslöjar arbetet en enkel men kraftfull händelsekedja. När njurtubuliceller skadas ändrar de sin interna kemi och släpper ut UDP i omgivande vävnad. Närliggande fibroblaster upptäcker denna molekyl genom sina P2Y6-receptorer, svarar med kalciumutbrott inne i cellen och går sedan in i ett ärrbildande läge—de förökar sig, migrerar och lägger ner kollagen. Att avbryta denna pyrimidinbaserade kalciumsignalering, särskilt vid P2Y6-steget, minskar kraftigt fibros i flera musmodeller. För patienter pekar detta mot ett nytt slags läkemedelsmål: föreningar som selektivt blockerar P2Y6 i njuren skulle kunna hjälpa till att bryta länken mellan vanliga njurskador och den långsamma, irreversibla ärrbildning som leder till kronisk njursjukdom.
Citering: Figurek, A., Jankovic, N., Kollar, S. et al. Pyrimidinergic calcium signaling links tubular metabolism to fibrosis in kidney disease. Nat Commun 17, 3004 (2026). https://doi.org/10.1038/s41467-026-69602-x
Nyckelord: kronisk njursjukdom, renal fibros, fibroblastsignalering, pyrimidinmetabolism, P2Y6-receptor