Clear Sky Science · sv
Dubbel rekrytering av två CCM2-molekyler till KRIT1 undertrycker KLF4-uttryck
Varför hjärnans blodkärl behöver noggrann kontroll
Blodkärlen i hjärnan balanserar mellan två krav: de måste vara robusta nog för att undvika läckage men samtidigt tillräckligt flexibla för att svara på kroppens behov. När denna balans rubbas kan människor utveckla cerebrala kavernösa missbildningar—ansamlingar av sköra, bubbliga blodkärl som kan blöda och orsaka anfall eller stroke. Denna studie avslöjar ett tidigare okänt molekylärt handslag mellan tre proteiner som hjälper till att hålla hjärnans kärl stabila, och visar hur ett avbrott i detta handslag kan driva sjukdomsutveckling.
Kassörerna för kärlhälsa
Cellernas beklädnad av blodkärlen styrs av ett par huvudbrytare, kallade KLF2 och KLF4, som reglerar gener som upprätthåller kärlens styrka och identitet. Om dessa brytare blir överaktiverade blir kärlen abnorma och mer sårbara för skada. Två andra proteiner, KRIT1 och CCM2, är kända för att vakta detta system. Personer som ärver felaktiga versioner av något av dessa proteiner har hög risk för cerebrala kavernösa missbildningar. Fram tills nu har forskare dock inte förstått exakt hur KRIT1 och CCM2 samarbetar för att hålla KLF4 i schack.
Ett förvånande team av tre
Forskarna använde humana endotel-liknande celler odlade i laboratorium och minskade selektivt mängden CCM2 eller KRIT1 med genetiska verktyg. När något av proteinerna utarmades steg KLF4-nivåerna dramatiskt, vilket efterliknar vad som ses i djurmodeller och hos patienter. Återställande av normala nivåer av CCM2 eller KRIT1 sänkte KLF4 igen—men bara om de återinsatta proteinerna fortfarande kunde binda till varandra. Genom att konstruera precisa förändringar i de regioner där CCM2 och KRIT1 interagerar visade teamet att denna fysiska kontakt är avgörande för att förhindra KLF4-uppreglering. Dessa experiment placerar entydigt KRIT1–CCM2-partnerskapet i centrum för kontrollsystemet för denna kraftfulla transkriptionsfaktor.
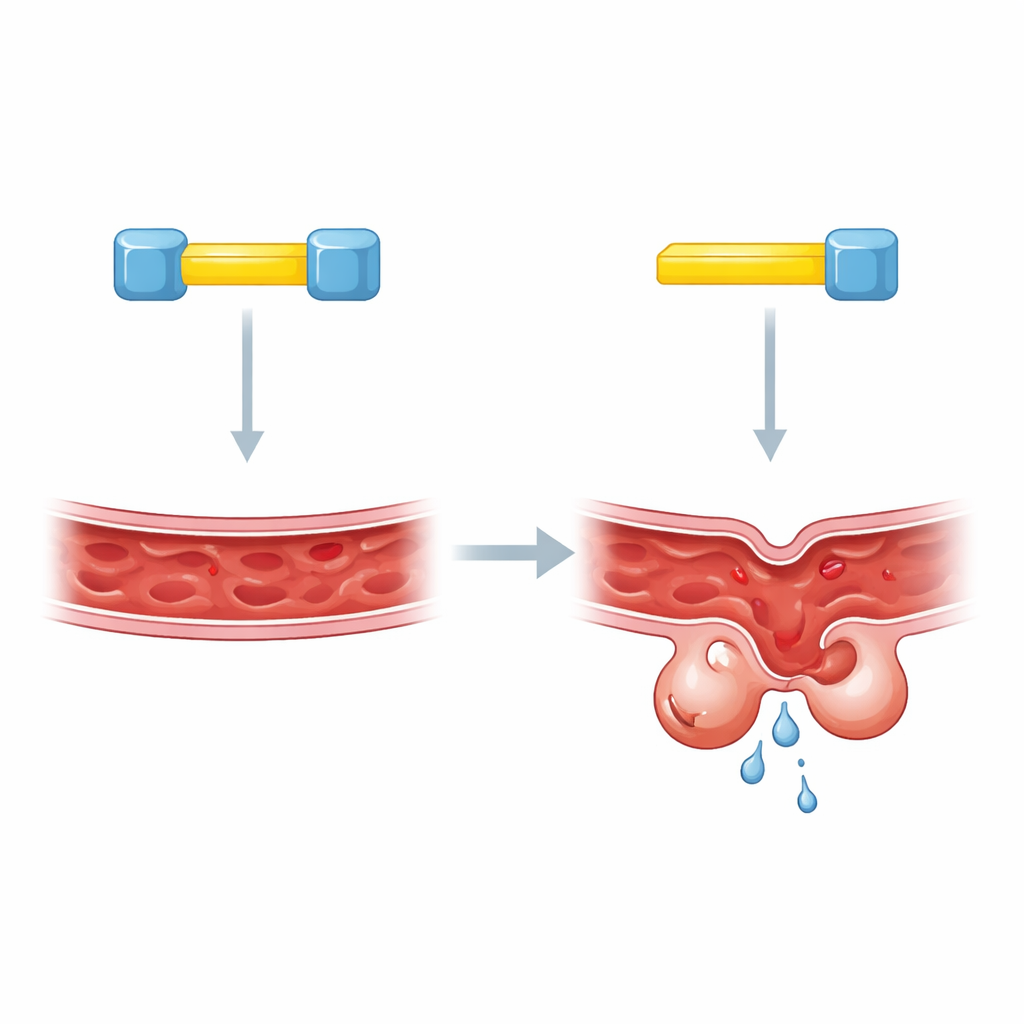
Två lås på en nyckel
För att gå djupare fokuserade författarna på korta segment inom KRIT1 som fungerar som molekylära dockningsplatser. Tidigare arbete föreslog att CCM2 fäster vid KRIT1 vid en av dessa platser, men olika metoder hade gett motstridiga svar om vilken det var. Den nya studien visar att förvirringen uppstod eftersom verkligheten är mer komplex: KRIT1 bär två närliggande dockningssegment, och båda behövs. När något av segmenten stördes förblev KLF4-nivåerna onormalt höga, precis som om KRIT1 saknades helt. Biokemiska tester i konstruerade celler visade att ett enda KRIT1-protein kan länka samman två separata CCM2-molekyler samtidigt, vilket antyder en oväntad treparts-uppbyggnad.
Att se den molekylära klämman i detalj
Teamet renframställde sedan de relevanta delarna av CCM2 och KRIT1 och undersökte hur de går ihop i lösning och i kristaller. Mätningar av komplexets massa indikerade att två kopior av en nyckelregion i CCM2 binder till en enda remsa av KRIT1 som bär paret av dockningsställen. Högupplösta strukturbilder bekräftade denna 2:1-ordning: ett förlängt KRIT1-peptid tränger sig mellan två CCM2-domäner, där varje dockningsplats vilar i en liknande ficka på en separat CCM2-molekyl. Ett kort helixsegment mellan dockningsställena hjälper till att positionera de två CCM2-domänerna sida vid sida och skapar en tät, klämoliknande struktur. Denna typ av dubbelbindning—två bindningsdomäner som hakar fast i tandade platser längs en partner—har inte tidigare observerats för denna familj av proteinmoduler.
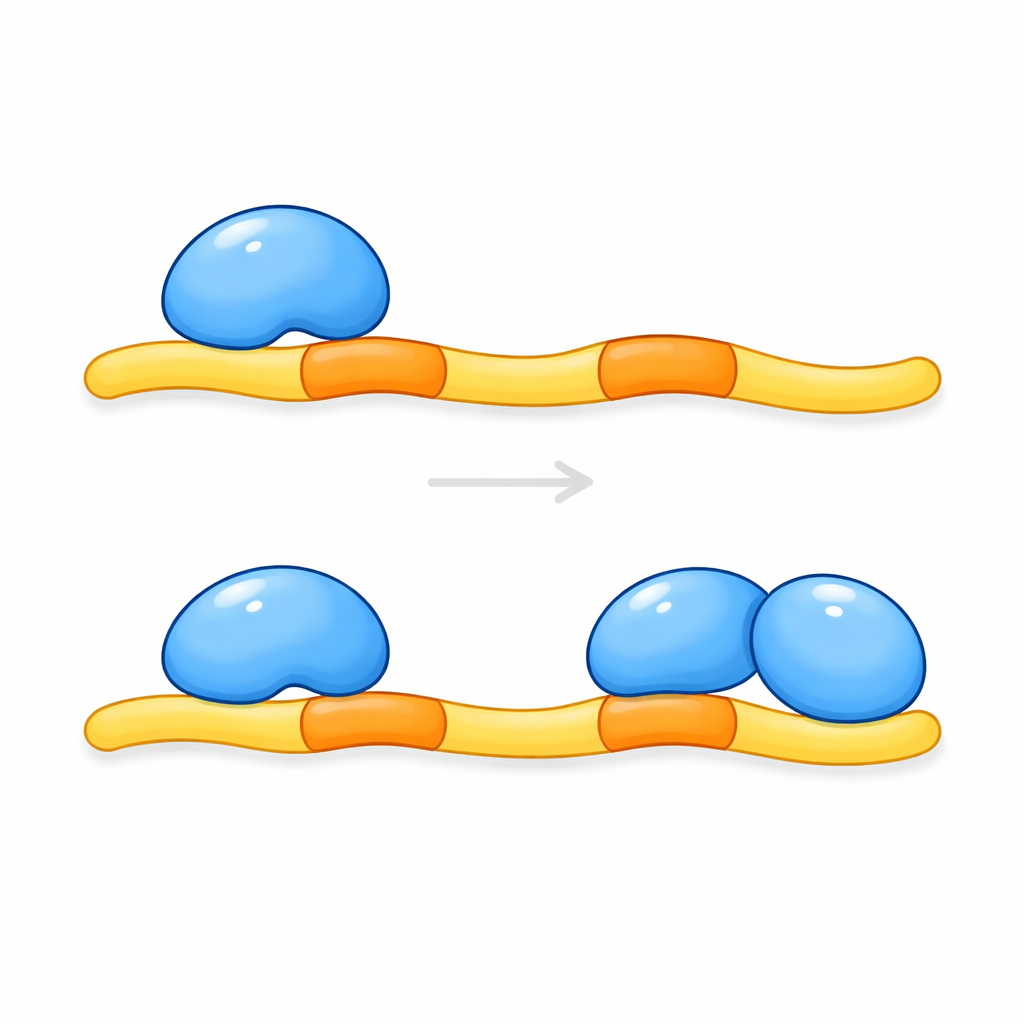
Konsekvenser för hjärnsjukdom och vidare
Dessa fynd visar att KRIT1 inte bara binder en CCM2-molekyl; istället fungerar det som ett ramverk som rekryterar ett par CCM2-proteiner. Först när båda dockningsställena på KRIT1 är upptagna kan komplexet effektivt hämma KLF4-produktionen och därigenom bidra till att förebygga spridning av sköra kärl. Mutationer i KRIT1 som stör något av dockningsställena förväntas därför försvaga denna skyddande klämma och kan förklara vissa ärftliga former av cerebrala kavernösa missbildningar. Eftersom många andra humana proteiner bär liknande tvillingdockningsmotiv antyder studien också en bredare princip: dubbelbindning av par av besläktade domäner kan vara ett vanligt sätt för celler att finslipa signalnätverk. Att förstå denna trepartsinteraktion kan i slutändan vägleda strategier för att stabilisera blodkärl hos personer med risk för hjärnblödningar.
Citering: Huet-Calderwood, C., Fisher, O.S., Das, S. et al. Dual recruitment of two CCM2 molecules to KRIT1 suppresses KLF4 expression. Nat Commun 17, 2719 (2026). https://doi.org/10.1038/s41467-026-69595-7
Nyckelord: cerebrala kavernösa missbildningar, endotelceller, KRIT1, CCM2, KLF4