Clear Sky Science · sv
Kontrastfri identifiering av gliomets blod‑hjärnbarriärstatus via generativ diffusion‑AI och icke‑kontrast‑MRI
Varför detta är viktigt för patienter med hjärntumörer
Personer med hjärntumörer genomgår rutinmässigt MR‑undersökningar, och många får även injicerat kontrastradiofärg för att läkare ska kunna se om hjärnans skyddande blod‑hjärnbarriär har skadats. Den informationen styr kirurgi, strålbehandling och prognos – men färgen kan medföra risker, ökar tid och kostnad och finns inte alltid tillgänglig. Denna studie presenterar ett artificiellt intelligens (AI)‑system som läser vanliga, färgfria MR‑bilder och virtuellt återskapar de saknade kontrastbilderna, så att läkare kan dra slutsatser om blod‑hjärnbarriärens status utan att injicera något kontrastmedel.
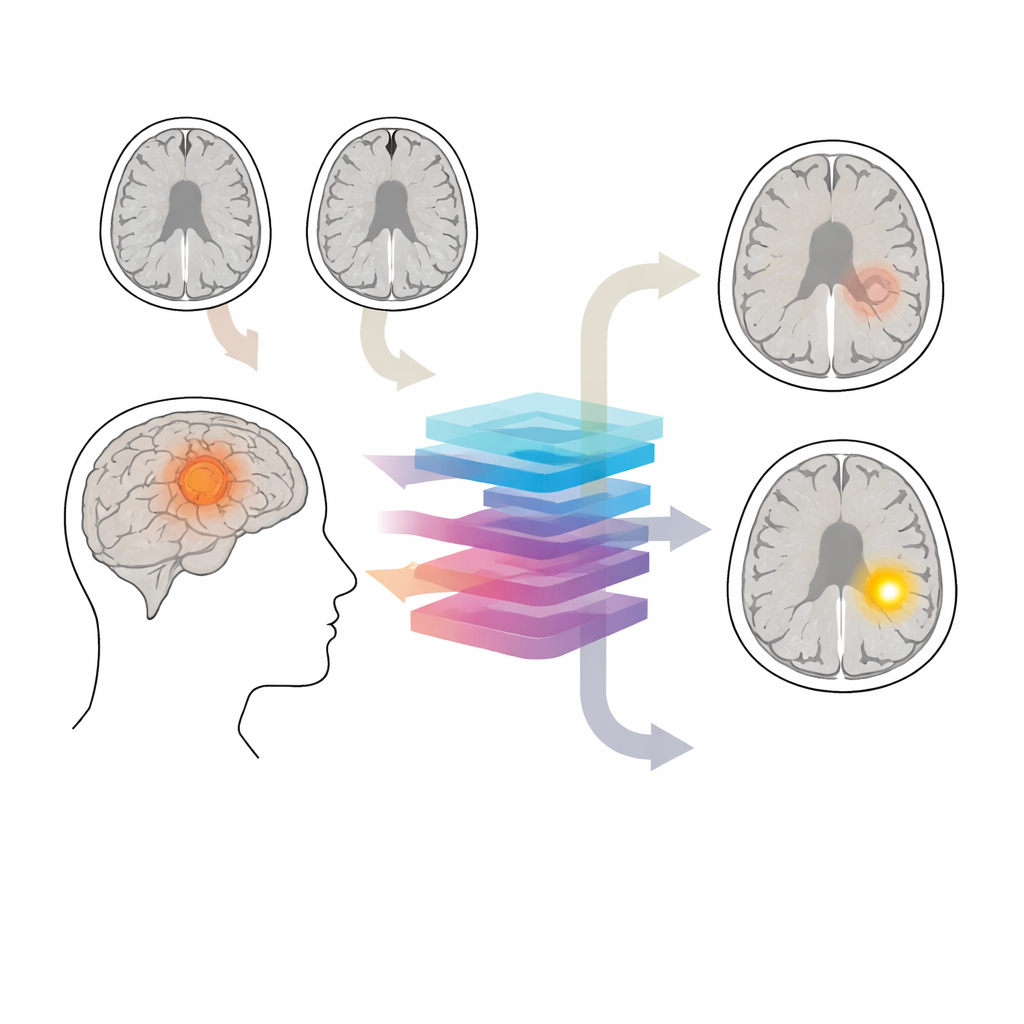
Hjärnans skyddande grindvakt
Blod‑hjärnbarriären fungerar som ett mikroskopiskt filter runt blodkärlen i hjärnan och släpper bara igenom mycket små molekyler. I många gliom tumörer blir denna barriär läckande. På standardiserade kontrast‑MRI lyser läckande områden upp efter injektion, medan intakta regioner förblir mörka. Dessa mönster påverkar hur aggressivt en tumör behandlas och hjälper till att definiera vad som ska avlägsnas kirurgiskt eller riktas med strålning. Ändå hoppar man ibland över kontrastundersökningar – till exempel i tidiga utredningar eller vid långtidsuppföljning av långsamt växande tumörer – och vissa patienter bör undvika kontrast helt på grund av njursjukdom, allergiska reaktioner eller oro för gadolinium‑deposition i hjärnan.
Att förvandla vanliga skanningar till virtuellt kontrast
Författarna undersökte om icke‑kontrast MR‑bilder, som redan ofta tas, innehåller tillräckligt subtil information för att AI ska kunna härleda vad en kontrastbild skulle ha visat. De fokuserade på två vanliga sekvenser: T1 och T2‑FLAIR. Även om dessa inte direkt visar blod‑hjärnbarriärens läckage fångar de tumörstruktur, omgivande svullnad och vävnadsskada som ofta följer med barriärsönderfall. Teamet byggde ett system kallat CBSI som först genererar syntetiska kontrastförstärkta bilder från dessa icke‑kontrastbilder och sedan använder dem, tillsammans med originalbilderna, för att avgöra om barriären är intakt eller störd i varje gliom.
Hur det nya AI‑systemet fungerar
I kärnan av CBSI finns en diffusionsmodell – en typ av AI som börjar från brusiga bilder och iterativt ”avbrusar” dem till realistiska bilder. Här lär den sig att omvandla icke‑kontrastinput till två alternativa virtuella kontrastbilder: en som antar en intakt barriär och en som antar en läckande barriär. En styrmekanism talar om för modellen vilket förstärkningsmönster den ska rikta in sig på, och ett hjälpsätt för segmentering hjälper den att lägga extra fokus på tumörområdet. I ett andra steg jämför ett separat nätverk de två syntetiska utfallen för varje patient och bedömer vilken som är mest självkonsekvent med den ursprungliga MR‑datan. Det beslutet översätts sedan till den förutspådda statusen för blod‑hjärnbarriären.
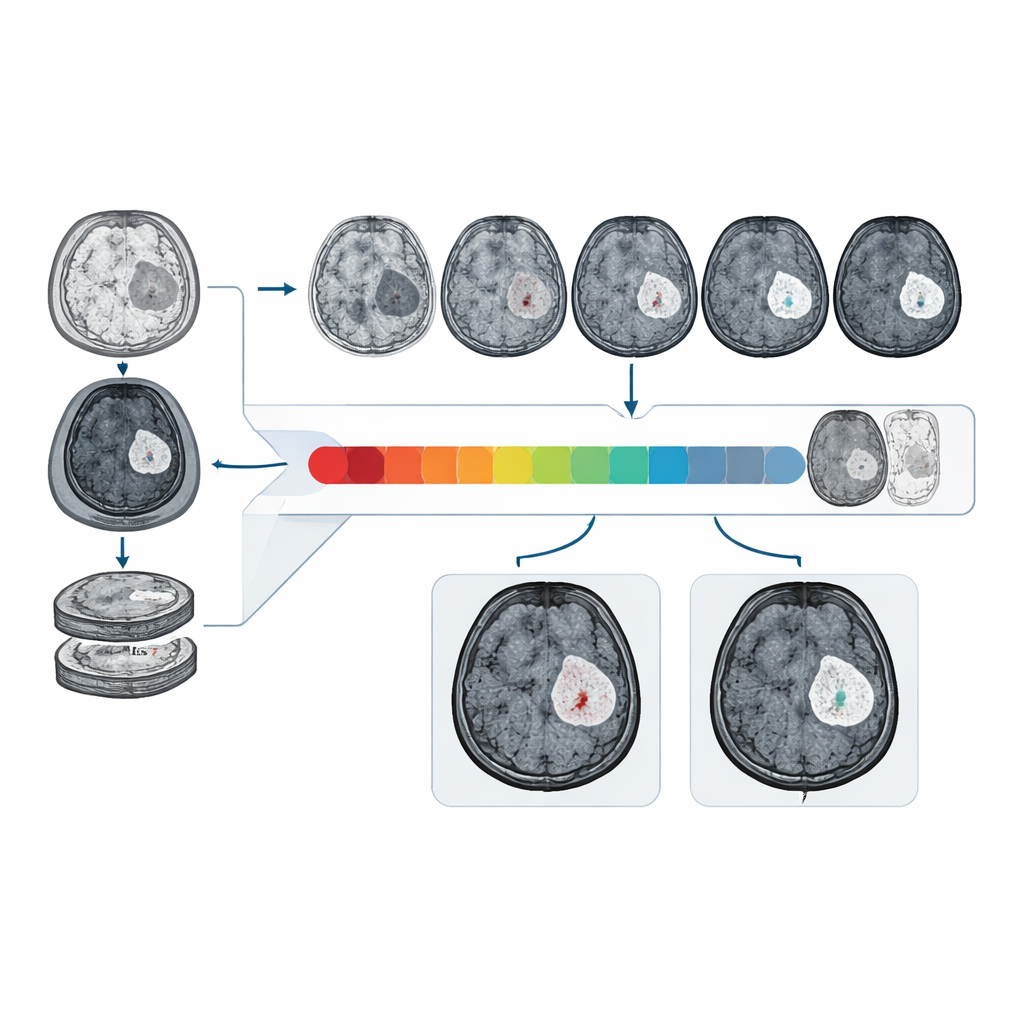
Hur väl det presterar på verkliga och mångsidiga data
Forskarna tränade och testade CBSI på MR‑data från 1 535 gliompatienter insamlade på flera sjukhus och från internationella öppna dataset. På en extern klinisk testuppsättning särskilde CBSI intakta från störda barriärer med ett area under kurvan på cirka 81 %, klart bättre än modeller som enbart förlitade sig på icke‑kontrastbilder och nära prestandan hos modeller som hade tillgång till verkliga kontrastbilder. Radiologer som visades randomiserade blandningar av riktiga och syntetiska kontrastbilder från systemet bedömde över 90 % av de syntetiska bilderna som av hög diagnostisk kvalitet, och deras förmåga att identifiera kontrastförstärkning på syntetiska bilder var liknande deras prestation på riktiga skanningar.
Fördelar för behandlingsplanering och framtida vård
Där de syntetiska kontrastbilderna från CBSI fångar tumördetaljer och förstärkningsmönster förbättrade de också efterföljande uppgifter såsom att avgränsa tumörgränser och uppskatta tumörgrad – båda beroende mycket på hur blod‑hjärnbarriären beter sig. Metoden generaliserade väl till olika scanner‑typer, bildprotokoll och patientgrupper, inklusive data från Subsahariska Afrika och större internationella kohorter. Författarna poängterar att varje djupinlärningssystem fortfarande är ett statistiskt verktyg snarare än ett direkt fönster in i biologin, men deras resultat tyder på att virtuell kontrastavbildning skulle kunna minska beroendet av injicerade medel, särskilt för sårbara patienter eller i miljöer där kontrastundersökningar är svåra att få fram. I praktiska termer skulle detta AI‑angreppssätt kunna göra det möjligt för läkare att utvinna avgörande behandlingsformande information om blod‑hjärnbarriären från de skanningar patienterna redan får – utan ett extra nålstick.
Citering: Zheng, K., Zhang, Y., Shu, H. et al. Contrast-free identification of glioma blood-brain barrier status via generative diffusion AI and non-contrast MRI. Nat Commun 17, 2162 (2026). https://doi.org/10.1038/s41467-026-69578-8
Nyckelord: gliom, blod‑hjärnbarriär, hjärn‑MRI, medicinsk bildbehandlings‑AI, kontrastfri avbildning