Clear Sky Science · sv
Nanobody‑baserade IgG hämmar samtidigt den allergena och enzymatiska aktiviteten hos den dominerande honungsbietoxinallergenen
Varför bistickallergier är viktiga
För de flesta är ett bistick smärtsamt men snabbt övergående. För andra kan det utlösa en livshotande helkroppsreaktion som kallas anafylaxi. Dagens huvudsakliga förebyggande behandling, venomimmunterapi, fungerar för många patienter men tar år, kräver frekventa injektioner och kan i sig framkalla allergiska biverkningar. Denna studie undersöker ett nytt, mer riktat sätt att skydda personer som är allvarligt allergiska mot honungsbietoxin genom att oskadliggöra en nyckelkomponent i giftet innan den kan orsaka skada.
Huvudboven i bisticket
Honungsbietoxin är en blandning av olika molekyler, men ett protein, kallat fosfolipas A2 (eller Api m 1), står ut. Det är den dominerande allergenen hos patienter med honungsbietallergi och finns hos nästan alla dem. Api m 1 har en dubbel funktion: det skadar cellmembran, vilket bidrar till smärta och inflammation vid stickstället, och det är också ett huvudmål för allergiframkallande antikroppar kallade IgE. När Api m 1 binder till IgE som är förankrade på immunceller som mastceller och basofiler kan det sätta igång en kedjereaktion som leder till ett plötsligt utsläpp av inflammatoriska ämnen och i svåra fall anafylaxi.
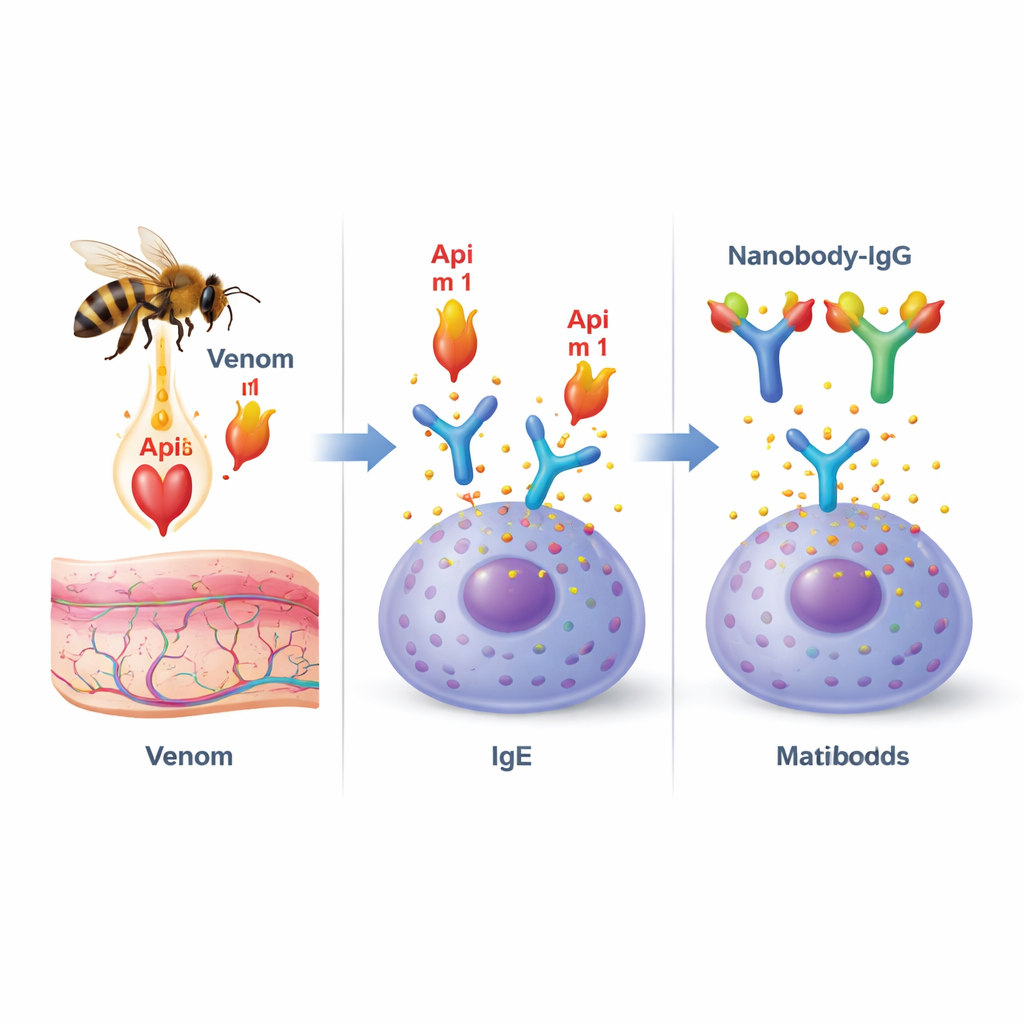
Designa små antikroppar för att blockera allergenen
Forskarna vände sig till ”nanobodies”, små, stabila antikroppsfragment som ursprungligen upptäcktes hos kameldjur. Eftersom de är små och avlånga passar nanobodies särskilt bra för att tränga in i fåror och fickor på proteiner. Teamet isolerade Api m 1‑specifika nanobodies från ett immunbibliotek och valde ut två framstående kandidater, benämnda AM1‑1 och AM1‑4. Detaljerade strukturarbeten med röntgendiffraktion visade att dessa två nanobodies klämmer fast på motsatta sidor av Api m 1 och inte stör varandra. En nanobody, AM1‑1, sitter rakt över enzymets aktiva centrum, vilket tyder på att den kan blockera Api m 1:s membranskadande funktion, medan AM1‑4 fäster i en separat ficka på proteinets yta.
Göra nanobodies till kraftfulla blockerare
För att förvandla dessa små bindare till långtidsverkande läkemedel fäste forskarna varje nanobody vid svansstycket (Fc‑regionen) av mänskligt IgG1, vilket skapade större antikroppsliknande molekyler med bättre stabilitet i blodomloppet. De konstruerade också en ”bispecifik” version som bär både AM1‑1 och AM1‑4 i en enda IgG‑lik molekyl. Laboratorietester visade att dessa nanobody‑IgG‑fusionsproteiner binder till Api m 1 med extremt hög affinitet och, när de är närvarande, kraftigt minskar bindningen av IgE från blodet hos honungsbiet‑allergiska patienter till Api m 1. I cellbaserade tester minskade de aktiveringen av basofiler, de immunceller som normalt reagerar kraftigt när de utsätts för Api m 1 hos allergiska individer.
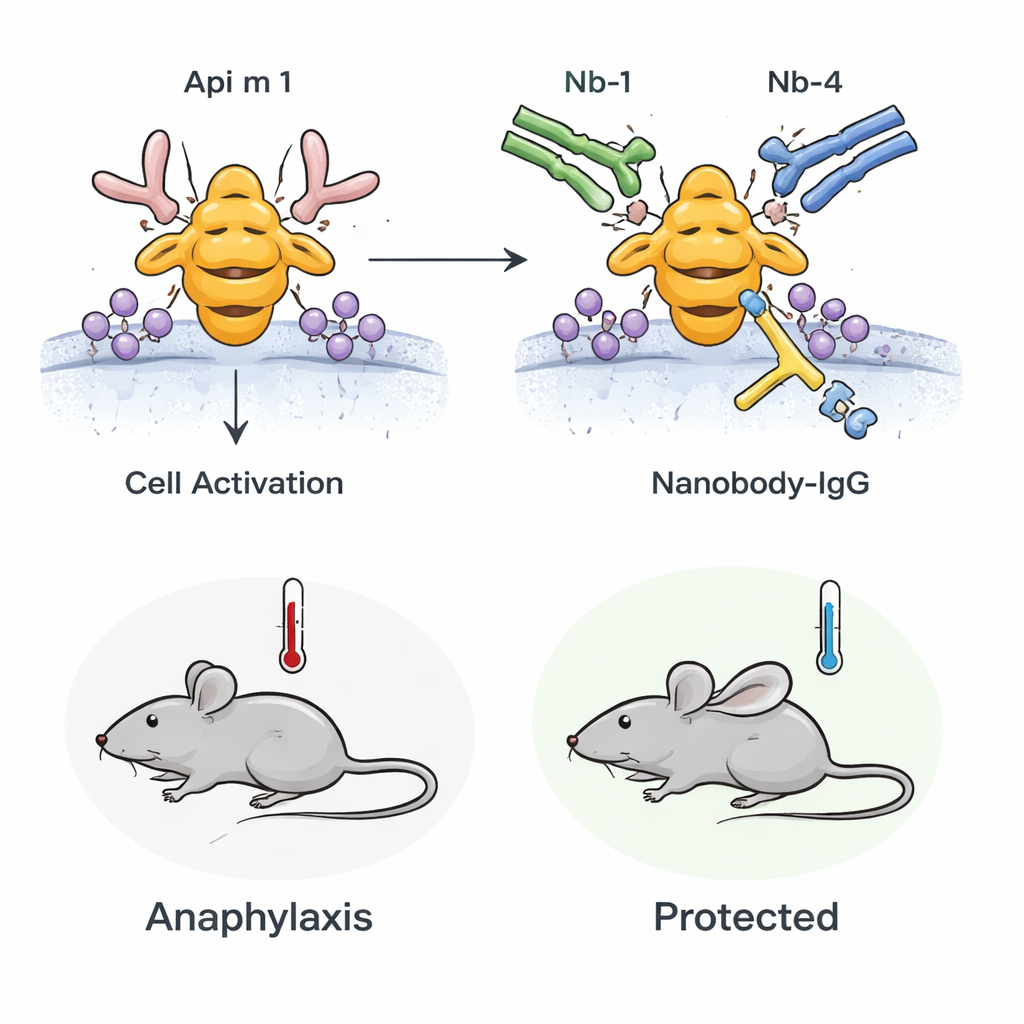
Från provrör till levande djur
Teamet undrade därefter om denna blockerande effekt skulle hålla i en levande organism. De använde möss sensibiliserade mot honungsbietoxin så att deras immunsystem reagerade på Api m 1 på ett sätt som efterliknar mänsklig allergi. När dessa möss utsattes för Api m 1 utvecklade de tecken på anafylaxi, inklusive kroppstemperaturfall och markörer för mastcellsaktivering i blodet. Men om mössen förbehandlades med den bispecifika nanobody‑IgG:n minskade både temperaturfallet och mastcellsaktiveringen avsevärt. Detta visar att förhandsbefintliga, högaffina blockerande antikroppar kan dämpa den systemiska allergiska reaktionen mot Api m 1 in vivo.
Vad detta kan innebära för personer med bistickallergi
Sammantaget visar studien att noggrant designade nanobody‑baserade IgG‑molekyler kan blockera både de allergena och enzymatiska effekterna av Api m 1, huvudsakliga boven i honungsbietoxinallergi. För patienter öppnar detta möjligheten till en säsongsbetonad, passiv immunisering: några injektioner av sådana antikroppar under månaderna då bistick är mest sannolika skulle kunna ge temporärt skydd mot svåra reaktioner, utan det långvariga åtagandet och riskerna med traditionell venomimmunterapi. Även om mer arbete krävs för att bredda angreppssättet till andra giftkomponenter och för att testa säkerhet och effektivitet hos människor, erbjuder denna nanobody‑strategi ett precist nytt sätt att skydda utsatta individer från farliga bistick.
Citering: Aagaard, J.B., Gandini, R., Ballegaard, AS.R. et al. Nanobody-based IgG simultaneously inhibit the allergenic and enzymatic activity of the dominant honeybee venom allergen. Nat Commun 17, 1814 (2026). https://doi.org/10.1038/s41467-026-69572-0
Nyckelord: allergi mot bistick, nanobodies, passiv immunterapi, fosfolipas A2, förebyggande av anafylaxi