Clear Sky Science · sv
Kooperativ klämma-medierad promotorigenkänning av poxvirus RNA‑polymeras och dess TBP/TFIIB‑lika partner
Hur ett virus omkopplar genkontroll inne i våra celler
Poxvirus, däribland det virus som historiskt orsakade smittkoppor, utför all sin genexpression i cytoplasman i våra celler, långt från cellens eget DNA‑kontrollcenter i kärnan. För att klara detta tar de med sig en egen mini‑"genfabrik". Denna studie avslöjar, på atomär nivå, hur ett sådant virus, Vaccinia, slår på en specifik våg av sina gener mitt under infektionen med hjälp av ett oväntat klämformigt protein som samarbetar med det virala kopieringsmaskineriet.
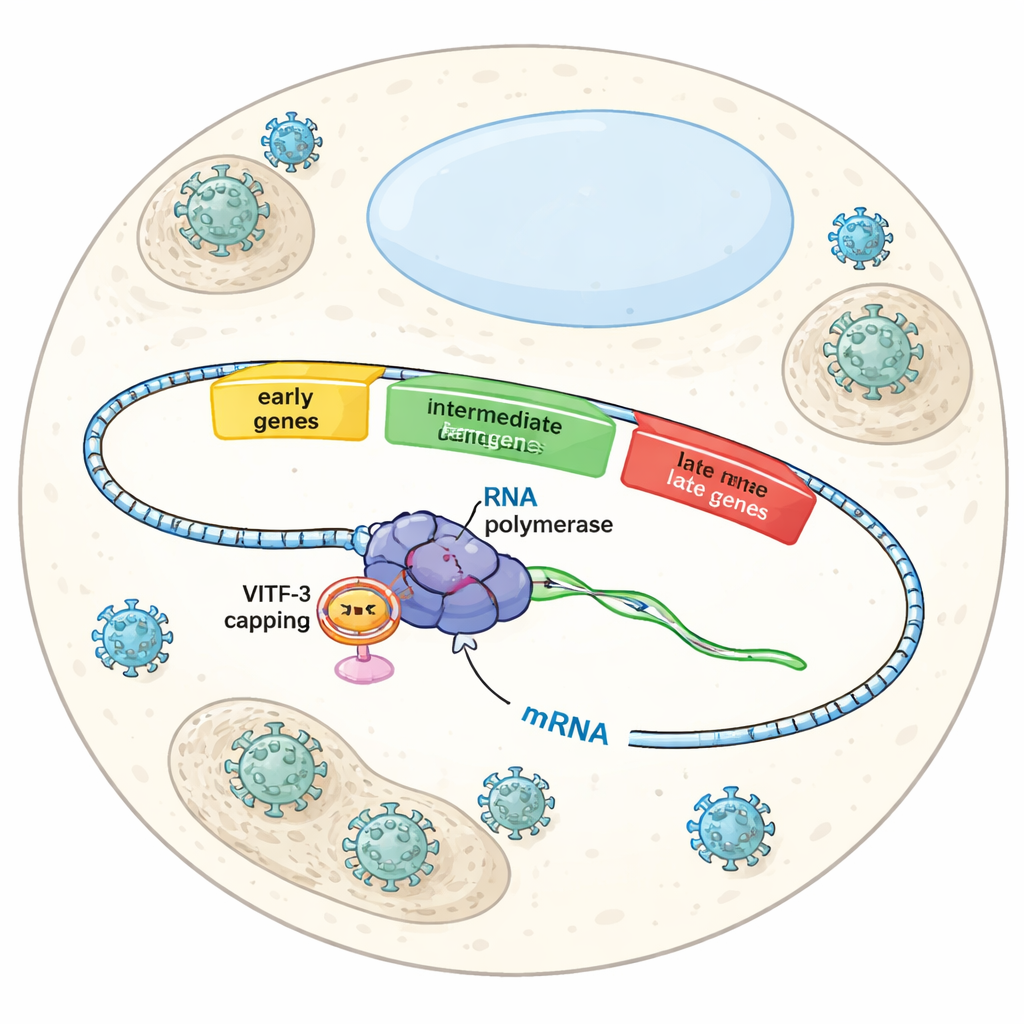
Tre vågor i en viral övertagning
När Vaccinia infekterar en cell slår det inte på alla sina gener samtidigt. Istället följer det ett noggrant tidsbestämt manus med tidiga, intermediära och sena gener. De tidiga generna förbereder marken för viral replikation, de intermediära generna hjälper till att bygga upp maskineriet för att skapa nya viruspartiklar, och de sena generna slutför montering och packning. Varje våg är beroende av samma virala RNA‑polymeras — enzymet som läser DNA för att skapa RNA — men olika hjälpfaktorer talar om för polymeraset vilken grupp gener som ska aktiveras i varje steg. Hittills hade forskare en relativt god förståelse för kontrollen av tidiga gener, men hur viruset specifikt känner igen och aktiverar de intermediära generna var fortfarande ett mysterium.
En ringformad hjälpare som behöver en partner
Forskarna fokuserade på ett tvådelat protein kallat VITF‑3, känt för att vara nödvändigt för att slå på intermediära gener. Många organismer, inklusive människor, använder ett par proteiner kallade TBP och TFIIB för att vägleda sitt RNA‑polymeras till rätt startpunkt på DNA. Teamet visade att VITF‑3 är en starkt ombyggd version av samma urgamla par. Men till skillnad från sina cellulära motsvarigheter binder VITF‑3 inte DNA på egen hand. Istället hakar dess två subenheter i varandra och bildar en sluten ring som i sig är inert gentemot DNA om inte det virala RNA‑polymeraset är närvarande. Det här var oväntat, eftersom i de flesta system binder den TBP‑lika komponenten först promotor‑DNA och rekryterar sedan polymeraset; här verkar viruset ha omvänt händelseordningen.
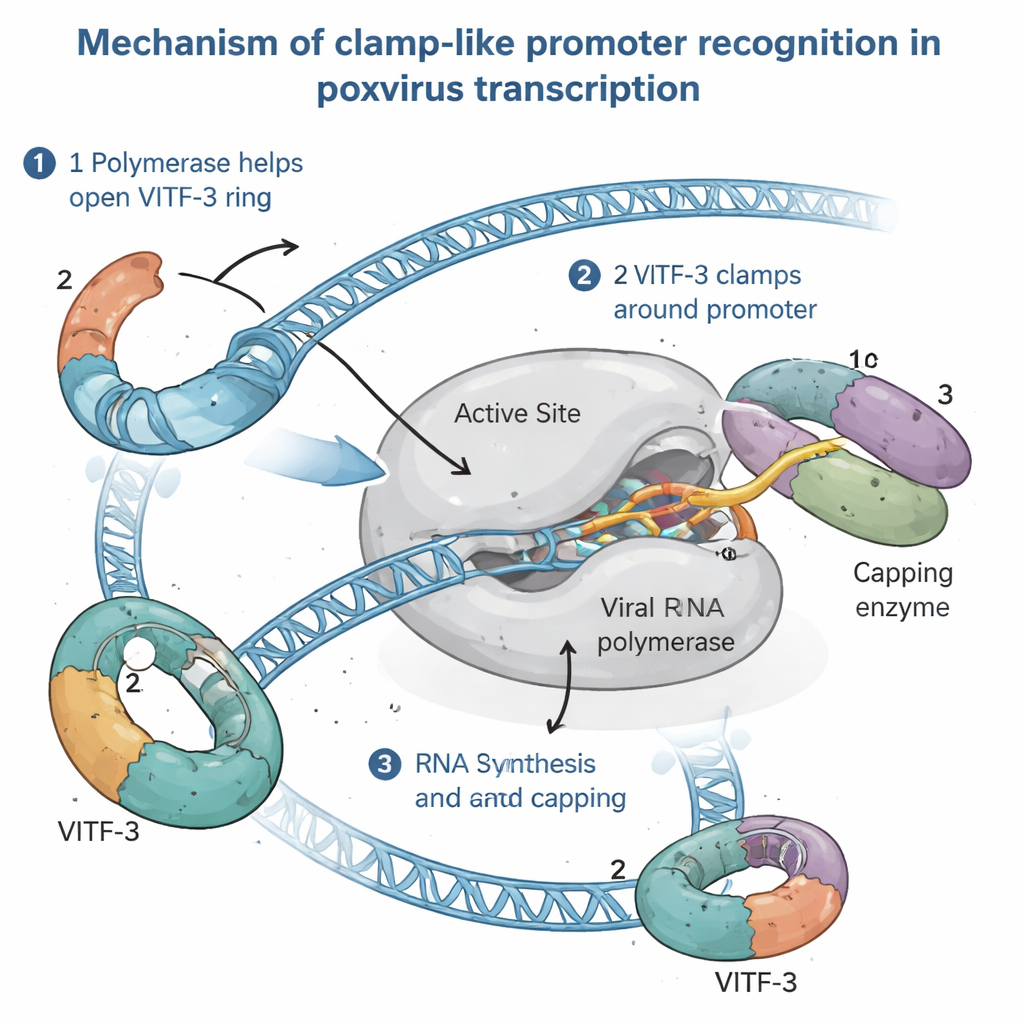
Att se det intermediära transkriptionsmaskineriet i arbete
För att förstå hur denna ovanliga uppsättning fungerar isolerade författarna det kompletta intermediära pre‑initieringskomplexet — den sammansättning som ligger precis innan RNA‑syntesen startar — från infekterade humana celler. Med hjälp av högupplöst kryoelektronmikroskopi visualiserade de komplexet med ungefär 2,4 Ångströms detalj, tillräckligt fint för att se sidokedjor på aminosyror och individuella DNA‑baser. Bilderna visade det virala RNA‑polymeraset som greppade promotor‑DNA:t, medan VITF‑3 bildade en tät ring runt en AT‑rik DNA‑sekvens strax uppströms startpunkten. Denna ring böjer DNA:t skarpt, med ungefär 90 grader, och matar in det i en fåra i polymeraset. Samtidigt är ett viralt cappingsenzym — ansvarigt för att lägga till det skyddande mössan på 5′‑änden av viralt RNA — dockat på polymeraset och redo att modifiera nysyntetiserade transkript så fort de framträder.
En kläm‑laddar‑mekanism lånad i anda
Genom att kombinera strukturella ögonblicksbilder med biokemiska tester föreslår studien att det virala RNA‑polymeraset aktivt lastar VITF‑3 på DNA, och fungerar som en "kläm‑laddare". Först binder polymeraset till en intermediär promotor och hjälper till att prångla upp VITF‑3‑ringen. Sedan stänger det, tillsammans med cappingsenzymet, ringen runt den AT‑rika regionen och klämmer fast komplexet på plats. DNA:t smälter nära startpunkten, och polymeraset läser direkt en kort fyrabokstavssignal (en TAAA‑motif) som markerar exakt var RNA‑syntesen ska börja. I takt med att RNA:t växer följer det samma bana som en del av VITF‑3 upptog i initialkomplexet, så det framväxande RNA:t pressar troligen VITF‑3 åt sidan, vilket tillåter polymeraset att lämna promotorn och fortsätta längs genen medan VITF‑3 kan bli kvar för att snabba upp återanvändning av samma promotor.
Vad detta betyder för förståelsen av och riktade insatser mot poxvirus
Enkelt uttryckt visar detta arbete att Vaccinia‑virus har omvandlat en universell modul för genkontroll till en klämma som endast greppar DNA när dess eget RNA‑polymeras säger åt den att göra det. Den smarta vridningen gör att viruset kan använda ett enda kärnenzym för att driva tre väldigt olika transkriptionsprogram, helt enkelt genom att byta ut scen‑specifika hjälpare. Eftersom samma typ av faktorer är bevarade hos många poxvirus, inklusive humana patogener, erbjuder den nyupptäckta kläm‑laddar‑mekanismen och den unika VITF‑3‑ringen konkreta strukturella mål för antivirala strategier som syftar till att störa virusets förmåga att tajma och kontrollera sina gener under infektion.
Citering: Jungwirth, S., Bartuli, J., Lamer, S. et al. Cooperative clamp-mediated promoter recognition by poxviral RNA polymerase and its TBP/TFIIB-like partner. Nat Commun 17, 1648 (2026). https://doi.org/10.1038/s41467-026-69571-1
Nyckelord: poxvirustranskription, Vaccinia‑virus, RNA‑polymeras, promotorigenkänning, transkriptionsfaktorer