Clear Sky Science · sv
En syntetisk cell med integrerad DNA-självreplikation och lipidsyntes
Bygga liv från grunden
Vad gör en levande cell mer än bara en påse molekyler? Ett svar ligger i dess förmåga att kopiera sina genetiska instruktioner och bygga sitt eget skyddande membran. Denna studie tar ett viktigt steg mot att återskapa detta i laboratoriet. Författarna designar små fetthaltiga bubblor, så kallade liposomer, som kan läsa en DNA-bit, kopiera den och tillverka nytt membranmaterial—allting inuti samma miniatyra rum. Deras arbete för oss närmare konstgjorda celler som kan växa, anpassa sig och kanske en dag evolvera självständigt.
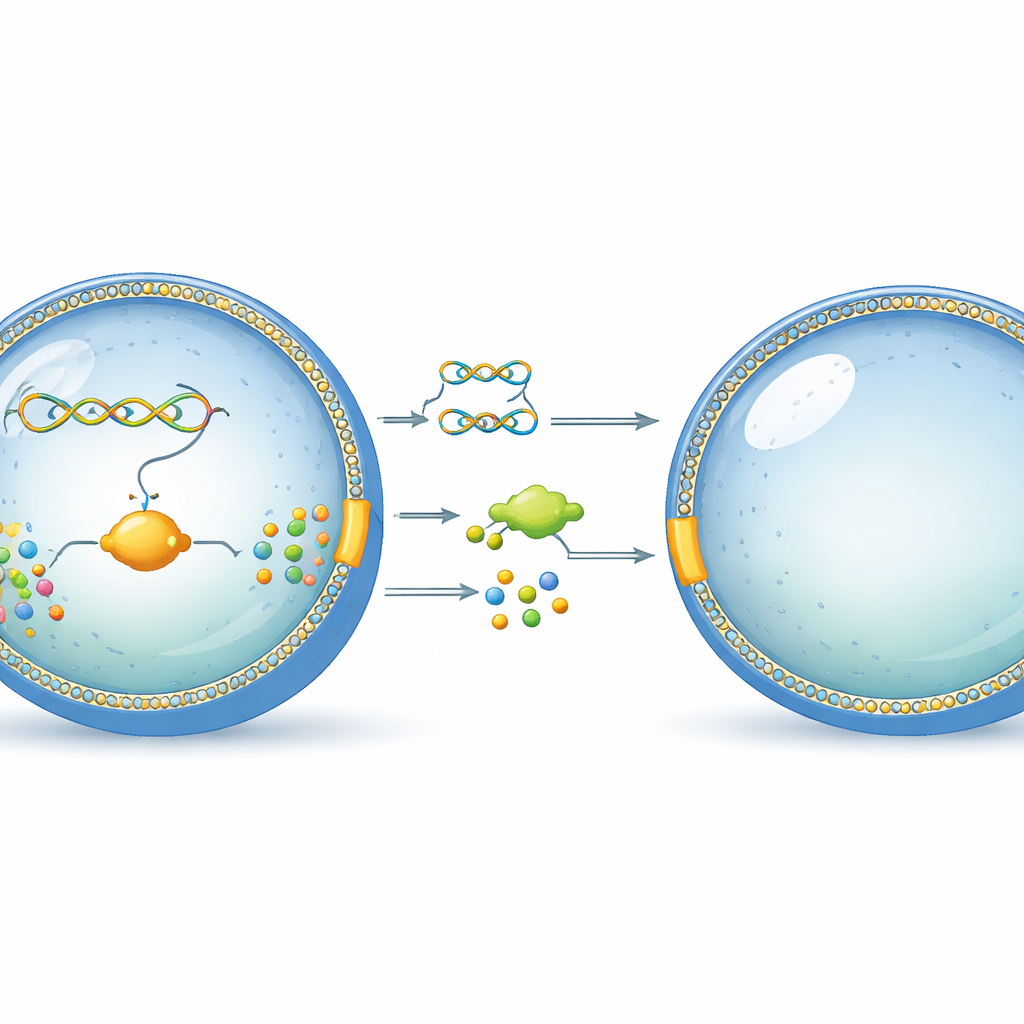
En liten bubbla som beter sig som en cell
Forskarna börjar med enkla, cellstora bubblor gjorda av fosfolipider, samma typ av molekyler som bildar den yttre skalet hos riktiga celler. I dessa bubblor packar de en noggrant designad DNA-sträng och en uppsättning renade cellulära maskiner som kan läsa DNA och tillverka proteiner. Denna uppställning, kallad ett cellfritt expressionssystem, fungerar som den avskalade kärnan i en levande cell och kan omvandla genetisk information till fungerande molekyler utan någon levande organism närvarande. Nyckelidén är att placera allt inuti liposomen så att det genetiska programmet och dess produkter hålls ihop, ungefär som i en naturlig cell.
Ett skräddarsytt DNA-program med två uppgifter
I centrum för deras syntetiska cell finns en specialbyggd DNA-molekyl som författarna kallar DNArep-PLsyn. Detta DNA bär instruktioner för sex proteiner. Två av dem kommer från ett virus som infekterar bakterier och kan tillsammans kopiera DNA:t självt, vilket utgör en inbyggd självreplikationsmodul. De övriga fyra kommer från tarmbakterien E. coli och bildar en reaktionskedja som omvandlar enkla utgångsmaterial till en specifik fosfolipid som används i membran. För att sätta ihop detta ovanliga genom fick teamet sy ihop DNA-bitar i provrör och i jästceller, och sedan omvandla resultatet till en linjär DNA-sträng som den virala kopieringsmaskineriet kan känna igen och replikera.
Tillverkning och testning av syntetisk aktivitet
När DNA:t och det proteinframställande maskineriet är förseglade inne i liposomerna värms bubblorna till olika temperaturer och får löpa fritt. Teamet kontrollerar sedan vad som hänt med hjälp av fluorescerande markörer: ett färgämne lyser upp när det binder DNA och visar hur mycket DNA som finns, och ett annat binder till den nya fosfolipiden om den produceras och införlivas i membranet. Med flödescytometri och högupplöst mikroskopi kan de analysera tiotusentals enskilda vesiklar. De finner att många bubblor framgångsrikt kopierar genomet, många andra tillverkar nya membranbyggstenar, och en mindre men betydande andel klarar att göra båda samtidigt. Ytterligare tester med DNA-kvantifiering och masspektrometri bekräftar att hela genomet amplifieras och att nya fosfolipidmolekyler verkligen syntetiseras, om än i modest mängd.
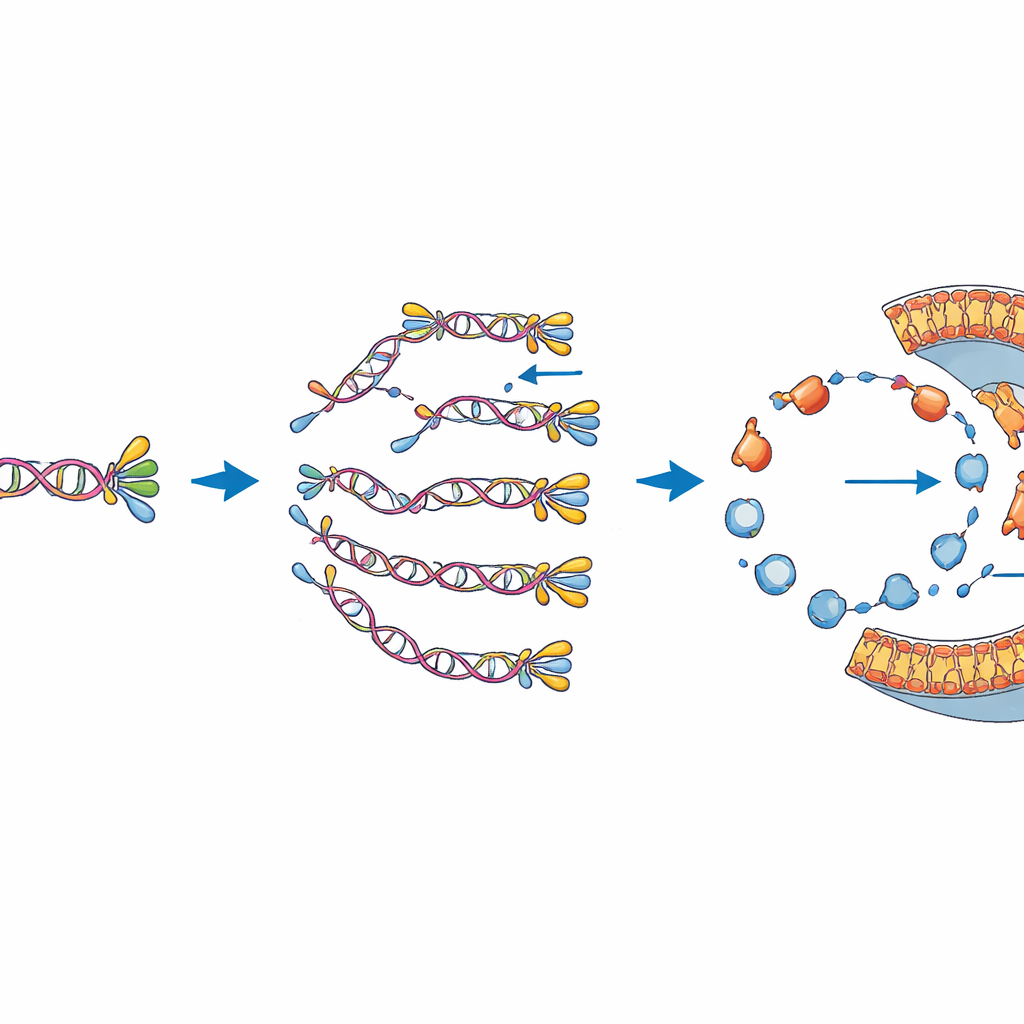
Att balansera två väsentliga uppgifter
Författarna undersöker sedan hur dessa två funktioner påverkar varandra. Genom att slå av och på DNA-kopierings- eller membrantillverkningens kemi via deras nödvändiga ingredienser visar de att varje process i stor utsträckning kan fungera utan att störa den andra. Men när båda modulerna kodas på samma DNA visar sig membransyntessidan vara mer skör: färre vesiklar uppvisar denna aktivitet jämfört med vesiklar som bara bär de lipidrelaterade generna. På samma sätt kopieras det kombinerade genomet inte lika effektivt som en mindre version som innehåller endast DNA-replikationsgenerna. Detta tyder på att även i detta avskalade system finns konkurrens om delade resurser och fysisk plats på DNA:t, vilket speglar trade-offs som ses i riktiga celler.
Förberedelser för evolution i provröret
För att gå bortom en enstaka demonstration designar teamet sitt system så att det i princip kan förbättras genom evolution. De framställer renare, mer pålitliga DNA-varianter med hjälp av plasmider odlade i jäst och bakterier, vilket ökar andelen fullt funktionella syntetiska celler. De visar också att det är möjligt att kapsla in, selektera och återvinna genom från vesiklar som utför både DNA-kopiering och membransyntes. Detta banar väg för framtida cykler där något olika genom konkurrerar, och de som presterar bättre berikas och kopieras.
Varför detta är viktigt för förståelsen av liv
I vardagliga termer har forskarna byggt en mikroskopisk bubbla som kan läsa sitt eget recept, kopiera det och använda det för att laga och utöka sitt yttre skal. Även om dessa syntetiska celler ännu inte kan växa mycket eller dela sig som levande organismer, visar arbetet att livets kärnegenskaper—informationslagring, självkopiering och grundläggande självkonstruerande—kan kombineras i ett enkelt, kontrollerbart paket. Detta lägger viktig grund för att utforska hur liv kan ha uppstått ur icke-levande kemi och för att konstruera konstgjorda celler som utför användbara uppgifter, från smart läkemedelsleverans till självförnyande små fabriker.
Citering: Restrepo Sierra, A.M., Ramirez Gomez, F., van Tongeren, M. et al. A synthetic cell with integrated DNA self-replication and lipid biosynthesis. Nat Commun 17, 2727 (2026). https://doi.org/10.1038/s41467-026-69531-9
Nyckelord: syntetiska celler, DNA-självreplikation, lipidsyntes, konstgjort liv, bottom-up-biologi