Clear Sky Science · sv
Laserinterstitiell termoterapi och adjuvant pembrolizumab vid återkommande höggradig astocytom: en fas 1/slumpmässig fas 2b-studie
Varför denna hjärntumörstudie är viktig
Återkommande höggradig astocytom, inklusive glioblastom, är en av de mest dödliga hjärntumörerna, och dagens behandlingar håller sällan sjukdomen under kontroll länge. Denna studie prövar en tvåstegsstrategi som använder värme från en laser för att förstöra tumörvävnad och öppna hjärnans försvar, följt av ett immunläkemedel som hjälper kroppens egna T‑celler att angripa kvarvarande cancer. För patienter och familjer som står inför denna diagnos undersöker arbetet om ett minimalt invasivt ingrepp kan förvandla en nästan okänslig tumör till en som slutligen svarar på immunterapi.
En ny metod för att angripa svåra hjärntumörer
Patienterna i denna prövning hade alla höggradiga astocytom som återkommit efter standardbehandling, som vanligtvis innefattar operation, strålning och kemoterapi. Forskarna fokuserade på två verktyg. Det första, laserinterstitiell termoterapi (LITT), är ett nyckelhålsingrepp där en tunn sond leds in i tumören under MRI‑vägledning och används för att värma upp och döda cancervävnad samtidigt som mycket av den omgivande hjärnan sparas. Det andra verktyget är pembrolizumab, ett brett använt immunterapiläkemedel som blockerar PD‑1, en molekylär ”broms” som ofta hindrar T‑celler från att angripa tumörer. Tidigare försök att använda sådana läkemedel ensamma mot dessa hjärntumörer har varit nedslående. Teamet frågade därför om lasern först kunde förbereda tumören och immunsystemet för att bättre svara på pembrolizumab. 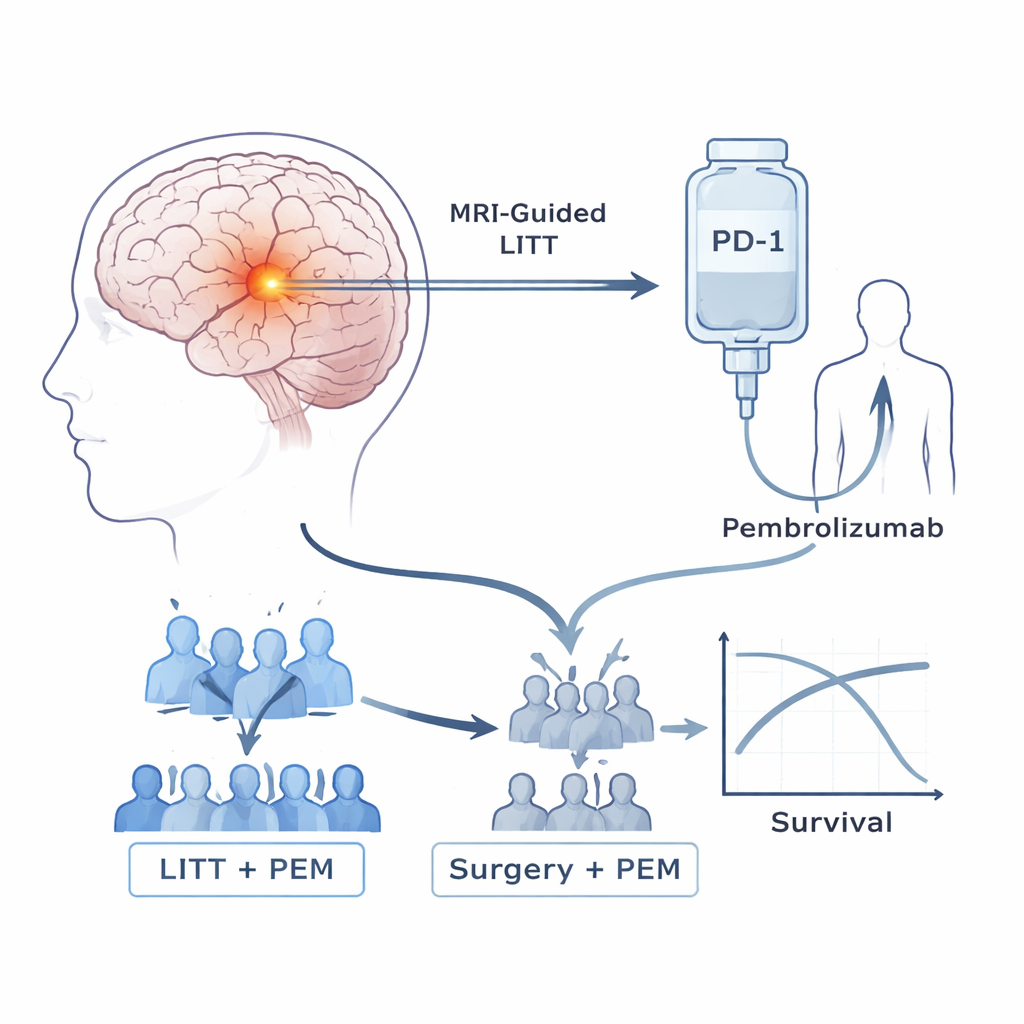
Hur kliniska prövningen genomfördes
Studien inleddes med en liten säkerhetsfas, som visade att patienter säkert kunde få pembrolizumab var tredje vecka efter LITT, utan dosbegränsande biverkningar. Den gick sedan in i en fas 2b‑prövning. Inledningsvis lottades patienterna till en av två grupper: LITT följt av pembrolizumab, eller konventionell upprepad hjärnoperation utan laser, följt av pembrolizumab. När utanförstående data ökade som indikerade att kirurgi plus immunterapi gav liten nytta på egen hand, granskade en oberoende kommitté tidiga resultat från denna prövning. När de såg tecken på att icke‑lasergruppen presterade dåligt medan LITT‑gruppen verkade leva längre, avbröt de fortsatt randomisering och alla senare patienter fick laser‑plus‑läkemedelskombinationen.
Vad som hände med överlevnad och tumörkontroll
Bland 39 patienter som fick behandling enligt plan levde de som erhöll LITT plus pembrolizumab märkbart längre än de som hade kirurgi plus pembrolizumab. Median överlevnad var omkring 11,8 månader med den kombinerade LITT‑metoden, jämfört med 5,2 månader med enbart kirurgi, och ingen av kirurgipatienterna var vid liv vid 18 månader jämfört med 42 % av dem i LITT‑gruppen. Tiden innan tumören började växa igen förbättrades också, från 1,6 månader i kirurgigruppen till 4,5 månader med LITT. Ungefär 27 % av LITT‑behandlade patienter uppvisade mätbar tumörminskning och 70 % uppnådde åtminstone temporär sjukdomskontroll, medan alla patienter som genomgick icke‑laseroperation plus pembrolizumab drabbades av progression. Biverkningar från den kombinerade behandlingen var mestadels milda och hanterbara, med vissa fall av diarré, muskelsvaghet och förhöjda levervärden, men inga behandlingsrelaterade dödsfall.
Vad immunsystemet gjorde
För att förstå varför kombinationen kunde fungera undersökte forskarna noggrant blodceller över tid med enkelcells‑RNA‑sekvensering och spårning av T‑cellsreceptorer. Efter LITT såg de att en specifik grupp av medfödda immunceller, kallade icke‑klassiska monocyter, gick över i ett mer aktivt tillstånd kopplat till migration, inflammation och interaktion med T‑celler—förändringar som inte observerades efter standardkirurgi. När pembrolizumab sedan startades visade patienter som överlevde längre starka vågor av CD8‑T‑cellsaktivering och klonal expansion, vilket betyder att många identiska T‑celler som riktar sig mot samma antigener mångfaldigades. Dessa T‑celler tenderade att gå in i minnes‑ och effektorstater som kan känna igen och döda tumörceller, istället för att bli utmattade och ineffektiva. Långtidsöverlevande visade också en minskning av IDO‑1, en molekyl kopplad till immunsuppression, vilket antyder att kombinationen kan lätta flera lager av immunskydd.
Vad detta kan betyda för patienter
För personer som lever med återkommande höggradig astocytom tyder detta arbete på att användning av MRI‑styrd laserablation för att avlasta tumören, temporärt luckra upp blod‑hjärnbarriären och släppa tumörfragment i cirkulationen kan skapa förutsättningar för att immunterapi ska fungera där den vanligtvis misslyckas. Genom att tända en ”signalfyr” för immunsystemet och sedan ta bort PD‑1‑bromsen med pembrolizumab verkar kombinationen framkalla mer bestående T‑cellsvar och förlänga överlevnad i en cancer med mycket få alternativ. Eftersom studien var relativt liten och randomiseringen avslutades tidigt betonar författarna att större, fullständigt kontrollerade prövningar fortfarande behövs. Ändå pekar resultaten mot en lovande ny strategi: att kombinera precist riktad fysisk tumörförstörelse med immunläkemedel för att omvandla en kall, resistent hjärntumör till en som kroppen slutligen kan känna igen och bekämpa.
Citering: Campian, J.L., Le, S.B., Ghiaseddin, A. et al. Laser interstitial thermal therapy and adjuvant pembrolizumab in recurrent high-grade astrocytoma: a Phase 1/randomized Phase 2b trial. Nat Commun 17, 1763 (2026). https://doi.org/10.1038/s41467-026-69522-w
Nyckelord: glioblastom, laserablation, pembrolizumab, immunterapi, hjärntumör